2026年1月6日,湖南农业大学谭碧娥、王婧团队在《Microbiome》发表题为 “Ningxiang pig-derived Enterococcus hirae protects against E. coli-induced gut dysbiosis and inflammation via acetate/propionate-MyD88-NF-κB axis in piglets” 的研究性论文。

该研究结合体内外实验、微生物组学、代谢组学、分子对接及公共数据集分析等技术,系统探究了宁乡猪源海氏肠球菌缓解大肠杆菌诱导仔猪肠道炎症的作用及分子机制。研究证实,该菌株可通过恢复肠道菌群平衡、促进乙酸和丙酸等短链脂肪酸合成,进而抑制 MyD88-NF-κB 信号通路激活,减少促炎细胞因子表达,同时该机制在克罗恩病患者中存在潜在临床相关性,为细菌性肠道炎症的益生菌和后生元治疗提供了新的理论依据和候选菌株。百迈客生物为该研究提供了细菌全基因组和16S rRNA基因测序服务。
研究背景
肠道炎症受菌群失调、饮食、免疫异常等因素诱发,克罗恩病等炎症性肠病的发生发展与肠道菌群失调密切相关,大肠杆菌是引发肠道炎症的重要致病菌,亟需研发有效策略抑制其增殖。益生菌是缓解肠道炎症的潜在手段,乳酸菌及短链脂肪酸等益生菌代谢产生的后生元备受关注,但其生物活性和作用机制尚未完全阐明。啮齿类模型无法充分反映人类肠道特征,而猪的肠道菌群、免疫反应与人类相近,是研究肠道疾病的适宜模型。
研究结果
♦ 低腹泻率宁乡仔猪的核心微生物标志物鉴定及海氏肠球菌的益生菌潜力验证
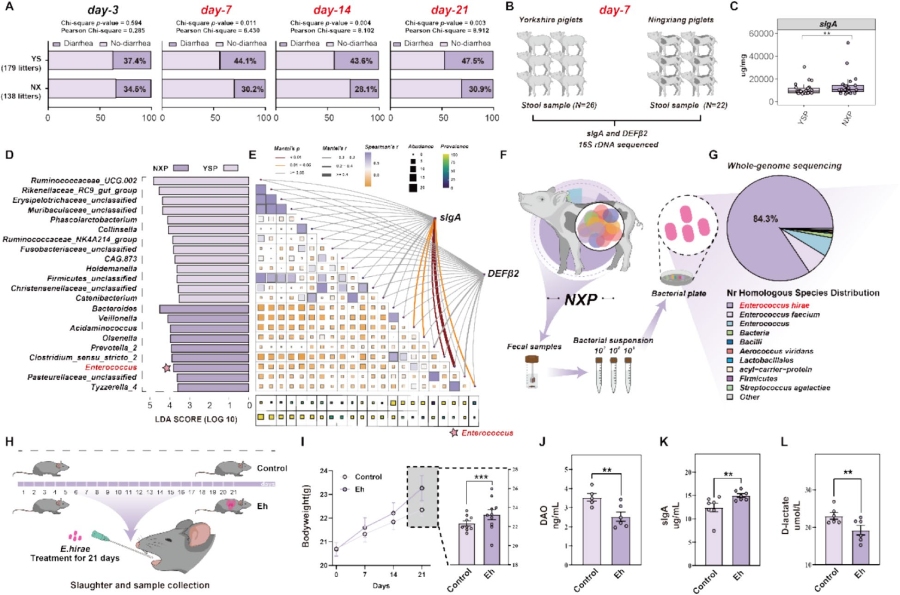
对比宁乡仔猪(138 窝)和约克夏仔猪(179 窝)哺乳期腹泻发生率,发现宁乡仔猪在7-21日龄腹泻率显著更低(日龄7天:30.2% vs 44.1%;日龄21天:30.9% vs 47.5%);7日龄粪便样本检测显示,宁乡仔猪分泌型免疫球蛋白A(sIgA)浓度显著高于约克夏仔猪,而防御素β2(DEFβ2)浓度无显著差异。16S rRNA基因测序分析表明,两种仔猪肠道菌群结构存在显著分离,宁乡仔猪肠道内拟杆菌门、变形菌门、梭杆菌门丰度更高,厚壁菌门丰度更低;属水平上,梭杆菌属、拟杆菌属在宁乡仔猪中富集,而未分类毛螺菌科、未分类Muribaculaceae在约克夏仔猪中丰度更高。
通过线性判别分析效应量(LEfSe)筛选出9个差异丰度微生物,其中肠球菌属与宁乡仔猪sIgA水平呈强正相关(p<0.01,R²=0.651),且在其粪便中检出率接近100%。从健康宁乡仔猪粪便中分离该菌株,经全基因组测序鉴定为海氏肠球菌,其呈均一球形,细胞形态完整,可利用乳糖、棉子糖、麦芽糖等多种多糖碳水化合物。该菌株对模拟胃肠道环境(pH 8.0人工肠液)、高浓度胆盐(0.3%-0.4%)具有良好耐受性,抗生素敏感性检测显示其对青霉素、红霉素等常用抗生素可控,符合益生菌候选标准。
小鼠灌胃实验证实,口服该海氏肠球菌(10⁸ CFU / 只,连续3周)可显著增加小鼠体重,提升小肠绒毛长度和隐窝深度,降低血清二胺氧化酶(DAO)、D – 乳酸水平(肠屏障损伤标志物),升高血清sIgA水平,显著改善宿主肠道健康状态。
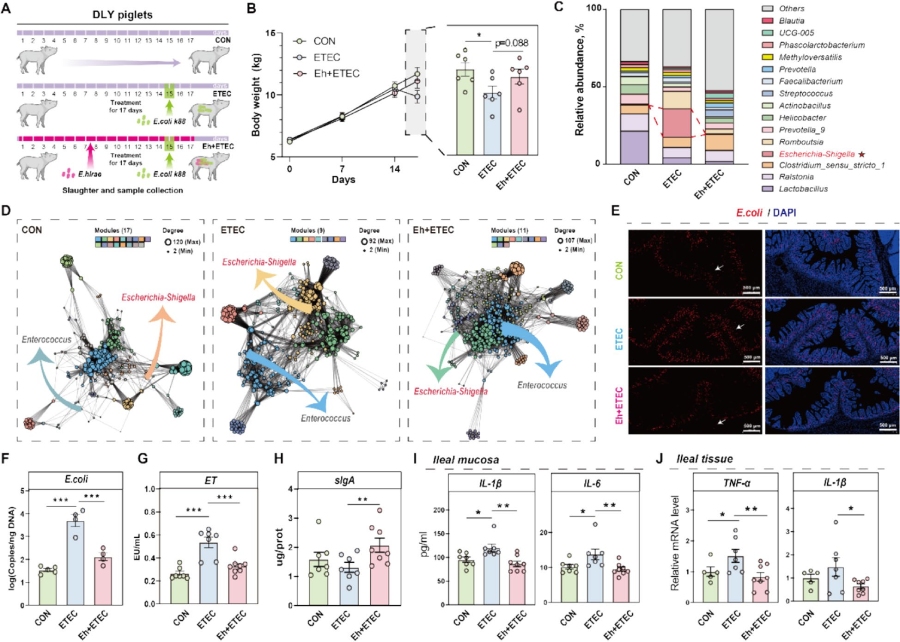
宁乡猪源海氏肠球菌抑制大肠杆菌定植并改善肠道炎症体外抑菌实验显示,该海氏肠球菌对大肠杆菌、沙门氏菌、金黄色葡萄球菌均有抑制作用,其中对大肠杆菌抑制效果最显著。构建大肠杆菌诱导的仔猪肠道炎症模型,将24日龄DLY仔猪分为对照组(CON)、大肠杆菌感染组(ETEC)、海氏肠球菌干预+大肠杆菌感染组(Eh+ETEC)。结果显示,海氏肠球菌可逆转大肠杆菌诱导的仔猪体重下降,16S rRNA基因测序表明其能恢复感染仔猪肠道菌群α、β多样性,降低变形菌门丰度,提升梭菌属、普雷沃氏菌属等有益菌丰度,显著降低埃希氏 – 志贺氏菌属的相对丰度和定植量。菌群网络分析显示,海氏肠球菌可恢复被大肠杆菌破坏的微生物群落稳定性,提升肠球菌属的生态地位。同时,该菌株能显著降低仔猪血清肠毒素(ET)水平,恢复回肠sIgA水平,降低回肠黏膜促炎细胞因子IL-1β、IL-6含量及TNF-α、IL-1β基因表达,有效缓解大肠杆菌诱导的肠道炎症和肠屏障损伤。
♦ 乙酸和丙酸是宁乡猪源海氏肠球菌发挥作用的核心功能代谢物
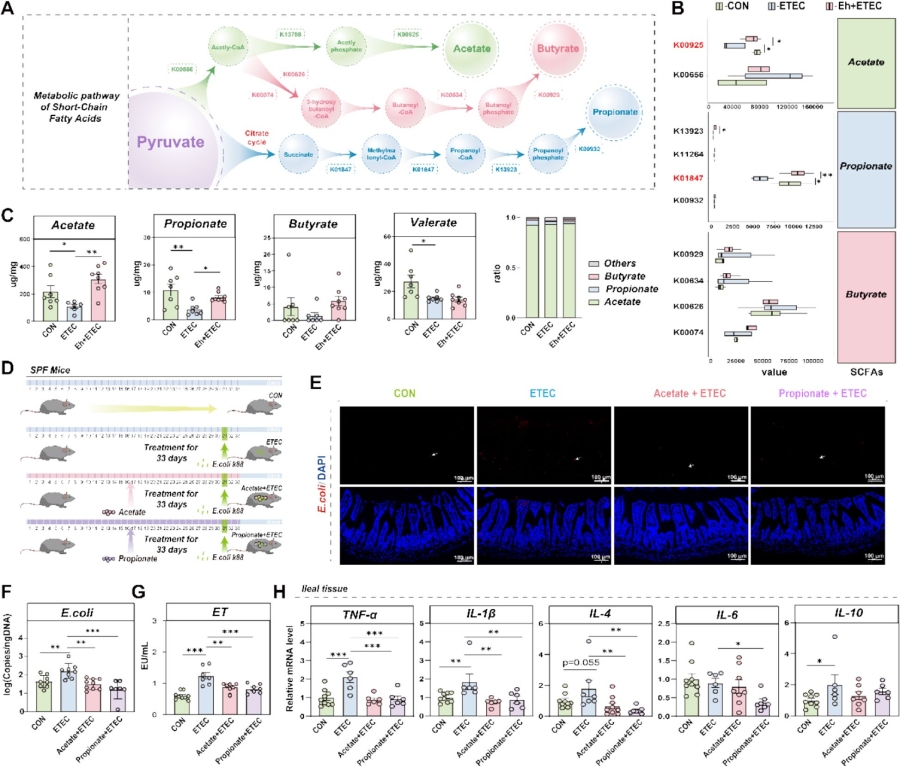
功能预测分析显示,海氏肠球菌可调控丙酮酸代谢通路,全基因组测序证实其携带乙酸、丙酸合成相关基因(K00926、K0184)。仔猪实验发现,大肠杆菌感染显著降低回肠食糜中乙酸、丙酸、戊酸浓度,而海氏肠球菌干预可特异性升高乙酸和丙酸水平(丁酸水平无显著变化),且宁乡仔猪粪便中乙酸、丙酸浓度显著高于约克夏仔猪。构建乙酸 / 丙酸干预的大肠杆菌感染小鼠模型,证实乙酸和丙酸可显著抑制大肠杆菌在小鼠回肠的黏附与定植,降低血清ET、DAO水平,减轻肠道形态损伤,且丙酸的作用效果更显著;同时可下调回肠组织TNF-α、IL-1β、IL-4、IL-6等促炎细胞因子基因表达,证实乙酸和丙酸是海氏肠球菌缓解肠道炎症的关键后生元。
♦ 乙酸和丙酸通过抑制MyD88-NF-κB通路缓解肠道炎症
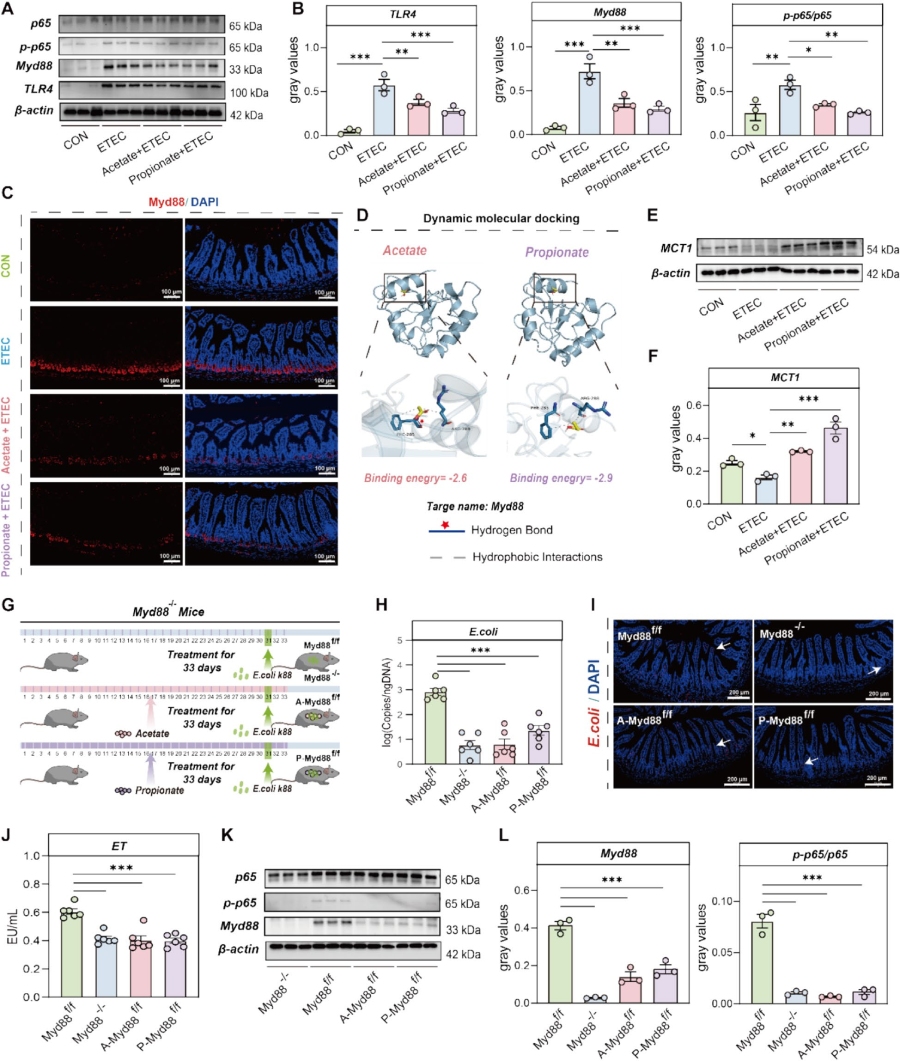
机制研究发现,大肠杆菌感染可显著激活仔猪、小鼠及IPEC-J2肠上皮细胞中 TLR4-MyD88-NF-κB信号通路,上调TLR4、MyD88、p65蛋白及基因表达,而海氏肠球菌、乙酸 / 丙酸干预可显著逆转该通路的异常激活。分子对接实验证实,乙酸和丙酸可与MyD88蛋白直接结合,结合位点为PHE-285和ARG288,其中乙酸与MyD88的PHE-285形成氢键,结合亲和力更强。乙酸和丙酸可上调大肠杆菌感染小鼠回肠组织单羧酸转运蛋白1(MCT1)表达,而海氏肠球菌可显著升高感染仔猪回肠SLC16A1(编码 MCT1)基因表达,提示SCFAs需通过MCT1转运进入细胞发挥作用。构建肠道上皮细胞特异性MyD88敲除(Myd88⁻/⁻)小鼠模型,证实敲除MyD88可达到与乙酸 / 丙酸干预相似的效果,显著抑制大肠杆菌定植、降低血清ET水平、缓解肠道炎症,证实乙酸 / 丙酸通过靶向MyD88-NF-κB通路发挥抗炎作用。
♦ 克罗恩病患者存在SCFAs下调及MyD88-NF-κB通路激活,具有临床相关性
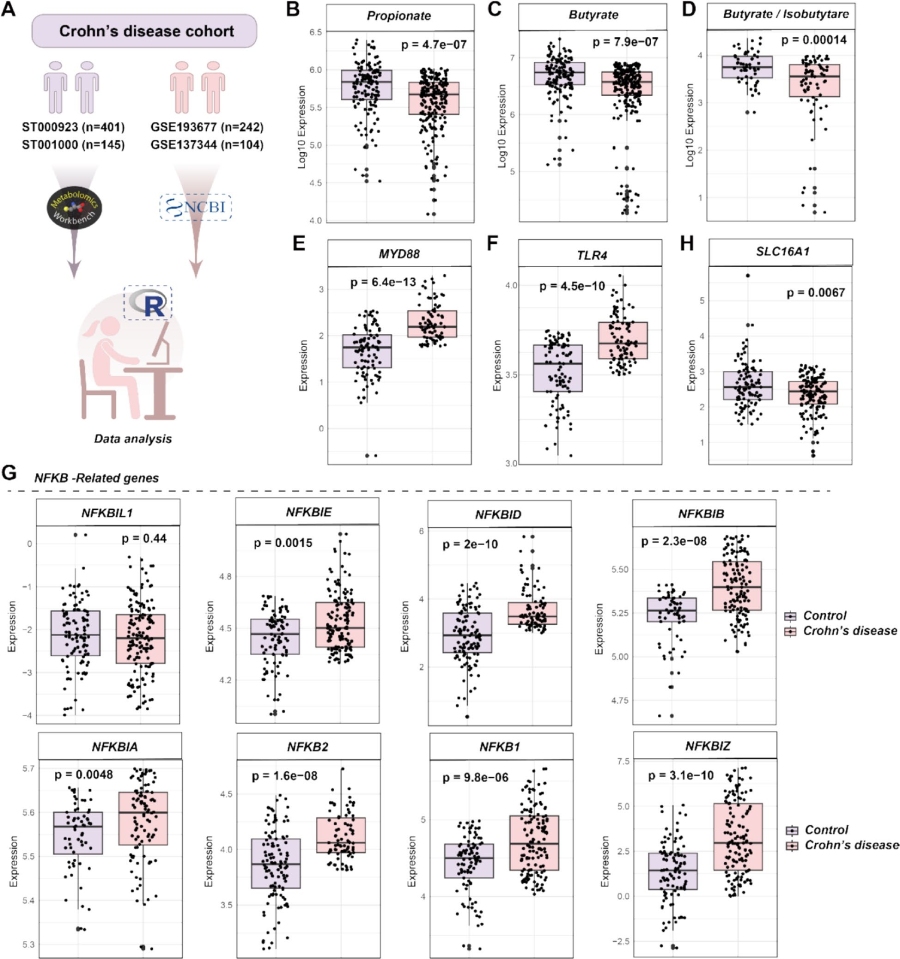
挖掘克罗恩病(CD)公共数据集,代谢组学分析显示,CD 患者粪便中丙酸、丁酸、丁酸 / 异丁酸浓度显著降低,且与CD发病概率呈显著负相关;另有研究证实 CD患者粪便乙酸水平(28.7±10.2 mmol/L)显著低于健康人群(50.7±14.3 mmol/L,p<0.01)。RNA-seq 数据显示,CD患者回肠组织中MyD88、TLR4 及 NF-κB家族相关基因(NFKBIA、NFKB2、NFKB1等)表达显著升高,SLC16A1基因表达显著降低,与动物实验中大肠杆菌感染模型的分子变化一致,提示海氏肠球菌 – 乙酸 / 丙酸 – MyD88-NF-κB 轴在人类肠道炎症疾病中具有潜在临床相关性。
研究总结
该研究指出大肠杆菌感染易破坏肠道稳态引发炎症,而抗生素、抗炎药等传统治疗存在耐药、菌群失调反复等局限,凸显了益生菌疗法的研究价值。该研究分离的宁乡猪源海氏肠球菌具优异益生菌特性,可通过产乙酸、丙酸调控肠道菌群,经 MCT1转运后结合MyD88,抑制NF-κB通路过度激活以缓解炎症,且首次证实该场景下乙酸、丙酸的调控作用优于丁酸。同时,克罗恩病患者的SCFA水平降低、MyD88-NF-κB通路激活的特征,验证了该机制的临床相关性。此外,研究也提及存在SCFA调控MyD88的分子细节未明、可能涉及其他代谢物 / 通路等局限,但该研究为细菌性肠炎及炎症性肠病的益生菌、后生元靶向治疗,提供了全新候选菌株与核心作用靶点,奠定了重要理论基础。
引用文献原文:https://link.springer.com/article/10.1186/s40168-025-02310-8
以上内容来源于益生相伴 菌之道,侵删






 京公网安备 11011302003368号
京公网安备 11011302003368号