华东理工大学赵黎明教授团队在国际期刊Gut Microbes上发表研究论文,题为“Targeted modulation of intestinal barrier and mucosal immune-related microbiota attenuates IgA nephropathy progression”。

该研究证明了部分肠道菌群与IgAN的之间的机制关系,为开发针对微生物群的食物干预措施改善IgAN提供科学依据。百迈客生物为该研究提供了全长16S rRNA测序服务。
研究背景
IgA肾病(IgAN)是全球最常见的免疫介导的原发性肾小球疾病,每年每10万成年人中至少有2.5例发病。具有显著的终身进展至终末期肾病(ESRD)的风险,约20%-40%的IgAN患者会在10至20年内进展至终末期肾病。因此迫切需要发现有效的治疗靶点和新的干预策略。
一般来说,人类肠道中居住着数以万亿的细菌,这些细菌以膳食营养为燃料,可合成多种生物活性化合物。这些微生物代谢物进一步向体内远处的器官发出信号,使它们能够与激素和免疫系统以及宿主的新陈代谢及其他功能相连接,肠道与宿主免疫系统之间复杂的相互作用影响着身体功能,这些功能将其与其他器官联系起来,并导致它们之间形成“轴”。
慢性肾脏病通常是进行性且不可逆的,肠道微生物群作为环境与人类之间的桥梁,在慢性肾脏疾病的发生和进展中发挥着根本性作用。IgA 肾病(IgAN)与肠道微生物群的平衡息息相关。然而,目前还不清楚肠道微生物群的变化是否会减弱IgAN或影响其进展。
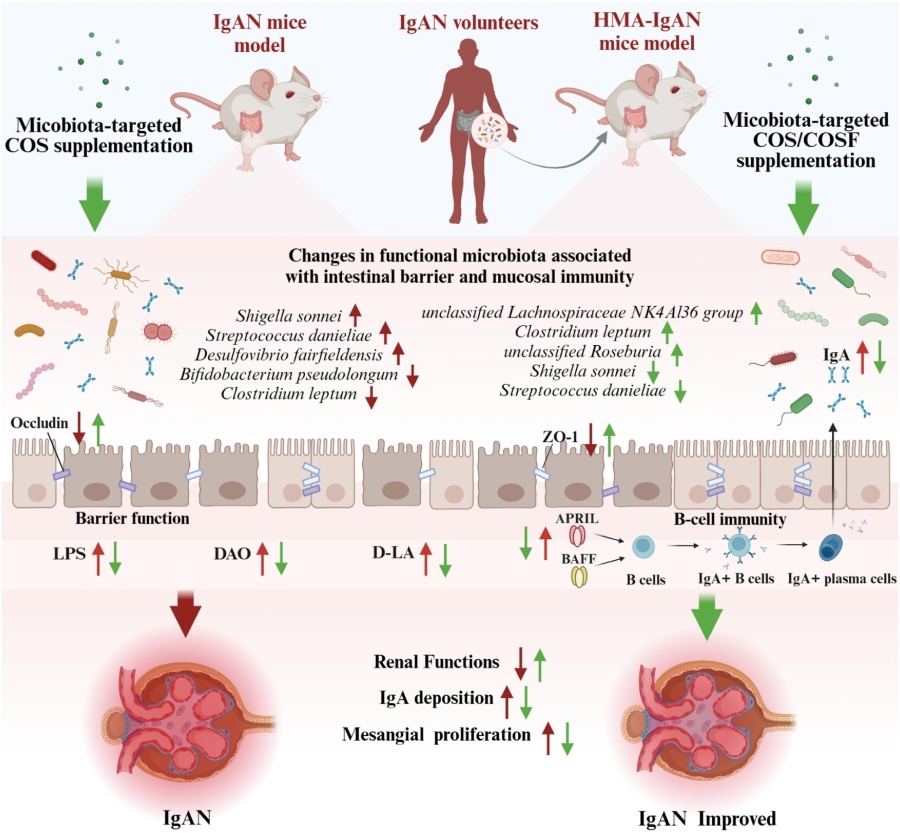
研究结果
♦ IgAN引起肾损伤和肾功能下降
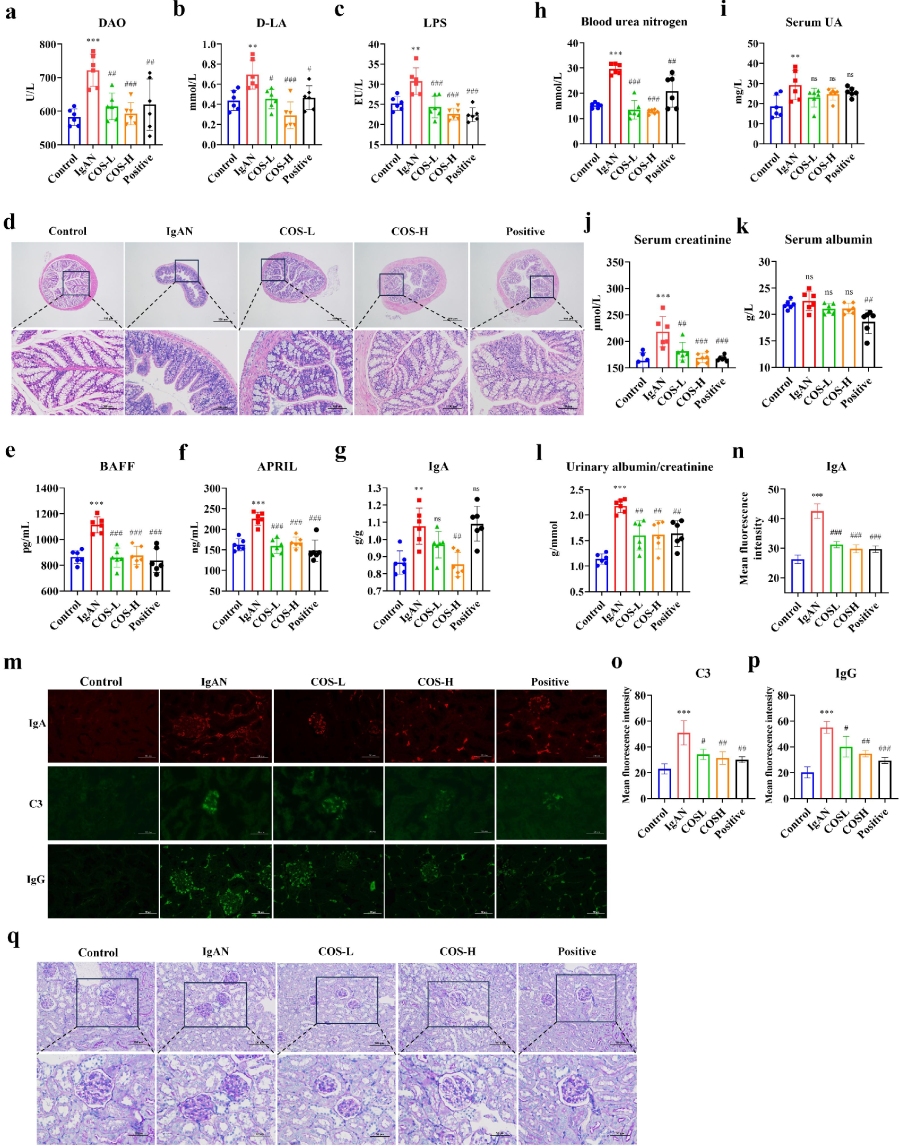
根据以上研究背景,作者首先确认了IgAN小鼠模型的成功建立。通过分析小鼠肾脏IgA免疫荧光染色,与对照组相比,IgAN组肾小球IgA(p < 0.001)、C3(p < 0.01)和IgG(p < 0.001)沉积显著增加。PAS染色显示,IgAN组肾小球系膜细胞增生、系膜基质增多及基底膜增厚。肾功能指标评估显示,与对照组相比,IgAN组小鼠血尿素氮(BUN)(p < 0.001)、尿酸(UA)(p < 0.01)、血清肌酐(Scr)(p < 0.01)、血白蛋白(BAL)(p < 0.05)及尿蛋白/肌酐比值(ACR)(p < 0.001)水平显著增加,IgAN组肾功能显著下降,这可能与肾脏结构损伤有关。
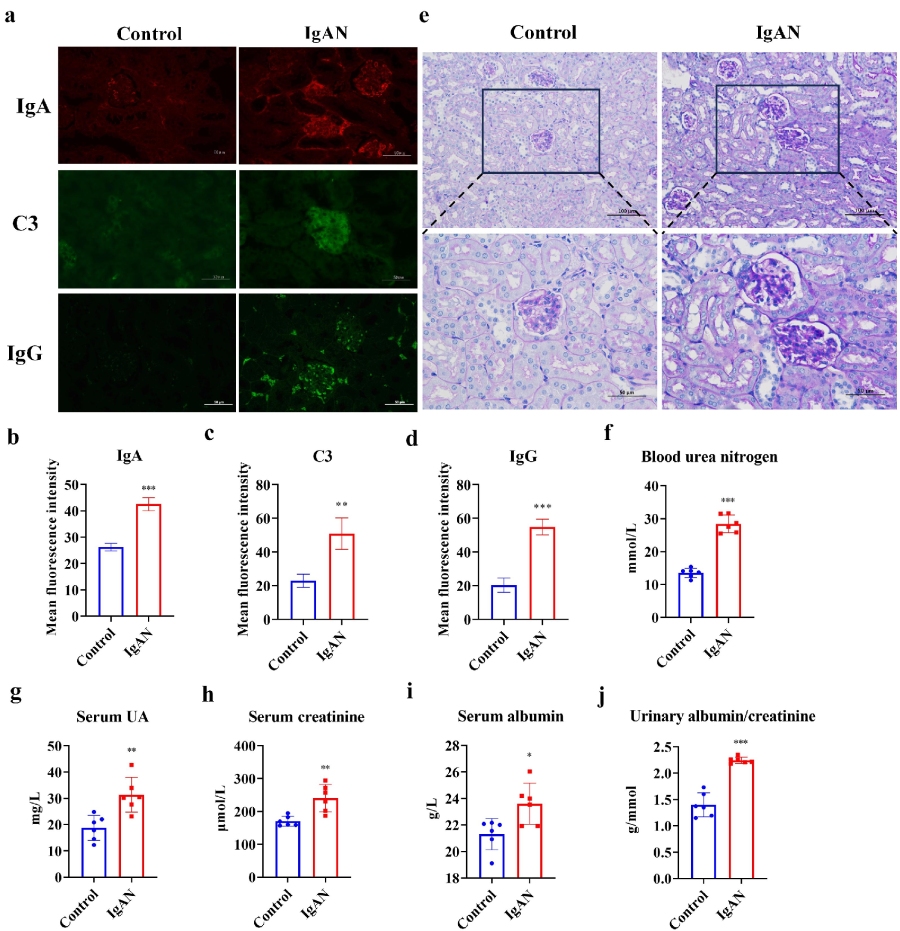
♦ IgAN引起肠道菌群结构紊乱和多样性失衡
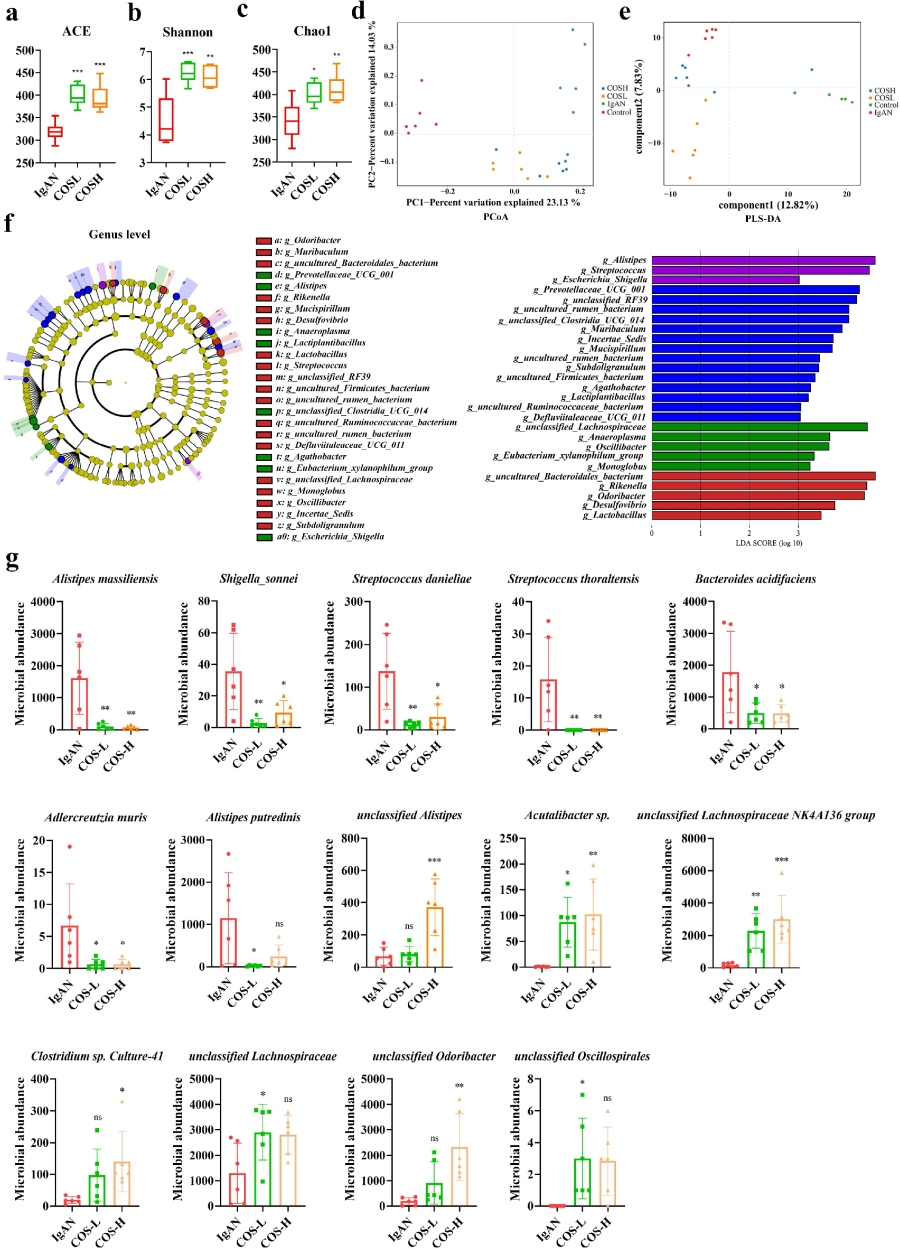
通过构建IgAN动物模型,作者发现与对照组相比,IgAN组的α多样性分析均显著降低。此外,采用非加权组平均法聚类(UPGMA树)分析、非度量多维尺度分析(NMDS)和主坐标分析(PCoA)进行相似性聚类分析。结果显示,IgAN组与对照组表现出明显的微生物聚类,两组间存在清晰的分组,表明IgAN诱导了微生物群落的转变。
为识别IgAN肠道微生物群的有效特征,作者进行了LEfSe(线性判别分析效应大小)。发现在属水平上,IgAN组中另枝菌属(Alistipes)、链球菌属(Streptococcus)、文肯菌属(Rikenella)、埃希氏菌属(Escherichia Shigella)和乳酸杆菌(Lactobacillus)的丰度显著增加。
相对应的种水平丰度也发生了显著的升高或降低,以上结果表明,IgAN诱导了肠道菌群结构紊乱和多样性失衡。
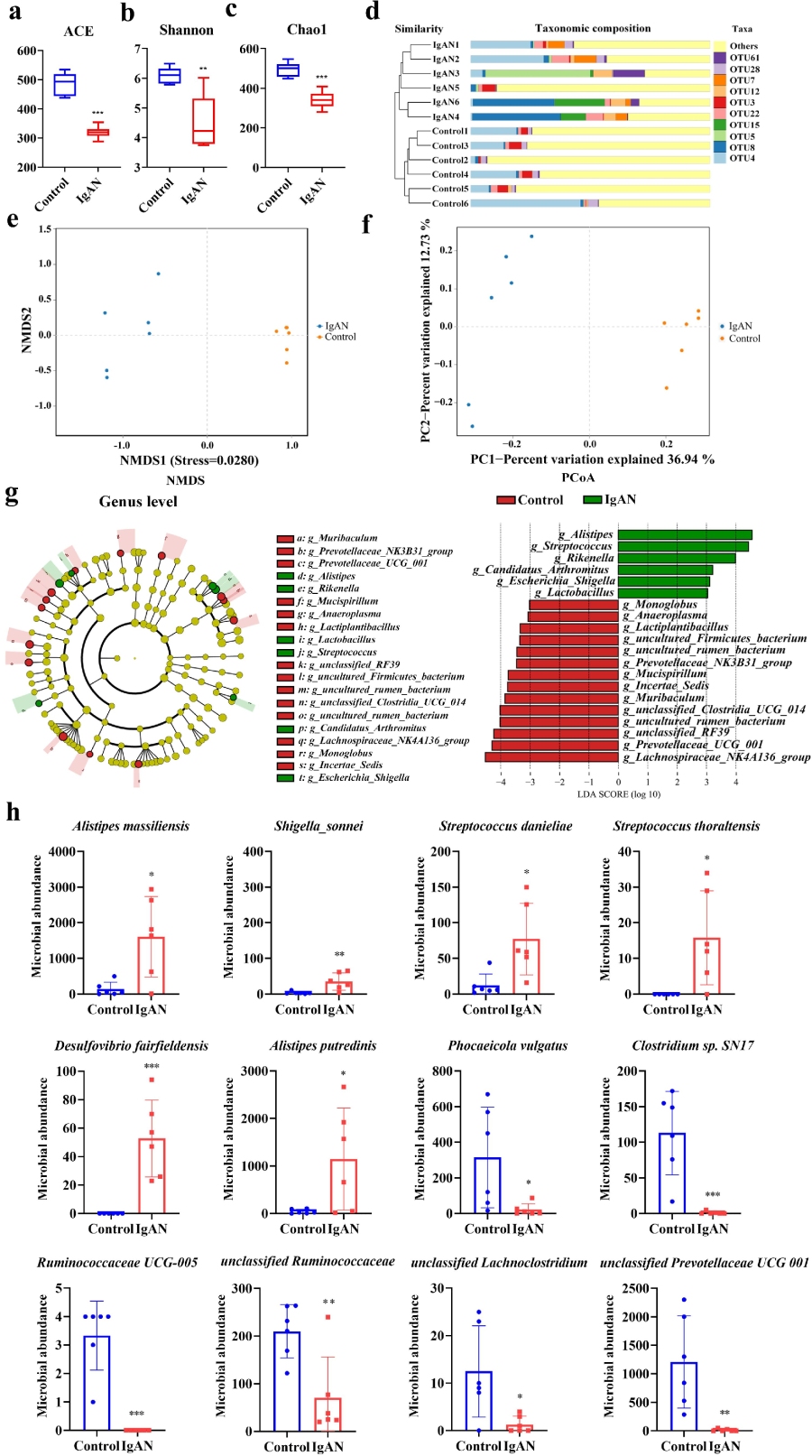
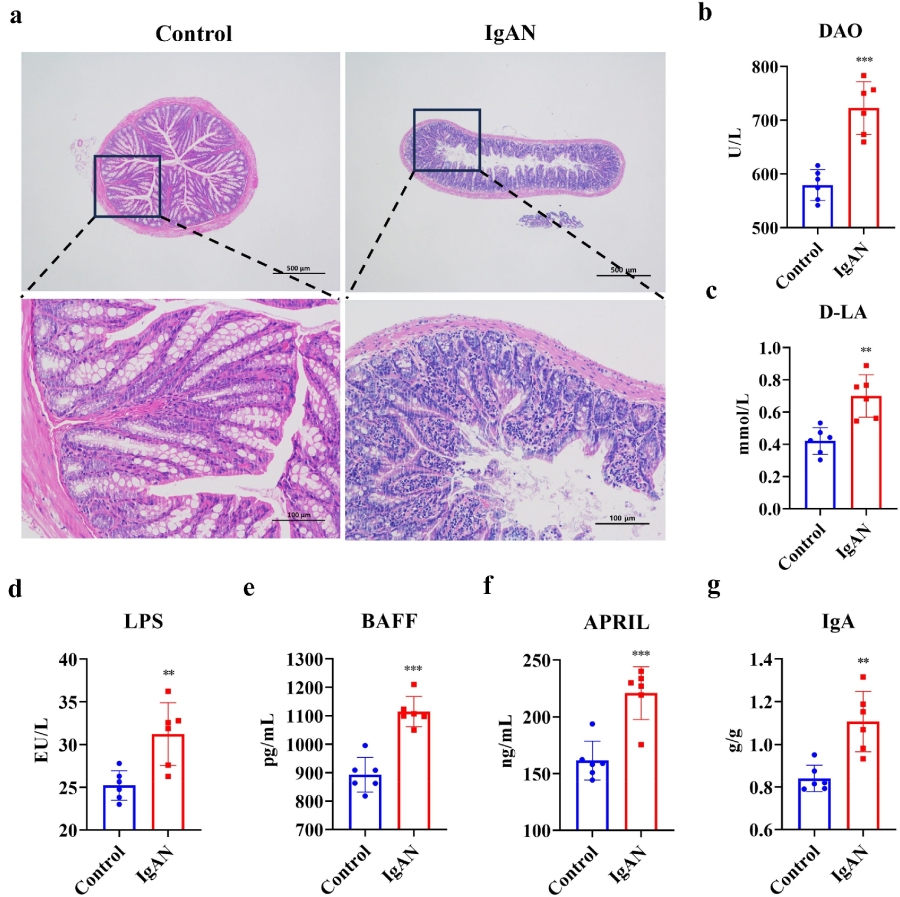
♦ IgAN引起肠道屏障损伤和肠道B细胞免疫失衡
随后作者采用苏木精-伊红(H&E)染色法评估了各组治疗小鼠的结肠完整性,以确定IgAN引起的肠道通透性变化。结果发现:对照组小鼠的黏膜上皮完整,固有层内腺体丰富且排列致密有序,肌层结构清晰。与此同时,IgAN模型小鼠的肠道腺体结构疏松,局部出现松散,肌层增厚,并伴有轻微的淋巴细胞浸润。此外,通过对肠道通透性指标的评估发现,IgAN组小鼠血清中的二胺氧化酶(DAO)(p < 0.001)、D-乳酸(D-LA)(p < 0.01)和脂多糖(LPS)(p < 0.01)水平显著升高,尤其是在DAO水平上,这表明IgAN模型小鼠的肠道通透性增加。
通过评估B细胞活化因子和IgA水平,企图阐明了IgAN的免疫失衡机制。结果显示,与对照组相比,IgAN组小鼠的B细胞活化因子(BAFF)(p < 0.001)和增殖诱导配体(APRIL)(p < 0.001)水平显著升高。IgA水平也异常升高(p < 0.01),这表明B细胞过度活化导致IgA稳态失衡。
总结来说,IgAN模型小鼠的肠道菌群失调导致其肠道屏障完整性降低和B细胞IgA分泌失衡。
♦ COS可重塑IgAN小鼠模型的菌群失调
随后,作者为探索调节IgAN的特定微生物群是否能改善疾病进展,应用了COS对IgAN中失调的微生物群进行靶向调节。α多样性比较结果显示,经不同剂量COS干预后,IgAN小鼠模型的肠道微生物群整体得到恢复。β多样性分析(PCoA和PLS-DA)表明,与对照组相比,COS干预后的肠道微生物群表现出显著改变,其结构向对照组方向转变。
肠道微生物群组成分析显示,不同剂量COS干预后富集的微生物群存在差异:COS-L组主要富集未分类的毛螺菌科(unclassified Lachnospiraceae)、支原体属(Anaeroplasma)、振荡杆菌属(Oscillibacter)、嗜木糖真杆菌群(Eubacterium xylanophilum group)和单球属(Monoglobus);而COS-H组主要富集未培养的拟杆菌目细菌(uncultured Bacteroidales bacterium)、理研菌属(Rikenella)、臭味杆菌属(Odoribacter)和乳酸杆菌属(Lactobacillus)。
与此同时发现:COS-L(低剂量壳寡糖)和COS-H(高剂量壳寡糖)均有效抑制了IgAN模型中显著增加的微生物丰度,由此,实现了对IgAN模型肠道微生物群的反向平衡调节。
♦ 靶向微生物调控减轻肠道屏障损伤,并且对IgA发挥免疫调节作用
此外,作者进一步探讨了调节特定微生物群落对肠道屏障和黏膜免疫的影响。结果显示,COS干预组显著改善了肠道通透性指标。对D-LA和LPS的改善效果呈剂量依赖性,其中COS-H组的改善效果最佳。阳性对照组也显示出对IgAN模型引起的肠道损伤的改善。H&E染色还显示,COS干预导致结肠结构清晰完整,肠腺排列规则,趋于正常化。
同时,COS干预缓解了IgAN模型中B细胞过度活化引起的IgA失衡。显著降低了小鼠血清中BAFF(COS-L组,p < 0.001;COS-H组,p < 0.001)和APRIL(COS-L组,p < 0.001;COS-H组,p < 0.001)的水平。COS-H组的IgA水平显著降低(p < 0.05)。总结来说,针对IgAN中特定微生物群落的靶向调节可抑制APRIL和BAFF的过表达,从而对IgA发挥免疫调节作用。
♦ IgAN患者粪菌移植会引起模型小鼠产生肾损伤
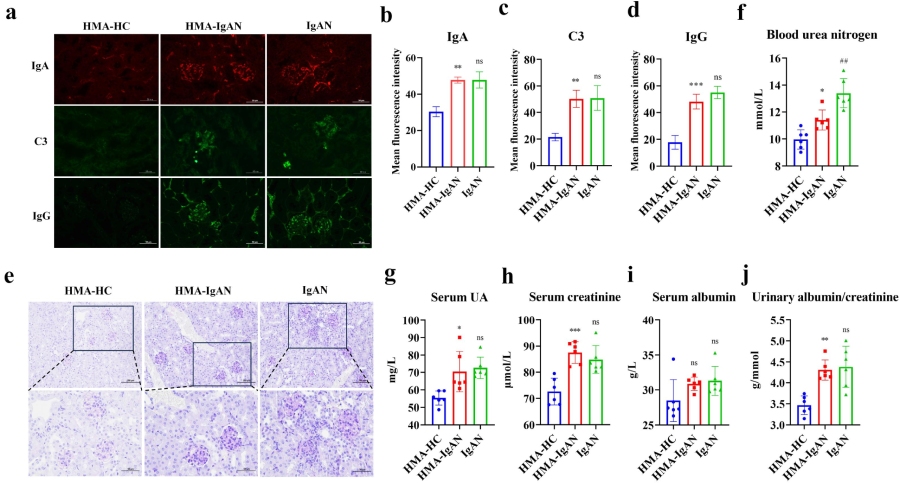
采用人类微生物群相关HMA-IgAN小鼠模型探讨小鼠模型与人类微生物群的差异,并计划验证IgAN诱导的人体肠道微生物群演变对小鼠肾功能的影响。肾免疫荧光显示,HMA-IgAN小鼠肾小球IgA(p < 0.01)、C3(p < 0.01)和IgG(p < 0.001)沉积与IgAN模型小鼠观察到的结果相似。PAS染色显示,HMA-IgAN小鼠肾小球系膜细胞显著增生伴炎性浸润,与IgAN模型组相似。与HMA-HC组相比,HMA-IgAN小鼠表现出与IgAN模型相似的肾损伤,血尿素氮(BUN,p < 0.05)、尿酸(UA,p < 0.05)、血肌酐(Scr,p < 0.001)和尿白蛋白/肌酐比(ACR,p < 0.01)显著升高。
这些结果表明,IgAN状态下的肠道微生物群可诱导成功构建IgAN小鼠模型,并导致宿主肾损伤,其损伤程度与IgAN小鼠模型观察到的损伤相当。
♦ HMA-IgAN小鼠模型重现了肠道菌群失调
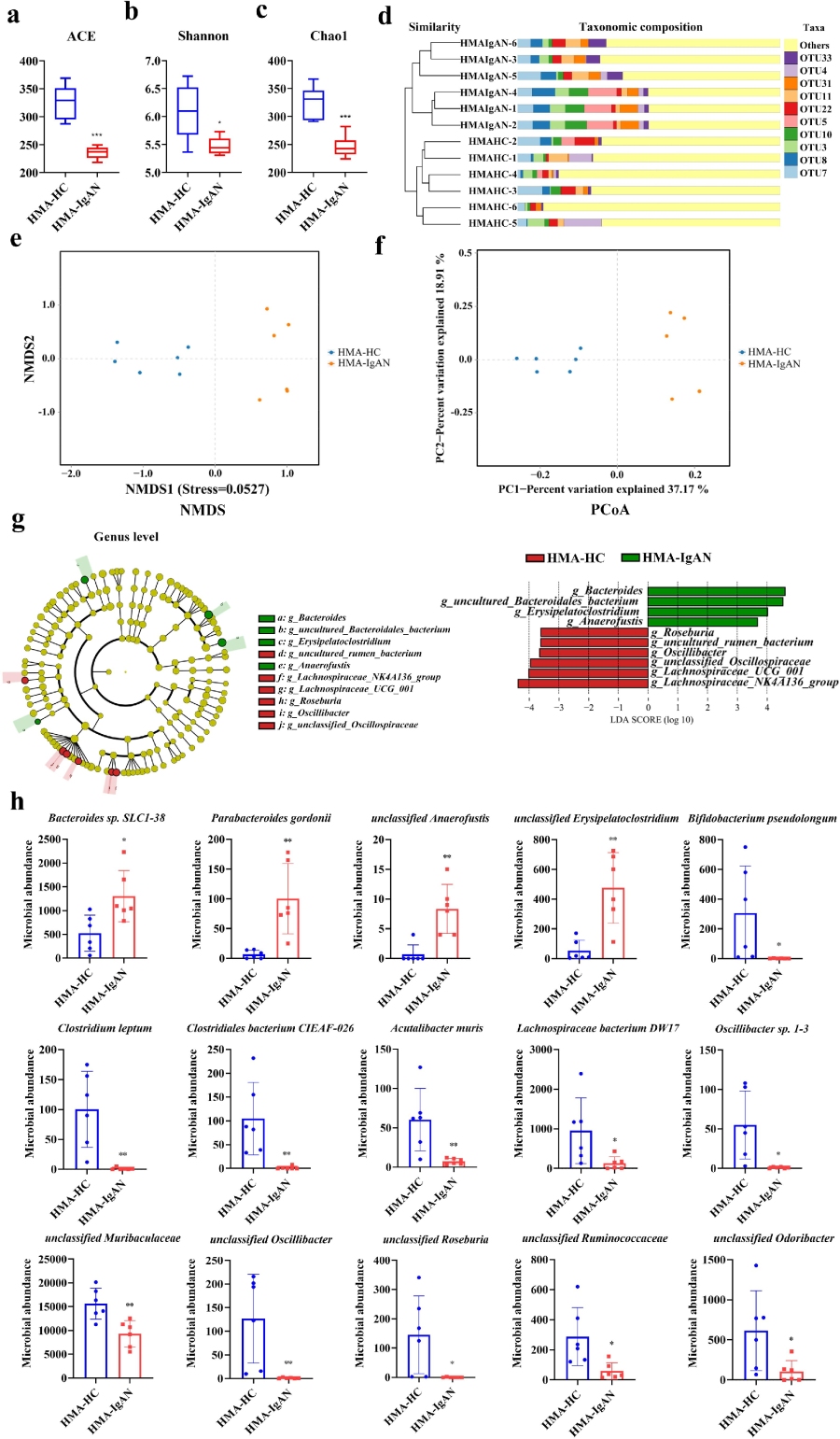
进一步分析发现:与HMA-HC组相比,HMA-IgAN组小鼠肠道微生物群的α多样性显著降低。β多样性分析显示,两组的聚类之间存在明显的分化。两组的微生物群特征也存在显著差异。在属水平上,HMA-IgAN小鼠表现出拟杆菌属(Bacteroides)、未培养的拟杆菌目细菌(uncultured Bacteroidales bacterium)、丹毒丝菌属(Erysipelatoclostridium)和厌氧梭菌属(Anaerofustis)的增加。相对应的种水平丰度也发生了显著的升高或降低,以上结果表明,HMA-IgAN小鼠模型可以诱导肠道微生物群多样性(ACE、Shannon和Chao1指数)的紊乱以及微生物群落结构的改变。
♦ COSF增加了HMA-IgAN小鼠模型肠道菌群多样性,并且维持了肠道稳态
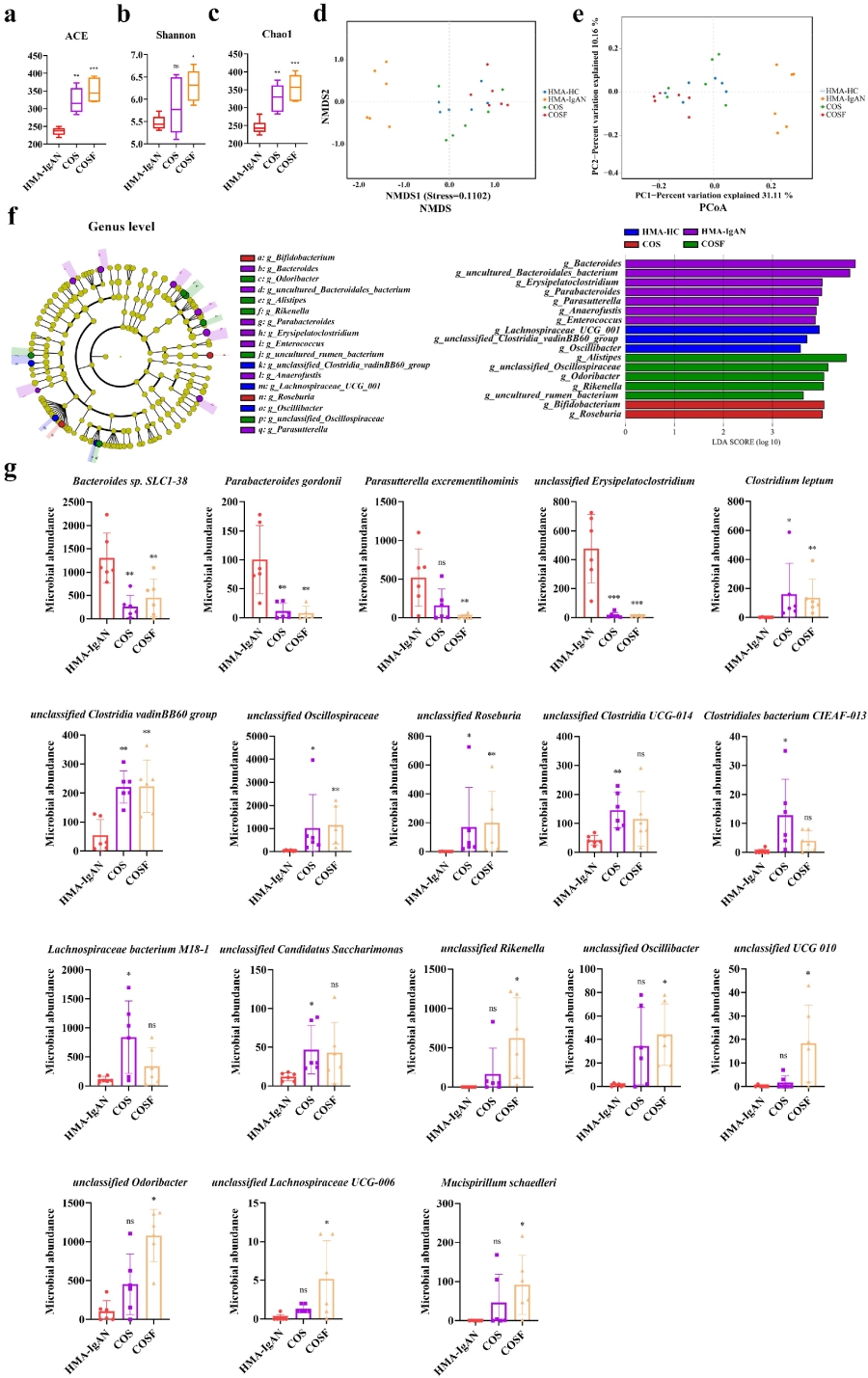
最后,作者在IgA肾病(IgAN)小鼠模型中,进一步给予COS和COSF(壳寡糖制剂)进行干预。结果显示,COS和COSF干预皆显著增加了HMA-IgAN小鼠肠道微生物群的α多样性指数,从而增加了肠道微生物群的丰富度。聚类结果显示,HMA-IgAN组的样本与对照组和干预组的样本明显分离,干预组样本倾向于与对照组相似。采用LEfSe分析比较了HMA-HC组、HMA-IgAN组、COS干预组和COSF干预组之间的差异微生物群,并鉴定了各组的差异微生物群。在属水平,COS可富集双歧杆菌(Bifidobacterium)和罗斯氏菌(Roseburia)。COSF组富集的微生物群包括普氏菌(Alistipes)、未分类的振荡螺菌科(Oscillospiraceae)、臭味杆菌(Odoribacter)、里肯氏菌(Rikenella)和未培养的瘤胃菌。
相对应的种水平丰度也发生了显著的升高或降低,结合前期介绍的IgAN模型组COS干预后的微生物变化,可得出结论:COS和COSF能够平衡两个模型中特定微生物群的失调。
♦ COSF可改善HMA-IgAN小鼠模型的肾功能修复
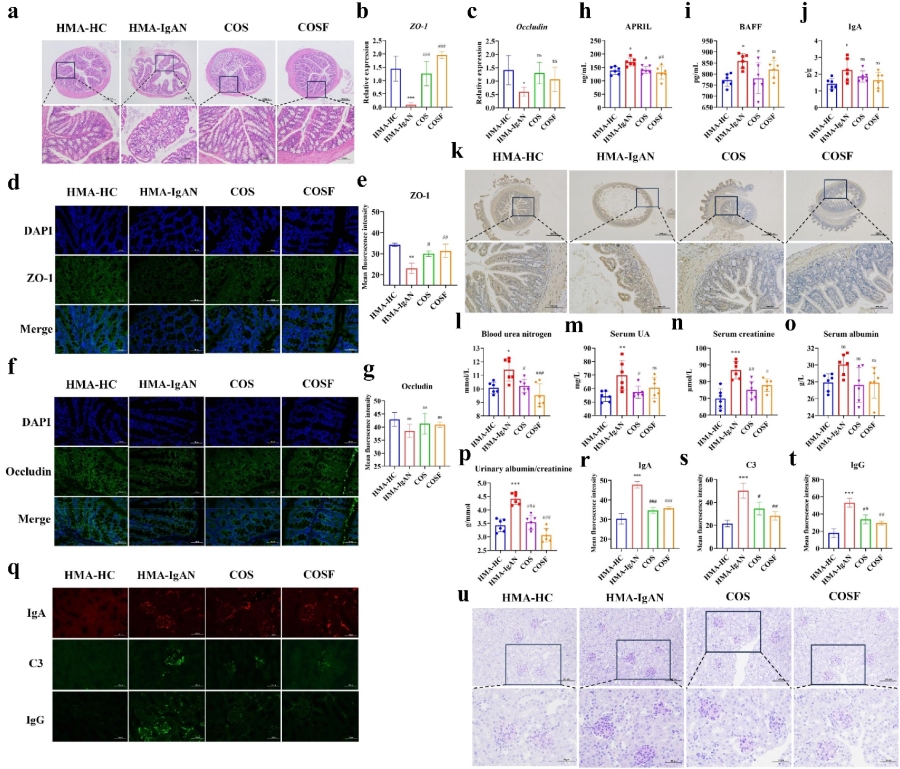
最后作者发现COS与COSF(壳寡糖制剂)皆显著改善了HMA-IgAN小鼠模型的各项肾功能指标,显著降低了UA(p < 0.05)、Scr(p < 0.01)、BUN(p < 0.05)和ACR(p < 0.001)水平。
肾小球PAS染色结果显示,COS和COSF干预显著降低了IgA(COS, p < 0.001; COSF, p < 0.001)、C3(COS, p < 0.05; COSF, p < 0.01)和IgG(COS, p < 0.01; COSF, p < 0.01)的沉积,并对系膜细胞增殖和基质扩张具有明显的抑制作用,其中COSF组在肾小球系膜区增殖方面显示出更显著的改善。
总结来说,COSF干预可通过靶向调节HMA-IgAN小鼠模型内的特定微生物群落来增强肾功能。
研究总结
该研究采用IgAN和人类微生物群相关模型来研究IgAN对肠道微生物群改变的影响以及肠道微生物群的可能会触发 IgAN的机制。此外,本研究还发现了壳聚糖 (COS)和COS制剂(COSF)具有微生物群靶向功能,可增强肠道屏障和肾功能的作用。这些结果表明,IgAN可导致α多样性降低和肠道微生物群的结构改变。同时,肠道也出现了B细胞免疫失衡和紧密连接蛋白水平降低(ZO-1和Occludin)。而COS/COSF可通过靶向调节富集肠道屏障和粘膜免疫相关微生物群来增强肠道ZO-1表达,减少B细胞活化因子(BAFF)和增殖诱导配体(APRIL)过表达,从而减少IgAN中的肾损伤。
总之,该研究证明了部分肠道菌群与IgAN的之间的机制关系,为开发针对微生物群的食物干预措施改善IgAN提供科学依据。
以上内容来源于网络,侵删





 京公网安备 11011302003368号
京公网安备 11011302003368号