2026年1月12日,西班牙马德里营养高级研究所Javier Moral-Sanz和Maria P. Ikonomopoulou在Nature Aging(IF=19.4)发表题为“Senotoxins target senescence via lipid binding specificity, ion imbalance and lipidome remodeling”的研究文章。

该文研究了SntI对基本细胞过程的影响,阐明了其与脂质的分子相互作用,评估了其对衰老癌细胞的选择性,并评估了增强生成的变异体在对抗癌症和化疗诱导的衰老方面的体内疗效。此外,该研究为一类天然衍生化合物能够靶向衰老细胞这一概念提供了理论依据,这有可能开创一种全新的衰老细胞清除剂的类别。百迈客生物为该研究提供了转录组测序服务。
研究背景
细胞衰老是衰老的驱动因素,也是肿瘤进展的屏障,但衰老细胞的持续积累会引发炎症和肿瘤复发。化疗虽能抑制肿瘤,却会诱导肿瘤微环境中出现衰老细胞,进而导致治疗相关不良反应并可能支持肿瘤复发。现有衰老溶解药物(senolytics)存在治疗窗口窄、脱靶毒性、效价低或生物利用度有限等问题,亟需开发更有效的衰老治疗方法和化合物。
毒液和毒素是新型治疗剂的宝贵来源,其具有极高的特异性和效价,部分毒液中的肽已被证实可抑制肿瘤细胞生长和扩散。
研究结果
- 探究来自加勒比海海葵毒液的成孔毒素Sticholysin I(StnI)的衰老溶解特性。
- 阐明StnI与脂质的分子相互作用及其对衰老癌细胞的选择性机制。
- 评估StnI优化变体(StnIG)在体内针对癌症和化疗诱导衰老的疗效。
- 提出 “senotoxins”(衰老毒素)这一新型天然来源化合物类别,为衰老相关疾病治疗提供新思路。
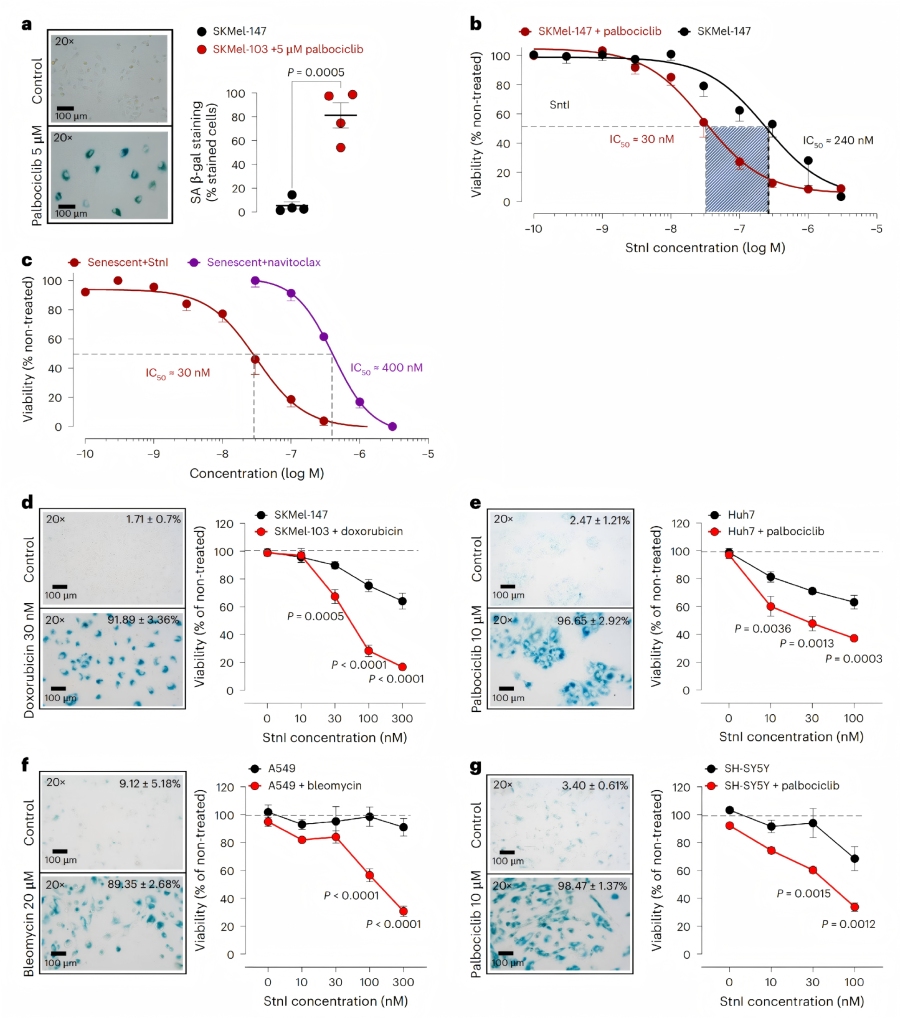
♦ StnI的体外衰老溶解特性细胞衰老诱导与表型验证
通过palbociclib抑制CDK4/6,或使用多柔比星、博来霉素处理,成功诱导人黑色素瘤SKMel-147细胞、肝癌Huh7细胞、肺腺癌A549细胞、神经母细胞瘤SH-SY5Y细胞进入衰老状态。衰老细胞表现为p53磷酸化水平降低、p21ⁿᵏ⁴ᵃ表达升高、SA-β-半乳糖苷酶活性增强,且形态增大变扁平。
浓度与时间依赖性:StnI(0.1 nM-3 μM)对衰老SKMel-147细胞的viability具有浓度依赖性抑制作用,增殖细胞的IC₅₀约为240nM,而palbociclib处理的衰老细胞IC₅₀约为30 nM,衰老溶解指数为8。低浓度StnI(10-30 nM)的作用具有时间依赖性,延长暴露时间可增强衰老溶解效果。
效价优势:StnI的衰老溶解功效与navitoclax相当,但效价是其13倍,且在多种化疗诱导的衰老模型中均保持强效活性。同时,StnI处理不会改变衰老细胞的p16ⁿᵏ⁴ᵃ、p21ⁿᵏ⁴ᵃ表达及p53磷酸化水平,仅选择性杀伤衰老细胞。
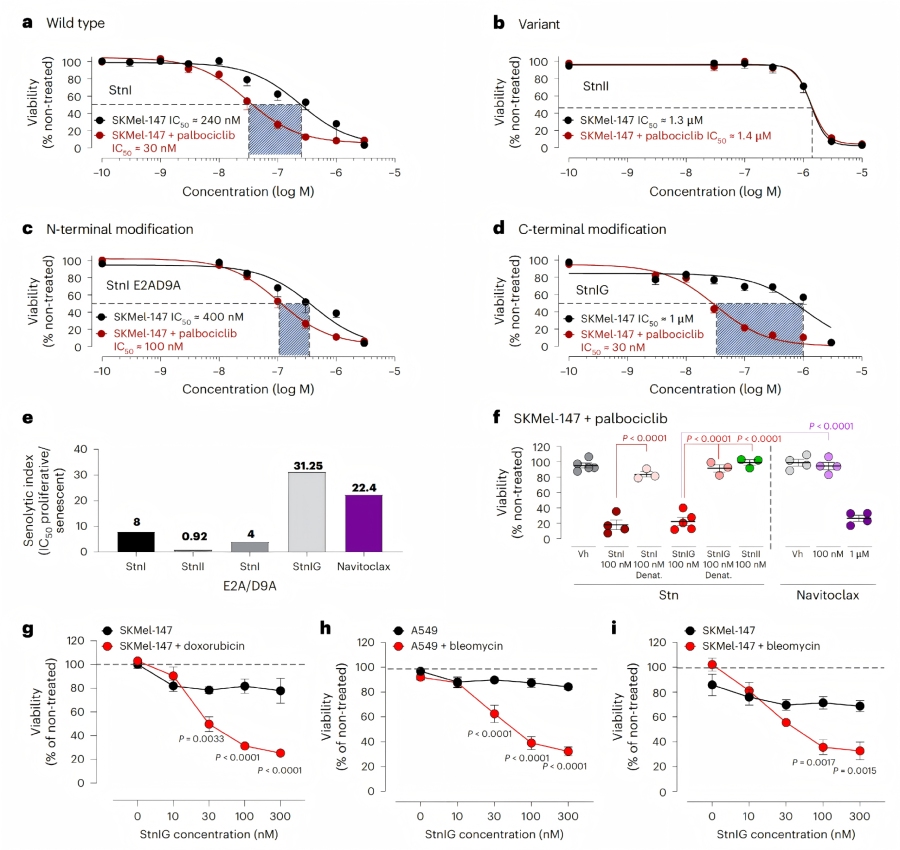
♦ StnI的结构改造与优化(StnIG的构建)
结构域功能验证:对StnI的N端两亲α-螺旋(aa1-29)、β-折叠区(aa58-101)、芳香簇(112-116)等结构域进行截短改造,所有截短体均丧失衰老溶解活性,且对增殖细胞和衰老细胞的细胞毒性极低。蛋白质变性(95℃处理45分钟)后,StnI的衰老溶解活性完全消失,表明其全长序列和构象对活性至关重要。
同源变体对比:StnI与同源变体StnII(序列同源性93%)相比,StnII对衰老细胞的细胞毒性低47倍(IC₅₀≈1.4 μM vs 30 nM),选择性指数仅为0.92,远低于 S8。差异源于N端电荷特性,StnI N端含酸性残基(E2、D9、E16)带负电,而 StnII N端为中性氨基酸。
StnIG的构建与优势:通过在N端引入甲硫氨酸(分泌时切除)、C端添加6xHis标签,构建优化变体StnIG。StnIG对增殖细胞的IC₅₀约为1 μM,对衰老细胞的IC₅₀仍为30nM,衰老溶解指数提升至31.25,高于StnI(8)和navitoclax(22.4)。StnIG处理24小时后,衰老细胞的损伤不可逆,而增殖细胞可逐渐恢复。
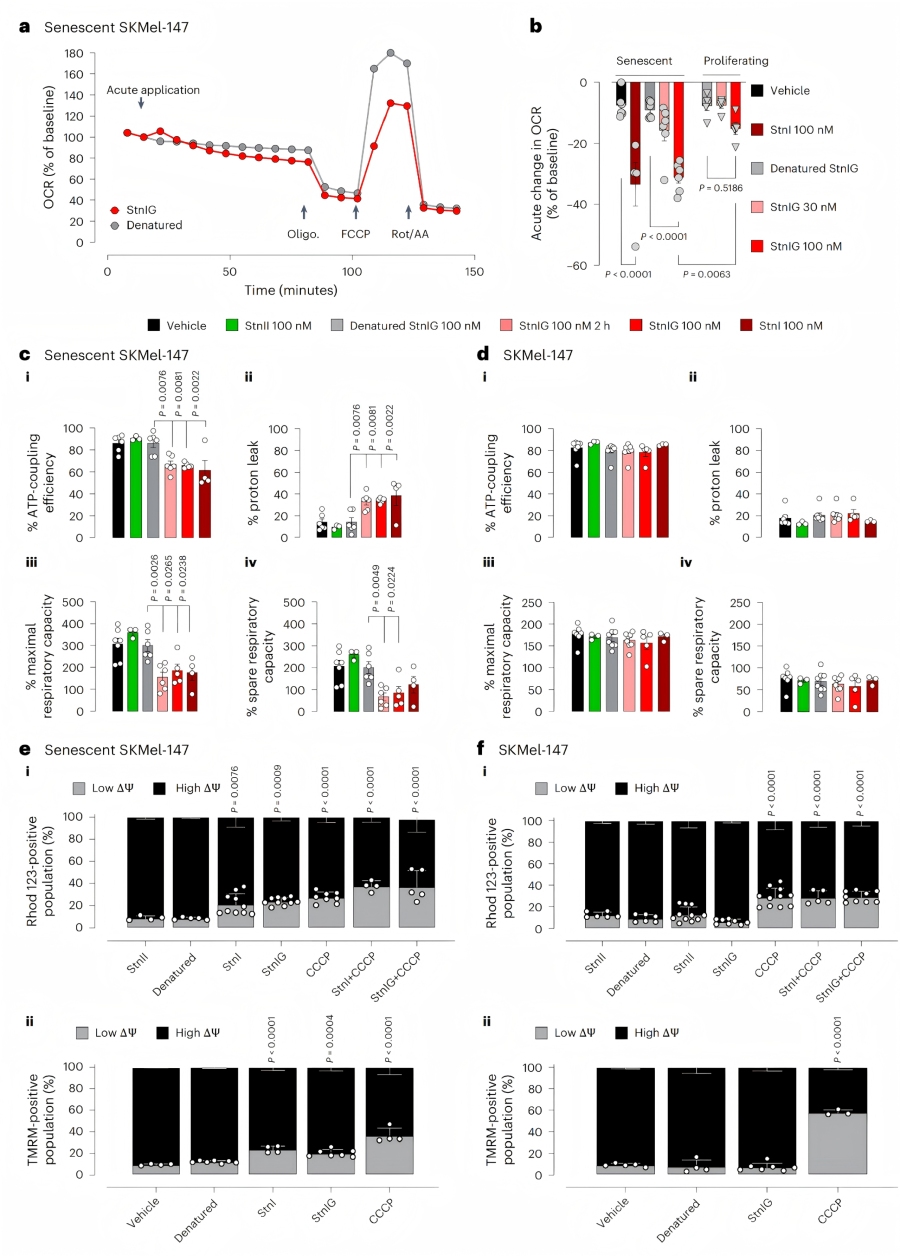
♦ StnI对细胞代谢与离子稳态的影响
转录组变化:对palbociclib诱导的衰老细胞进行StnI(100 nM)处理,RNA测序显示,6-12小时后细胞代谢通路(戊糖磷酸途径、氧化磷酸化、三羧酸循环等)显著失调,肿瘤相关信号通路(TGF-β、JAK-STAT、MAPK等)下调。同时,鞘脂生物合成通路及离子转运、钙稳态相关基因(41个膜电位相关基因、40 个钙信号相关基因)早期即出现表达异常。
线粒体功能损伤:StnI和StnIG处理后,衰老细胞的线粒体呼吸在15分钟内短暂升高,随后持续下降(StnI组降低33.5%±7%,StnIG组降低31.1%±2%),而变性StnIG无此效果。增殖细胞经StnIG处理后,基础呼吸仅降低15.1%±2%,远低于衰老细胞。衰老细胞的线粒体膜电位去极化,ATP偶联效率、最大呼吸能力和备用呼吸容量均显著降低,且持续24小时以上,伴随凋亡增加(Annexin V阳性细胞比例升高)。
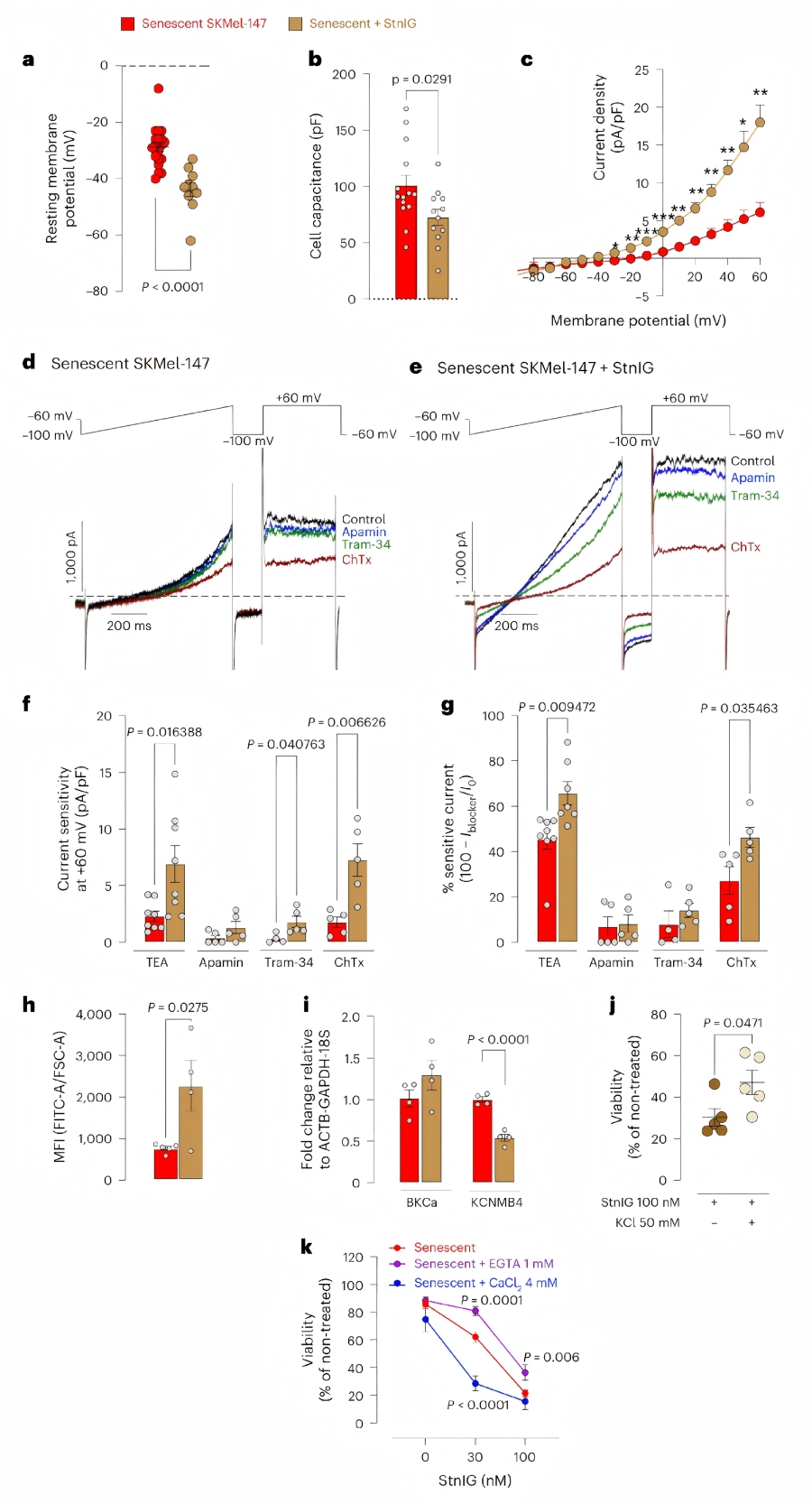
离子平衡紊乱:膜片钳分析显示,衰老细胞的细胞膜去极化,钾通道(主要为钙激活钾通道KCa)密度降低。StnIG处理后,衰老细胞出现持续的钾外流、钠内流和钙内流,细胞膜超极化。其中,钙内流主要来自细胞外,且可激活KCa通道(尤其是BKCa和IKCa亚型),进一步促进钾外流,导致细胞体积减小。
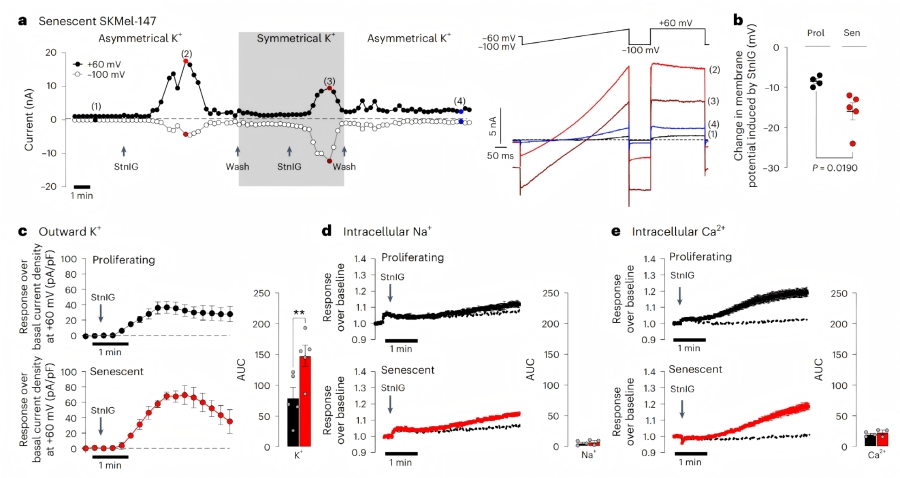
♦ StnIG诱导衰老细胞死亡的机制
钙依赖性细胞死亡:StnIG处理后,衰老细胞内钙水平持续升高,下调BKCa通道调节亚基KCNMB4,增强BKCa通道活性。使用钙螯合剂(EGTA、BAPTA)或 BKCa通道阻滞剂(charybdotoxin)可显著削弱StnIG的衰老溶解效果,表明钙内流和BKCa激活是细胞死亡的关键环节。
凋亡与焦亡的协同作用:StnIG诱导的衰老细胞死亡不依赖坏死性凋亡,但对caspase-1/4抑制剂(VX-765)和泛caspase抑制剂(z-VAD FMK)敏感。流式细胞术证实,StnIG可诱导衰老细胞发生早期凋亡(不依赖BKCa激活),而持续的钙内流和BKCa激活促进细胞体积减小和晚期凋亡,同时伴随焦亡发生。BKCa激活剂BMS-191011可增强StnIG的细胞毒性。
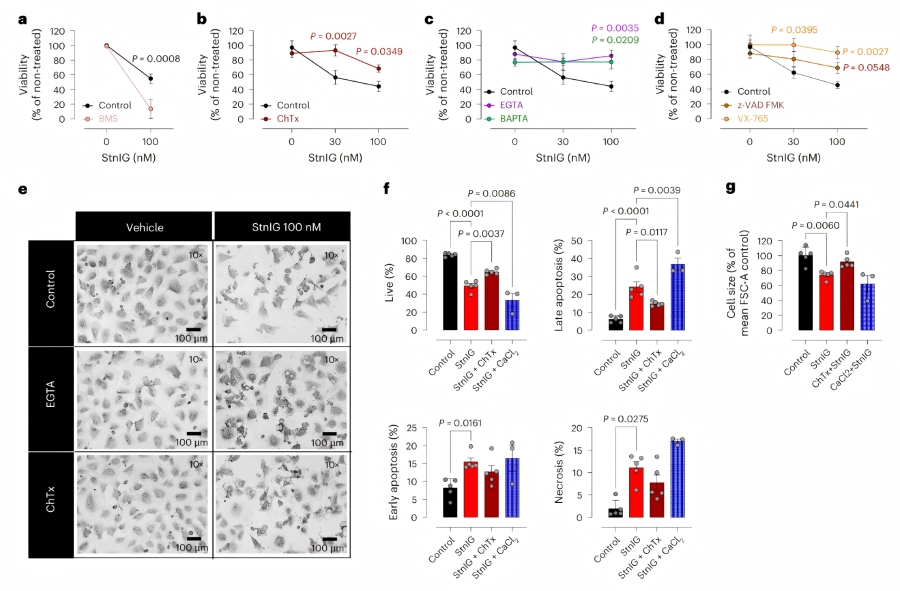
♦ StnIG对衰老细胞的选择性机制(脂质结合特异性)
衰老细胞的脂质组重塑:与增殖细胞相比,衰老SKMel-147细胞的脂质谱发生显著变化,磷脂酰丝氨酸(PS)、鞘磷脂(SM)和线粒体心磷脂(CL)含量降低,磷脂酰胆碱(PC)、醚键磷脂酰乙醇胺(PE O-)、胆固醇酯(CE)和甘油三酯(TAG)含量升高。同时,溶血磷脂(LPC、LPE-O、LPI、LPS)含量增加。
脂质对StnIG毒性的调控:补充PC(100 μM POPC)可增强增殖细胞对StnIG的敏感性;外源性鞘磷脂酶降解SM后,StnIG的细胞毒性增强;补充SM(100 μM)可减轻StnIG对衰老细胞的损伤,但会增加其对增殖细胞的毒性;脂蛋白耗竭血清(LPDS)处理后,StnIG对增殖细胞的毒性增强,对衰老细胞的毒性减弱。
分子结合机制:基于同源蛋白FraC的晶体结构建模显示,StnIG的α2螺旋(膜结合区)含关键残基Gln130、Tyr133、Glu134等,其中Glu134和Gln130可与 PE、PS脂质的头部基团形成稳定氢键(结合距离<3 Å),且结合持续时间显著长于与其他脂质的相互作用。健康细胞中PE、PS位于细胞膜内叶,而衰老细胞的膜不对称性破坏,PE、PS暴露于外叶,为StnIG提供特异性结合位点。
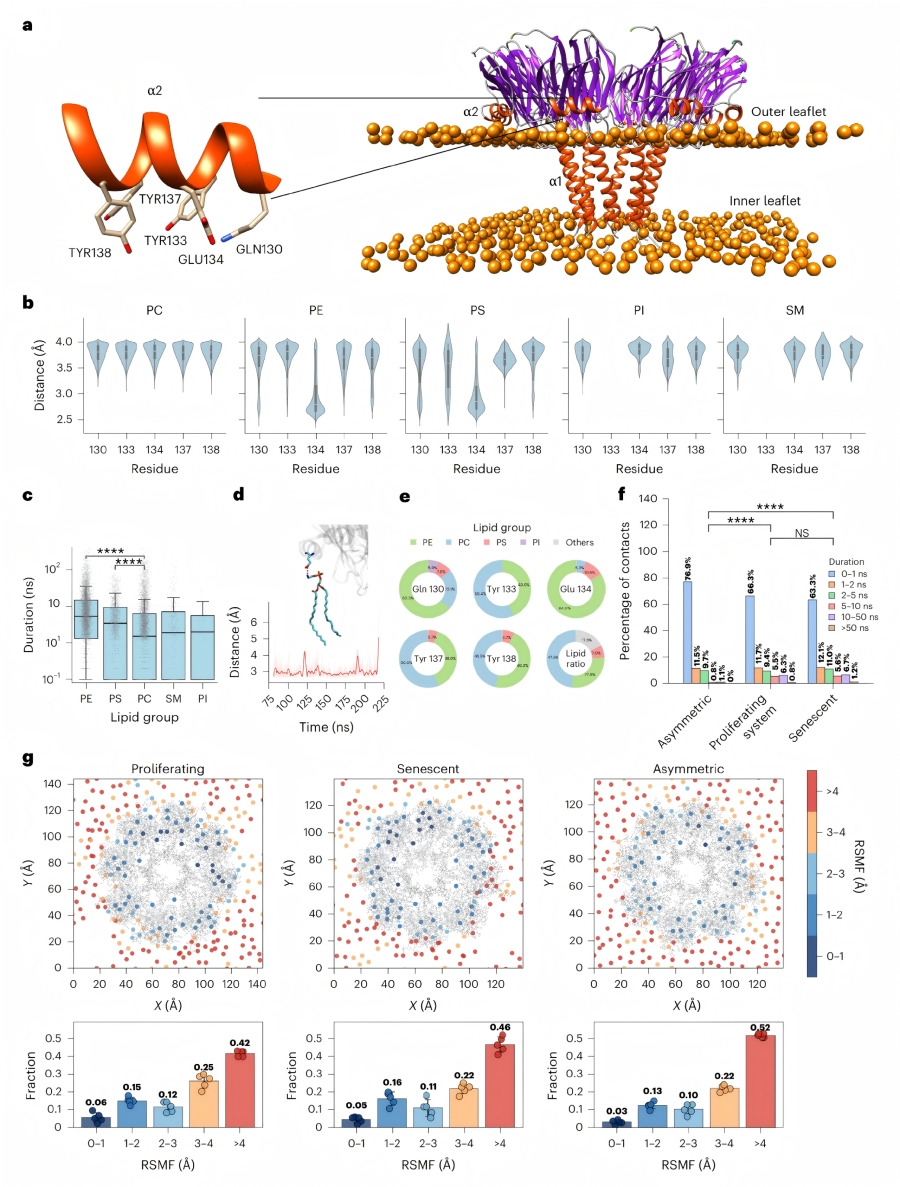
♦ StnI/StnIG的体内疗效验证
斑马鱼异种移植模型:将palbociclib诱导的衰老SKMel-147细胞注射到斑马鱼胚胎的Cuvier循环导管,10 nM StnIG处理6天后,衰老细胞积累量显著降低,效果与1μM navitoclax相当,且无明显毒性。
小鼠异种移植模型:在SKMel-147黑色素瘤和Huh7肝癌小鼠异种移植模型中,palbociclib(100 mg/kg,口服)联合StnIG(2 mg/kg,腹腔注射,每48小时一次)治疗,肿瘤体积显著缩小,疗效与palbociclib联合navitoclax(50 mg/kg,口服)相当。肿瘤组织中SA-β-半乳糖苷酶活性降低,SASP相关基因(IL-6、BCL2、CASP1)表达显著下调。
安全性评估:StnIG处理的小鼠体重仅降低5%-10%(navitoclax组为 5%),对脑、心、肺、肝、肾等器官无明显组织学损伤,肝肾功能指标正常。仅在衰老肿瘤组中观察到血钾水平升高,可能与肿瘤细胞裂解释放钾离子相关,可作为治疗效果的生物标志物。
♦ StnIG在非转化细胞中的作用
对化疗诱导的新生儿包皮成纤维细胞和真皮成纤维细胞无衰老溶解效果,但对复制性衰老成纤维细胞具有显著的衰老溶解活性。
在人肺成纤维细胞IMR90中,StnIG具有衰老形态调节作用(senomorphic effect),10.13 nM即可显著降低SA-β-半乳糖苷酶活性,且不诱导细胞死亡;134.6 nM时表现出衰老溶解活性,有效清除衰老细胞群体。
研究总结
该研究为StnIG在癌症治疗中的潜在作用提供了概念性证明,表明其与诱导肿瘤衰老的化疗药物联合使用时疗效显著提升。还证实了StnIG在人类成纤维细胞中的衰老相关潜力,这引发了关于其在衰老及与衰老相关疾病中的作用的更多疑问。然而,关于senotoxins对未转化和有复制能力的衰老细胞的衰老消除作用背后的机制仍不清楚。未来的研究还应探究StnIG在其他与衰老相关的疾病(如肺纤维化 、肾脏疾病或甚至改善早老症综合征的症状)中的疗效。
参考文献
[1] Moral-Sanz, J., Fernández-Carrasco, I., Ramponi, V., Garrido, A., Karbat, I., Cabezas-Sainz, P., Rivera-De-Torre, E., Elsallabi, O., Martín-Hernández, R., López-Aceituno, J. L., Price, N. L., Sanchez, L., Colmenarejo, G., Martínez-Del-Pozo, Á., Vetter, I., Cogolludo, A., Perez-Vizcaino, F., Del-Pozo, J., Reuveny, E., . . . Ikonomopoulou, M. P. (2026). Senotoxins target senescence via lipid binding specificity, ion imbalance and lipidome remodeling. Nature Aging.
以上内容来源于网络,侵删






 京公网安备 11011302003368号
京公网安备 11011302003368号