家畜不仅是人类重要的食物来源,更是解析复杂生物学机制的理想模型。与啮齿类相比,猪、牛、羊、骆驼等大型家畜在器官结构、生理代谢、免疫系统及发育时间轴上与人类高度相似,为神经科学、生殖发育、代谢疾病、再生医学及异种移植等领域提供了不可替代的转化研究平台。同时,家畜自身也承载着极端环境适应、驯化进化、高效生产等独特的生物特性,具有重要的农业经济价值。
空间转录组技术的出现,为家畜研究打开了“分子显微镜”下的新维度。它不再满足于“有哪些细胞、表达哪些基因”,而是将基因表达精确地定位到组织的原始空间坐标上,让我们能够原位看见细胞的分化梯度、信号通路的激活路径、免疫细胞的浸润路径以及病原与宿主的互作解析。
空间转录组在家畜领域研究的五大核心方向
方向1、神经科学与疾病模型
猪等大型家畜的大脑具有沟回结构,与人类高度相似,是研究认知功能和神经退行性疾病的理想模型。空间转录组能够精确定位疾病相关基因的皮层分层,揭示免疫细胞浸润的空间路径,为阿尔茨海默病、亨廷顿病等提供新的治疗靶点,同时推动异种移植神经并发症的防控【1-3】。
例如:利用空间转录组学和代谢组学,构建了猪前额叶皮层的高分辨率多维图谱,揭示猪前额叶皮层认知相关基因及位置【3】;通过结合单核转录组测序、空间转录组学及T细胞受体测序,提出CCL8介导的适应性免疫浸润为潜在干预靶点【1】;空间转录组成功应用于马背根神经节FFPE样本,为兽医神经病理学提供新工具【2】。

方向2、生殖发育与胎盘生物学
家畜的生殖周期长、胚胎体积大,使其成为研究生殖发育的理想模型。空间转录组技术能够原位追踪生殖细胞迁移、减数分裂启动及胎盘形成的动态过程,发现传统单细胞方法难以捕获的大细胞(如双核滋养层细胞)和稀有细胞(如具有免疫特征的滋养层细胞),为人类不孕不育与妊娠并发症提供新的认知,同时直接指导家畜繁殖效率的提升【4-12】。
例如:奶牛胎盘空间图谱成功鉴定出双核滋养层细胞【6】;以大鼠、小鼠和猪为生物医学模型,结合单细胞与空间转录组技术,发现了一类兼具免疫功能的滋养层细胞(iTrophoblast),并揭示了其在子痫前期中的异常转化【12】;空间转录组联合类器官解析了猪子宫和胎盘的新标记物,能够精确分离母胎界面的组织学结构【8】;利用单细胞转录组与空间转录组绘制了猪早期卵巢及卵子发生的时空动态图谱,揭示了颗粒细胞的“两波”模型及皮质‑髓质生殖细胞梯度【7】;同样基于上述联合策略,构建了涵盖蒙古牛下丘脑‑垂体‑卵巢轴的全面细胞图谱【11】。

方向3、皮肤与毛囊发育
猪皮肤在结构、厚度、毛囊密度和伤口愈合方式上与人类高度相似,是研究无瘢痕愈合和毛囊再生的优质模型【13-14】。
例如:研究发现哺乳动物皮肤中表皮嵴的演化涉及用一套独特的相互连接附属器网络程序,取代了形成离散微观附属器(包括毛囊和汗腺)的分子程序【13】;对四个发育时期的正常和无毛胎猪皮肤样本进行了单细胞和空间转录组分析,在无毛猪模型中定位毛囊基板祖细胞(OGN⁺/UCHL1⁺)的缺失【14】。
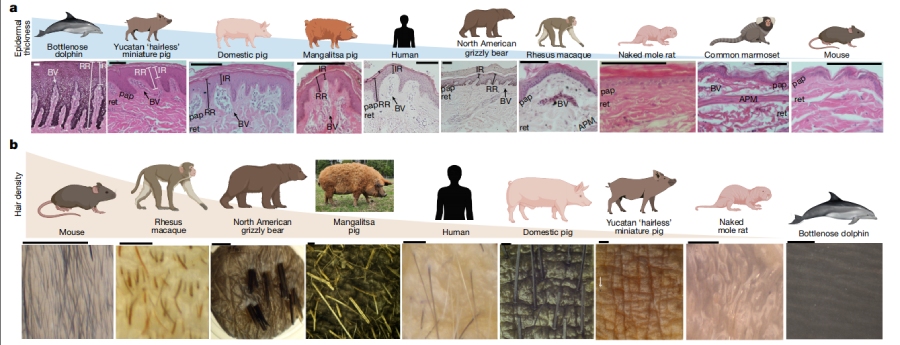
doi: 10.1038/s41586-025-10055-5.

方向4、肌肉与脂肪代谢
家畜是研究肌肉发育和脂肪沉积的重要模型,与人类代谢疾病(如肥胖、肌少症)密切相关。此前,研究者常通过微生物代谢组分析瘤胃或肠道菌群代谢产物,推测其对宿主营养吸收的影响,但缺乏基因表达的空间证据。空间转录组的加入,填补了这一空白:它能够原位定位营养物质转运蛋白、代谢酶及信号分子的表达区域,将微生物代谢物变化与特定上皮层次(如瘤胃基底层、棘层、颗粒层)的宿主响应直接关联,从而真正实现“菌群代谢物—宿主空间响应”的机制解析,为家畜营养吸收研究提供了前所未有的空间分辨率【15-17】。
例如:在奶牛瘤胃上皮中,单细胞转录组结合空间转录组结合解析随着前胃上皮细胞从基底层向角质层分化,线粒体呼吸和抗氯化能力同步增强,形成代谢—氧化还原协同上升的趋势,功能实验证实GPX1是介导氧化磷酸化(OXPHOS)和瘤胃上皮细胞分化的关键抗氧化靶点【15】;单细胞转录组+空间转录组解析猪背最长肌中肌内脂肪的空间异质性,揭示TGF‑β信号通路在IMF中的特异性富集——瘦型猪中IMF通过自分泌产生更多TGF‑β2,而肥胖猪中IMF接收更多内皮来源的TGF‑β1,为肥胖相关肌肉萎缩提供潜在治疗靶点【17】。

方向5、比较与进化生物学
家畜在驯化和适应极端环境过程中形成了独特的生理特征。空间转录组通过跨物种比较,能够发现物种特异性细胞类型和适应性基因表达模式,揭示驯化对免疫系统的影响,为理解进化适应机制、保护濒危家畜品种以及培育抗逆新品种提供理论基础【18-19】。
例如:单细胞转录组+国产平台BMKMANU S1000构建骆驼与牛54个组织单细胞图谱,发现骆驼特有的胃上皮高增殖细胞群及肾脏S100A4⁺血管平滑肌细胞【18】;家猪与野猪肺发育比较揭示驯化对免疫细胞比例的影响【19】。

空间转录组区别于传统组学的七大核心优势
优势1、保留空间结构,看见真正的“组织地图”
传统单细胞测序将组织解离成悬液,细胞的空间位置信息完全丢失,而空间转录组直接在组织切片上捕获RNA,原位保留细胞在组织中的真实分布。
案例:在猪早期卵巢发育研究中,空间转录组清晰展示了生殖细胞从“随机分布”到“皮质→髓质梯度”的动态迁移轨迹,这是单细胞测序完全无法实现的【10】。
案例:在鹿角快速再生研究中,空间转录组将细胞类型精确映射到从远端干细胞到近端软骨的连续分层,揭示了每日厘米级伸长的“连续流”生长模型【20】。

优势2、解析组织异质性,发现“隐藏的”细胞亚型
同一组织内不同区域的细胞可能具有完全不同的转录组特征。空间转录组能够区分层特异性、区域特异性的分子差异。
案例:在猪前额叶皮层研究中,认知差异相关的分子变化主要发生在皮层III层——如果使用bulk转录组,这种层特异性的差异可能被完全掩盖【3】。
案例:在奶牛胎盘研究中,空间转录组以Bin 100分辨率区分了单核滋养层细胞的7个亚群,并成功定位了双核滋养层细胞(常规单细胞可能难以捕获)的空间分布【5】。

优势3、验证单细胞发现,给细胞类型身份双重肯定
单细胞RNA测序可以发现新的细胞亚群,但无法确认这些细胞在组织中的真实存在和位置。空间转录组是原位验证的“金标准”。
案例:在骆驼肾脏中,单细胞测序发现了一个独特的S100A4+血管平滑肌细胞亚型。空间转录组将其精确定位到肾小球入球/出球小动脉区域,证实了该细胞群的真实性,并提示其可能参与血压调节【18】。
案例:在猪皮肤毛囊基板研究中,单细胞数据提示OGN⁺/UCHL1⁺细胞是毛囊基板的祖细胞。空间转录组在原位证实了这些细胞位于表皮基底层,并揭示了BMP/TGFβ信号为关键的信号通路【14】。

优势4、推断细胞间通讯,提供“面对面”互作证据
细胞通过配体-受体相互作用沟通,但这种互作需要空间邻近性。空间转录组可以直接展示配体和受体在组织切片上的共定位,为细胞通讯提供比表达相关性更强的证据。
案例:在亨廷顿病猪模型研究中,空间转录组展示了IFN相关小胶质细胞与CCR5⁺ CD8⁺ T细胞在HD-KI猪纹状体中呈现明显空间共定位【1】。
案例:在猪母胎界面研究中,研究者利用空间转录组的spot间距离信息过滤了空间上不可能发生的配体-受体互作,使细胞通讯推断更符合生理实际【8】。

优势5、区分来源细胞,解决“谁是谁”难题
在异种移植、母胎界面等混合细胞来源的场景中,空间转录组结合种间序列差异,可以精准区分供体vs受体或胎儿vs母体来源的细胞。
案例:在猪-非人灵长类肾异种移植研究中,空间转录组利用种间特异性探针,发现移植物内皮逐渐表达受体来源的PECAM1、VWF、MHC分子和血型抗原,揭示了此前未被认识的“系统性转移”现象【12】。
案例:在奶牛胎盘研究中,空间转录组结合SNP分型,成功区分了胎儿来源和母体来源的spots,这是空间转录组分析中少有的亮点【6】。
优势6、兼容FFPE样本,解锁珍贵临床资源
许多珍贵的人或动物样本是以福尔马林固定石蜡包埋(FFPE)形式存档的。新一代空间转录组技术(如百创FFPE空间转录组)可以直接对这些样本进行分析,极大拓展了回顾性研究的可能性。
案例:在马背根神经节研究中,研究者使用空间转录组对FFPE存档的马神经组织进行区域选择性空间转录组分析,用人源探针成功获得了可分析的转录组数据,为兽医神经病理学开辟了新途径【2】。

案例:在异种移植肾研究中,空间转录组成功从中提取了高质量的空间转录组数据,精确定位了肾小球中VEGFA的丢失与血栓性微血管病的关联【12】。
优势7、作为类器官验证的“金标准”
类器官是重要的体外模型,但我们需要知道它是否真实重现了体内组织的细胞组成和空间结构。空间转录组提供了体内参考图谱,可用于验证类器官的生理相关性。
案例:在猪滋养层类器官研究中,研究者将类器官的单细胞数据与母胎界面的Visium空间数据整合,通过概率映射为细胞群赋予了明确的体内身份,验证了类器官对体内细胞异质性的重现能力【8】。

空间转录组研究方案设计推荐
方案一:单纯空间转录组
优势:单组学入门门槛低,成本可控,分析流程标准化。
解决的问题:回答“哪些基因在组织的哪个区域/层次表达?”无需多组学复杂整合,即可快速获得组织空间图谱,为后续机制研究提供精准的“导航图”。
方案二:单细胞+空间转录组
优势:经典“发现+验证”组合,兼顾单细胞分辨率与空间原位信息,能够识别稀有/新型细胞亚群并直接验证其在组织中的真实位置和微环境。
解决的问题:回答“新发现的细胞类型真的存在于组织中吗?它和哪些细胞在空间上邻近、可能发生互作?”。
案例:
猪皮肤毛囊基板:scRNA-seq发现OGN⁺/UCHL1⁺祖细胞,空间转录组验证其在表皮基底层的空间定位及BMP/TGFβ信号先于WNT 激活【14】。
骆驼肾脏:scRNA-seq发现S100A4⁺VSMC亚型,BMKMANU S1000空间转录组将其定位到肾小球入球/出球小动脉,并显示DLK1-NOTCH3共定位【18】。
亨廷顿病猪模型:snRNA-seq发现CD8⁺ T细胞,空间转录组揭示CCL8与CCR5(T细胞)在纹状体病变区域的空间共定位【1】。
猪卵子发生:scRNA-seq+10x Visium+BMKMANU S1000绘制时空图谱,确定了猪卵巢皮质和髓质区颗粒细胞系的分子特征和空间动力学。通过空间共定位分析和细胞间通讯分析,揭示了皮质和髓质区域生殖细胞和体细胞之间独特的细胞-细胞通讯模式【10】。
方案三:单细胞+空间+多组学(代谢/表观/功能验证)
优势:多维度机制解析,形成“发现→验证→功能”闭环。可联合空间代谢组构建基因-代谢物调控网络,或联合snATAC-seq解析表观调控与空间位置的关系,并通过体外/体内功能实验直接验证关键信号通路。
解决的问题:回答“基因表达变化导致哪些代谢物改变?表观调控如何影响空间分布?预测的信号通路是否具有功能必要性?”
案例:
猪前额叶皮层:空间转录组联合空间代谢组,通过WGCNA发现turquoise基因模块与氨基酸/脂质代谢模块高度相关【3】。
鹿角再生:snRNA-seq+snATAC-seq+空间转录组三组学联合,解析从远端干细胞到近端骨组织的连续分化梯度,发现转分化中间态细胞【20】。
奶牛瘤胃上皮:scRNA-seq+空间转录组+LiP-MS揭示氧化还原调控前胃上皮代谢重塑与分化的全新机制【15】。
从基础生命机制解析到人类疾病模型构建,从家畜育种改良到异种移植转化应用,空间转录组早已不只是生成精美图谱的技术工具,更是驱动大动物生物医学与农业育种研究的核心引擎,为生命科学探索与产业应用升级打开了全新视野,真正让生命机制研究从 “模糊” 走向 “精准”。
参考文献:
- 【1】Li J, Lin Y, Gao J, et al. Single-nucleus transcriptomics of an engineered pig model reveals microglia–T cell interactions driving Huntington’s disease neurodegeneration. Nature Biomedical Engineering, 2026.
- 【2】Finno CJ, et al. Spatial transcriptomics defines the cell-specific RNA landscape of equine dorsal root ganglia. Veterinary Pathology, 2025.
- 【3】Cui S-D, et al. The integration of spatial transcriptomics and metabolic data from the cortical region of the brain identifies key genes associated with cognitive ability in pigs. Zoological Research, 2026.
- 【4】Su J, et al. A dynamic transcriptional cell atlas of testes development after birth in Hu sheep. BMC Biology, 2025.
- 【5】Jin H, et al. Dissecting the development of bovine testicular tissue using spatial transcriptomics. Journal of Animal Science and Biotechnology, 2026.
- 【6】Tan G-H, et al. Spatial transcriptomic analysis of the cow placenta reveals heterogeneity and differentiation of trophoblast cells. Zoological Research, 2024.
- 【7】He P, et al. A spatiotemporal transcriptomic atlas of porcine (Sus scrofa) female early gonadal development. Communications Biology, 2026.
- 【8】McCutcheon C R, et al. Defining cellular diversity at the swine maternal-fetal interface using spatial transcriptomics and organoids. PLOS Biology, 2025.
- 【9】Zang X, et al. Cross-species insights into trophoblast invasion during placentation governed by immune-featured trophoblast cells. Advanced Science, 2024.
- 【10】Ge W, et al. Spatiotemporal dynamics of early oogenesis in pigs. Genome Biology, 2025.
- 【11】Ba Y, et al. Single-nucleus and spatial transcriptomics of the hypothalamus-pituitary-ovary axis in Mongolian cattle. Animals, 2025.
- 【12】Rosales I A, et al. Mechanistic insights from transcript analysis of long-term pig to non-human primate kidney xenografts. Kidney International, 2026.
- 【13】Thompson S M, et al. Rete ridges form via evolutionarily distinct mechanisms in mammalian skin. Nature, 2026.
- 【14】Wang Y, et al. Integrating single-cell and spatial transcriptomics reveals heterogeneity of early pig skin development and a subpopulation with hair placode formation. Advanced Science, 2024, 11: 2306703.
- 【15】Zhu S-L, et al. Antioxidants promote metabolic remodeling in cattle rumen epithelium revealed by single‑cell resolution. iMeta, 2025.
- 【16】Jin L, et al. A pig BodyMap transcriptome reveals diverse tissue physiologies and evolutionary dynamics of transcription. Nature Communications, 2021.
- 【17】Wang X, et al. Integrating spatial transcriptomics and single-nucleus RNA-seq revealed the specific inhibitory effects of TGF-β on intramuscular fat deposition. Sci China Life Sci, 2025.
- 【18】Shi T, et al. Single-Cell Transcriptomic Atlases of Camels and Cattle Unravel Molecular Evolution of Digestive and Metabolic Systems. Advanced Science, 2026.
- 【19】Huang F, et al. Dynamic lung single-cell atlas of domesticated and wild pigs. Science China Life Sciences, 2026.
- 【20】Ba H, et al. A vast stem-progenitor cell pool, richly vascular system, and hybrid ossification drive the daily centimeter-scale elongation of bony antlers. iMeta, 2025.
- 【21】Tao K-S, et al. Immune cell landscape in a human decedent receiving a pig liver xenograft. Nature Medicine, 2025.
- 【22】Fan Y, et al. A cell transcriptomic profile provides insights into adipocytes of porcine mammary gland across development. Journal of Animal Science and Biotechnology, 2023.






 京公网安备 11011302003368号
京公网安备 11011302003368号