空间转录组学作为连接基因表达与空间位置信息的核心技术,打破了传统转录组研究的平均化局限,为解析植物发育机制、逆境响应、物种进化及品质改良提供了原位、高分辨率的全新视角。
当前植物空间转录组的核心瓶颈集中在植物样本特性、技术通量、分辨率平衡、数据解析、非模式植物适配,近年来,随着10× Visium、BMKMANU 、Stereo-seq等技术平台的迭代创新,植物空间组学研究呈现出多组学融合、非模式植物拓展、亚细胞分辨率突破的显著特征,相关成果持续发表于Cell、Nature、Nature Plants等国际期刊,平均影响因子持续走高。本文基于植物空间组学研究转化成果,系统梳理研究趋势、技术格局与应用方向,并深入呈现百迈客生物在该领域的技术积累与实践成果。
研究发表趋势——从高质量深耕到爆发式增长
植物空间转录组研究经历了清晰的发展阶段,呈现出“起步-深耕-爆发”的轨迹。自2017年[1]首篇论文发表后,2022年前发文量长期维持个位数,2022-2025年研究热度持续高位,发文量稳定增长,研究重心从模式植物向粮食作物,经济作物园艺植物转移,进一步延伸至林木和中药等研究领域,体现了技术向农业生产实际需求的转化。
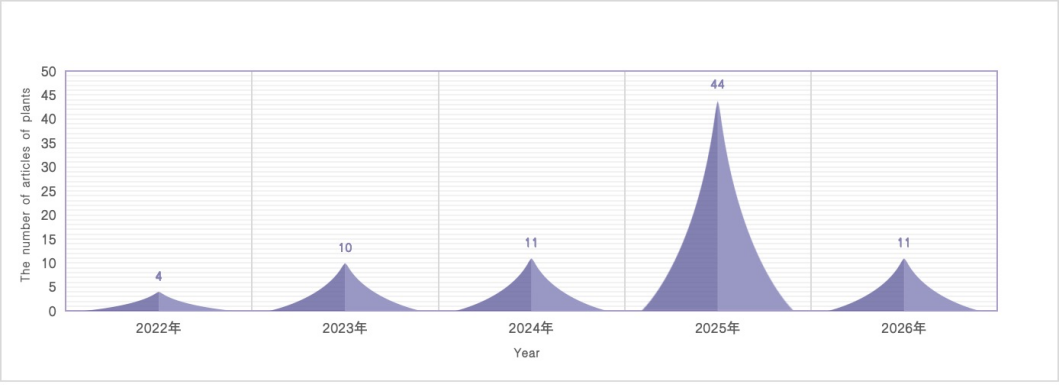
Date of publication (Until 2026 April) of plants
技术平台格局——从国外平台主导到国产技术突破
国外平台以10X Visium、Xenium、MERFISH为代表,占据早期市场主导地位。其中10× Visium凭借成熟的实验流程、全转录组覆盖能力,早期成为植物研究最常用的平台之一,广泛应用于拟南芥[1]、大豆[2]、棉花[3][4]、蝴蝶兰[5]等多物种组织解析。然而近年来,国产平台(如BMKMANU、Stereo-seq)迅速崛起,在组织适配、分辨率、实验稳定性、数据质量等方面均有突出表现,受国产高分辨、植物适配平台冲击,截至2022年底,10X Visium占植物ST研究约60%,而到2025年9月已降至40%[6]。
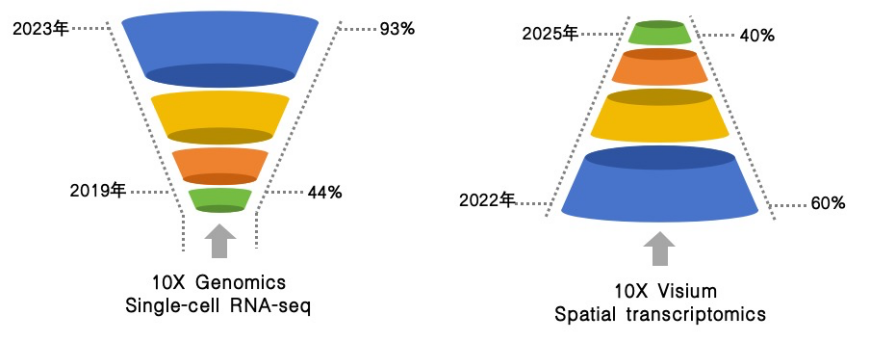
Date of publication (Until 2026 April) of plants
从2022到2025年的植物空间转录组发文数据中,两大趋势清晰可见:国产平台全面崛起,研究从模式物种走向非模式应用。
技术格局上,10X Visium占比从50%持续下滑至30%,以BMKMANU、Stereo-seq为代表的国产平台占比攀升至70%,凭借植物专属优化的技术优势,成为科研首选。
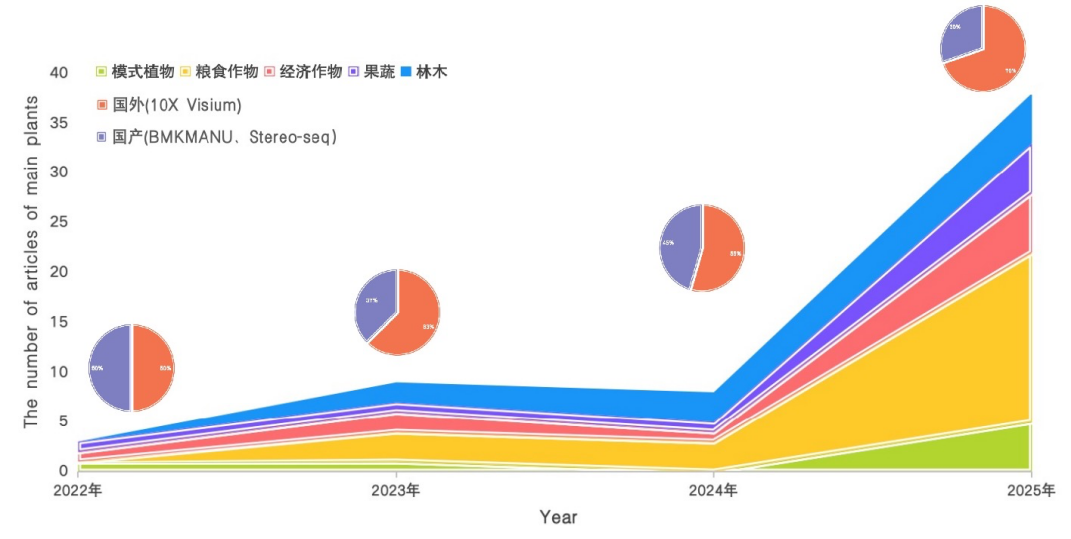
Date of publication (Until 2025) of main plants
研究物种上,模式植物占比持续收窄,粮食作物、经济作物等非模式植物发文量爆发式增长,植物空间组学彻底从技术验证走向农业应用,为作物育种、品质改良提供了核心技术支撑。

Plants with published spatial transcriptome studies(Until April 2026)
百迈客生物多年打磨空间转录组学在植物中研究应用中的技术,包括植物组织冷冻包埋、冷冻切片染色、组织优化、数据分析,特别是针对植物空间转录组数据分析,目前植物空间转录组已在千余种物种上积累丰富经验,建立植物组织透化体系,主要包括根,茎,叶,花,幼嫩果实,种子等组织类型。其BMKMANU S系列空间转录组技术(http://www.biomarker.com.cn)作为百迈客生物专为植物样本特性深度优化的空间转录组技术平台,针对植物细胞壁厚、液泡占比高、多酚/叶绿素干扰强、组织类型复杂等痛点,从样本制备、捕获效率到数据分析全链条完成了植物专属适配,已成为非模式植物、粮食作物、经济作物、林木等研究的常用技术,深度覆盖植物科学全场景研究。
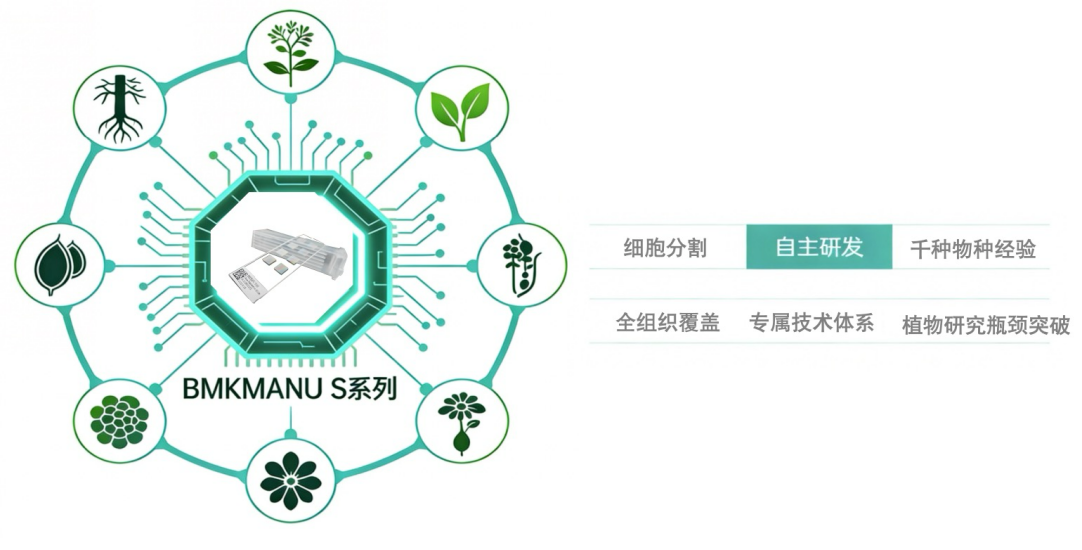
Advantages of BMKMANU S Spatial Transcriptomics
植物空间转录组研究在样本制备、透化、测序与数据分析环节存在显著技术壁垒,整体研究难度远高于动物领域。据不完全统计,截至2026年4月,全球已发表相关文章仅约77篇(不含综述类),近年发文量呈稳步增长态势,反映出该领域正从技术探索迈向应用爆发期。其中,百迈客生物BMKMANU S系列空间转录组凭借对植物样本优化的技术积累与成熟的空间转录组解决方案,已助力发表15篇高水平研究论文(含见刊及预印本,不含综述),占总发文量近20%。其研究方向覆盖多物种多组织,集中发表于Molecular Plant、PNAS、Advanced Science、Genome Biology等期刊,重点聚焦于发育调控[7]、作物抗逆[8][9]、器官发生[10]等各个方向,覆盖主粮作物、经济作物、林木、药用植物等;自2023年起,BMKMANU S3000从2D切片快速迈向3D全组织器官重构,已经积累了大量经验,该技术通过细胞级分辨率与多组学融合,成为植物发育、逆境、育种的核心工具。
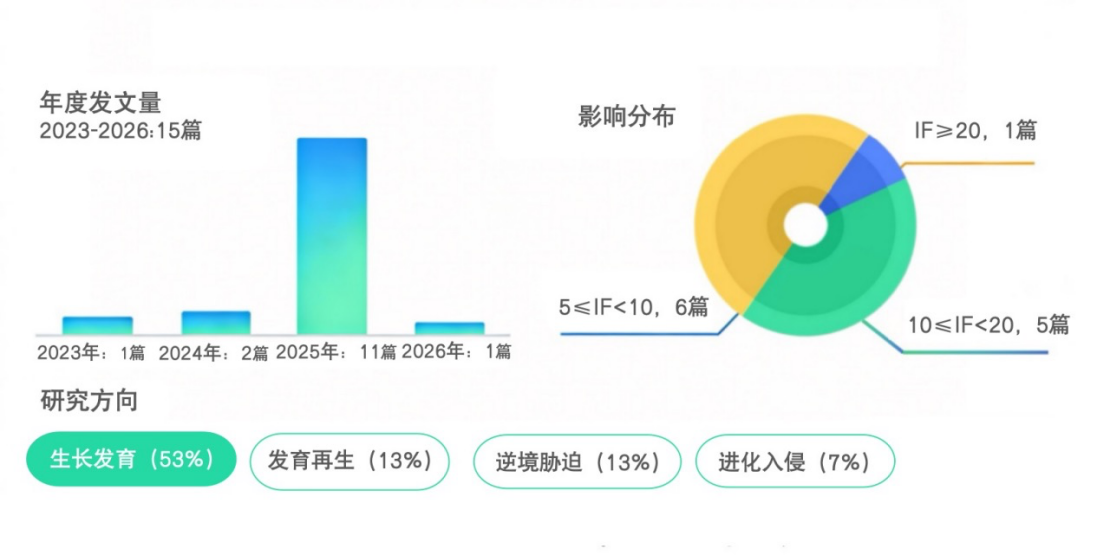
Statistics of Publications on Plant ST by Biomarker (BMK)
期刊影响因子分布——聚焦高分期刊,成果影响力持续提升
IF>40:CNS主刊
随着空间转录组技术在植物样本适配性、分辨率与通量上的关键突破与成熟度跃升,其研究价值与学术认可度实现从0到1的里程碑式跨越——2025年以前该领域长期无CNS主刊发表,而2025年一年内即有4篇相关成果发表在CNS主刊(IF>40),即:2篇Cell[11][12]和2篇Nature[13][14]。
从研究对象来看,重点依旧以模式物种拟南芥及粮食作物(大豆,水稻)为核心研究对象;从技术应用角度讲,深度整合空间转录组、单细胞(核)转录组、单细胞ATAC等多组学技术,可从细胞异质性分型、空间原位定位、染色质表观调控三个维度实现多模态数据整合;在科学问题的设计上,规避传统的发育图谱,聚焦免疫新细胞类型、衰老主动程序、土壤胁迫细胞通讯、豆科作物调控网络等高创新性议题,实现从“细胞类型注释”到“分子机制解析”的范式升级,代表植物空间组学研究的高水平。
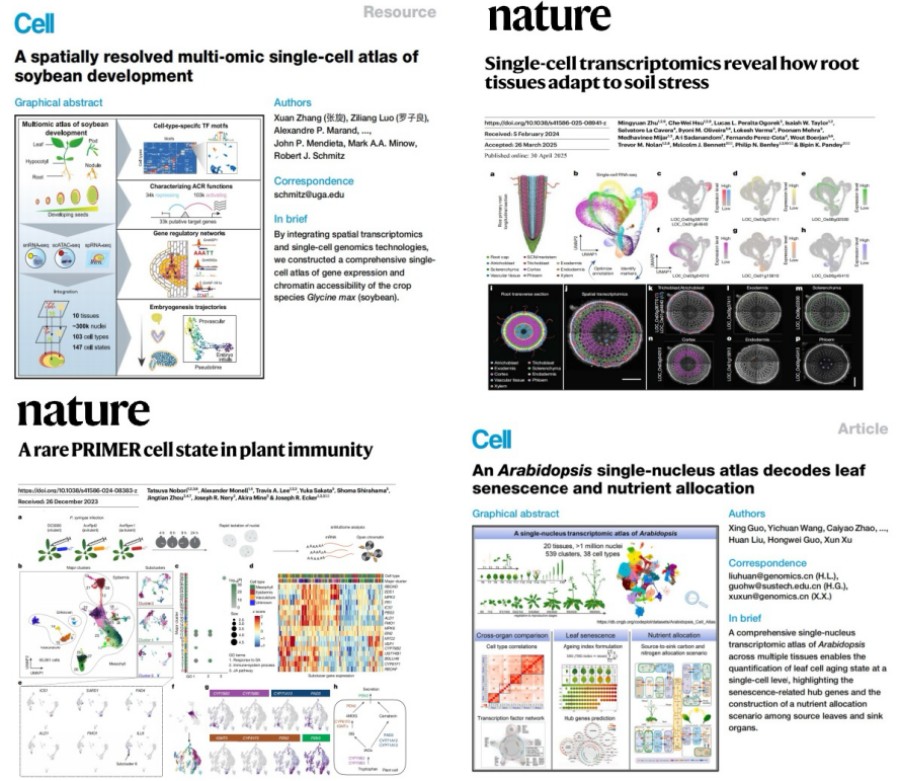
CNS Articles Published in 2025 (IF>40)
IF=24.1:Molecular Plant
Molecular Plant(简称“MP”) 是由中国科学院分子植物科学卓越创新中心与中国植物生理与植物分子生物学学会共同主办的英文学术期刊,2024年影响因子24.1,连续4年在全球植物科学研究类期刊中排名第一,是纯植物领域IF较高、国际认可度较高的权威期刊,代表植物科学领域的学术标准与前沿方向。
截止到2026年3月,4项发表于Molecular Plant的重磅研究中,以水稻[15]、小麦[7]、大豆[16]、杨树[17]等关键作物与经济林木为核心研究对象,高度聚焦植物发育生物学核心科学问题:从解析杨树茎次生维管组织中两类分生干细胞池的发育起源,到揭示水稻根系适应干旱环境的发育调控机制,再到构建大豆全生命周期器官发育的整合转录组图谱与小麦穗发育的单细胞分辨率空间转录组图谱,系统实现了从细胞命运决定、组织时空分化到关键调控因子(如HMGB1)的深度解析,为作物产量提升、抗逆遗传改良与林木生长调控提供了里程碑式的理论基础与基因资源。这一系列高质量成果的集中发表,充分彰显了MP作为植物科学重要期刊对空间转录组技术应用于作物发育研究的高度认可。

Summary of Plant Spatial Transcriptomics Research in Molecular Plants
10<IF≤20
在10<IF≤20这一类植物领域的高水平期刊(涵盖Nature Communications、Nature Plants、Advanced Science等期刊的子刊与权威专业期刊)中,植物空间转录组研究“物种覆盖全面化、研究方向场景化、技术思路多组学整合化”的核心特征,代表了当前植物空间组学领域的主流高水平研究水准。
从研究物种来看,研究已实现从模式植物到主粮作物、经济作物的全面覆盖:既包含拟南芥[18]等经典模式植物的基础机制解析,也深度聚焦玉米[19]、小麦[20]、水稻[21]、大豆[22]等主粮作物的产量性状调控,同时延伸至棉花[4]、花生[23]等经济作物,以及蝴蝶兰[5]、菠菜[24]、火龙果[25]等花卉与果蔬类物种,说明国产空间转录组技术的赋能进一步提升了在不同植物类群中的普适性,推动其成为植物学各研究方向的通用技术;从研究方向来看,主要围绕植物发育与器官建成,生物与非生物逆境响应,共生与互作,代谢与品质调控等方向,兼顾了基础研究与农业应用的双重需求。
整体而言,该IF区间的植物空间转录组研究,既代表了当前领域的主流科研水平,也为更高水平(CNS 主刊)研究奠定了方法学与数据基础,其研究模式可复制性强、应用场景广泛,是植物空间组学技术落地与成果产出的核心阵地。
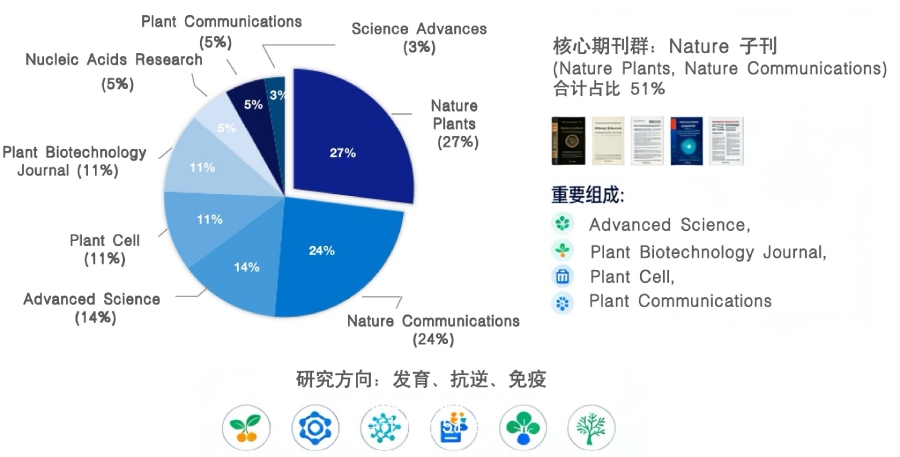
Journal Distribution of Plant Spatial Transcriptomics Publications (10<IF≤20)
5<IF≤10
在Genome Biology、Horticulture Research、Developmental Cell、PNAS、New Phytologist等5<IF≤10这类中高水平期刊区间区间期刊的植物空间转录组研究成果中,实现全类群覆盖,在模式/主粮作物基础上,大量拓展至园艺作物(番茄[26]、桃[27]、辣椒[28])、经济林木(杨树[29]、竹子[30])、特色物种(火龙果[31]、连翘[32]、榛子[33]),聚焦细分应用场景问题:果蔬品质形成、采后衰老、休眠调控、抗逆、特色作物性状解析等,问题更具物种特异性与产业针对性。

Journal Distribution of Plant Spatial Transcriptomics Publica (5<IF≤10)
组织类型分布——器官特异性研究成为核心方向
通过植物空间转录组组织研究分布与技术难度梯度可以发现,植物空间转录组研究呈现“茎 / 叶 / 根 / 花(易、多)>种子(中、中)>果实(难、少)”的梯度,因此可以看到果实组织是突破技术适配性的关键方向,植物果实因细胞壁薄、多糖、多酚,样本制备与数据质控难度极大,导致目前发表成果极少,是当前植物空间转录组研究的核心难点与技术攻坚区,而果实研究直接关联果蔬产业的品质、保鲜、育种等核心需求,因此是空间转录组技术突破后极具潜力的应用方向。
目前植物空间转录组研究的组织类型已实现“营养-生殖-特化”全维度覆盖,兼顾基础研究(分生组织、细胞分化)与应用研究(果实品质、逆境响应、育性调控),核心围绕“组织功能特化、细胞异质性、时空动态调控”三大核心,为解析植物生命活动机制、挖掘作物关键性状调控靶点提供了精准的原位研究载体。
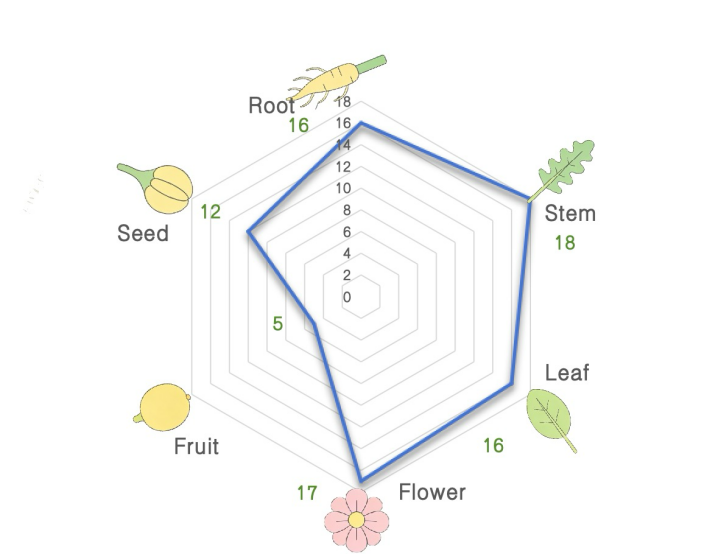
Tissue Distribution in Published Plant Spatial Transcriptomics Articles
特定组织
根系组织:根尖干细胞分化、根毛发育、逆境响应是研究重点。拟南芥根尖空间转录组构建了三维细胞分化轨迹,解析了干细胞维持机制[34];水稻根系旱地适应研究,通过比较空间转录组识别了细胞壁重塑关键通路,为耐逆育种提供靶点[15]; 同时包括根部特殊组织:植物-微生物互作组织(如根瘤),如大豆及豆科植物根瘤互作研究解析了细胞间通讯机制,为生物固肥研究提供依据[35]。
Species targeting vegetative organ (root tissue)
地上营养组织:叶片、茎秆是光合作用、物质运输的核心器官。叶片发育研究验证了”近轴-中-远轴”三域模型,解析了细胞分化调控机制,杨树叶芽休眠与再生研究,明确了不同细胞类型的表达差异,为木本植物发育研究提供参考[1]。在叶片相关研究中,胁迫响应组织(如病斑)成为新兴热点,水稻/玉米/马铃薯叶片[8][9][36]—微生物互作研究识别了宿主与微生物的空间分布热点,揭示了互作调控网络。

Species targeting vegetative organs (leaf/stem tissues)
生殖与种子组织:花芽、种子、果实发育直接关联作物产量。黄瓜花芽研究揭示了下位子房形成的细胞谱系,为葫芦科作物育种提供新方向[37];大豆种子发育研究定位了脂质代谢与蛋白质代谢的空间分布,关联营养品质调控[16];火龙果原位解析外果皮、中果皮等组织的衰老时空轨迹阐明果实衰老的细胞异质性与层特异时序调控机制[25]。

Species targeting plant reproductive organs (floral/fruit/seed tissues)
分布特征
研究组织从”器官-组织-细胞” 多尺度解析延伸,生长发育周期涵盖“seed to seed”全生命周期,同时从正常发育组织向逆境胁迫组织拓展,全面覆盖植物生命活动的核心场景[2][16]。
![Spatial multi-omics for developing soybean seeds[2]](http://www.biomarker.com.cn/wp-content/uploads/2026/04/15.jpg)
Spatial multi-omics for developing soybean seeds[2]
![Cell type cluster and spatial localization map of reported genes leading to new gene discovery for nodule development[16]](http://www.biomarker.com.cn/wp-content/uploads/2026/04/16.jpg)
Cell type cluster and spatial localization map of reported genes leading to new gene discovery for nodule development[16]
领域研究方向——多组学融合与亚细胞分辨率突破
核心研究方向
基于植物空间转录组学研究的全维度数据,结合当前前沿技术落地趋势,对植物研究领域方向进行了复盘,发现植物空间转录组技术在植物各个研究领域赛道中应运而生。
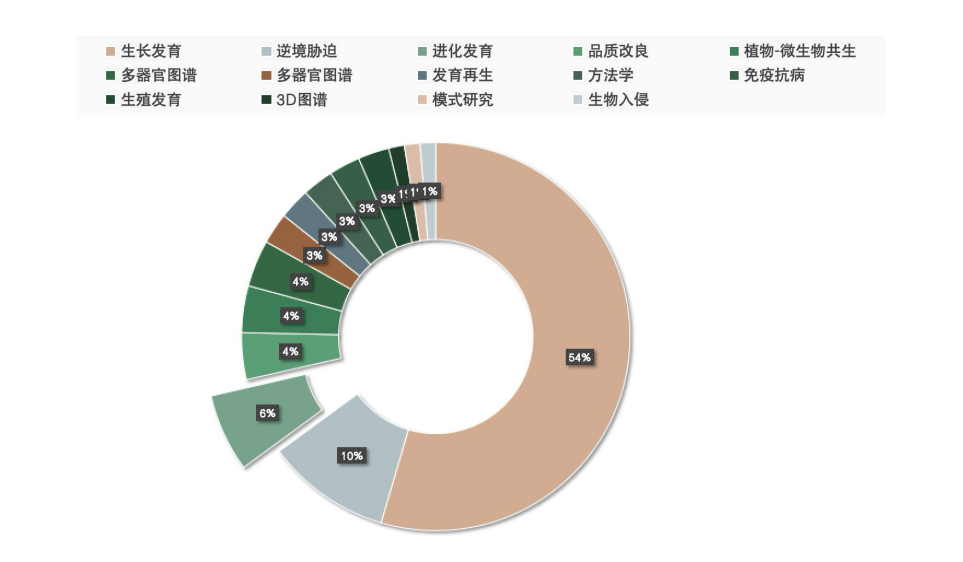
Research directions of plant spatial transcriptomics (Until April 2026)
生长发育:该方向占据绝对主导地位,聚焦植物器官发生、组织分化、胚发育等核心生命过程,依托空间转录组技术精准解析基因在组织/细胞空间的表达分布特征,深度揭示植物根、茎、叶、花、果实等关键器官的发育分子机制,是连接基础发育生物学与作物遗传改良的核心桥梁。
逆境胁迫:聚焦植物应对生物胁迫(病原菌、微生物互作)与非生物胁迫(干旱、盐碱、高温、低温)的空间分子响应机制。通过空间转录组技术可明确胁迫信号在植物组织中的传导路径、关键响应基因的空间表达模式,为培育抗逆作物品种、解析植物环境适应机制提供高精度分子靶点,是农业生产提质增效的关键研究方向。
进化发育:从空间维度解析不同植物组织器官的演化规律;
多器官图谱:构建植物全器官基因表达空间图谱,破解植物生命的“分子蓝图”;
品质改良:挖掘作物营养、农艺性状的关键调控基因;
植物-微生物共生:解析植物与微生物的互作机制(该方向目前主要以抗逆性生物胁迫为主要研究方向)。
此外包含发育再生、方法学、免疫抗病、生殖发育等技术迭代与细分研究,以及3D图谱、模式研究、生物入侵等前沿小众方向,共同推动植物时空多组学领域技术迭代与升级。
时空多组学联合分析
时空多组学联合分析是在时间(发育/胁迫动态)与空间(组织/细胞位置)两个维度进行整合分析的前沿研究方法,其中空间转录组与单细胞(核)转录组测序(snRNA-seq/scRNA-seq)、单细胞ATAC-seq、空间代谢组的联合应用,成为解析植物调控网络的主流策略,可从染色质(调控层)→基因表达(转录层)→代谢物(功能层)的层级递进式数据挖掘,实现分子调控网络的完整解析,是当前空间组学研究的热门新范式。
![Applications of spatial multiomic technologies in plant science[6]](http://www.biomarker.com.cn/wp-content/uploads/2026/04/18.jpg)
Applications of spatial multiomic technologies in plant science[6]
时空多组学彻底打破了传统单一组学的局限,完整还原了从基因到表型的全链条分子调控网络,既为植物基础研究提供了全景视角,又为作物精准育种、抗逆改良、品质提升提供了核心靶点,是连接植物基础研究与农业产业的关键技术桥梁,引领植物科学研究进入“时空组学”新时代。
参考文献:
[1]Giacomello S, Salmén F, Terebieniec BK, et al. Spatially resolved transcriptome profiling in model plant species. Nat Plants. 2017;
[2]Zhang X, Luo Z, Marand AP, et al. A spatially resolved multi-omic single-cell atlas of soybean development. Cell. 2025;
[3]Sun X, Qin A, Wang X, et al. Spatiotemporal transcriptome and metabolome landscapes of cotton fiber during initiation and early development. Nat Commun. 2025;
[4]Ge X, Yu X, Liu Z, et al. Spatiotemporal transcriptome and metabolome landscapes of cotton somatic embryos. Nat Commun. 2025;
[5]Liu C, Leng J, Li Y, et al. A spatiotemporal atlas of organogenesis in the development of orchid flowers. Nucleic Acids Res. 2022;
[6]Yao J, Marand AP, Bai Y, Schmitz RJ, Fan L. Advances in plant spatial multi-omics data analysis. Trends Plant Sci. 2026;
[7]Zhang X, Wang YP, Song X, et al. A single-cell-resolution spatial transcriptomic atlas decodes wheat spike development and yield potential. Mol Plant. 2026;
[8]Wang W, Zhang X, Zhang Y, et al. Single-Cell and Spatial Transcriptomics Reveals a Stereoscopic Response of Rice Leaf Cells to Magnaporthe oryzae Infection. Adv Sci (Weinh). 2025;
[9]Wang Q, Sun X, Sun Y, et al. Integrated Single-Cell and Spatial Transcriptomics Reveal Cell-Type Specific Immune Regulatory Networks in Maize Responding to Southern Corn Rust. Adv Sci (Weinh). 2026;
[10]Song X, Guo P, Xia K, et al. Spatial transcriptomics reveals light-induced chlorenchyma cells involved in promoting shoot regeneration in tomato callus. Proc Natl Acad Sci U S A. 2023;
[11]Zhang X, Luo Z, Marand AP, et al. A spatially resolved multi-omic single-cell atlas of soybean development. Cell. 2025;
[12]Guo X, Wang Y, Zhao C, et al. An Arabidopsis single-nucleus atlas decodes leaf senescence and nutrient allocation. Cell. 2025;
[13]Nobori T, Monell A, Lee TA, et al. A rare PRIMER cell state in plant immunity. Nature. 2025;
[14]Zhu M, Hsu CW, Peralta Ogorek LL, et al. Single-cell transcriptomics reveal how root tissues adapt to soil stress. Nature. 2025;
[15]Zhong L, Geng L, Xiang Y, et al. Comparative spatial transcriptomics reveals root dryland adaptation mechanism in rice and HMGB1 as a key regulator. Mol Plant. 2025;
[16]Fan J, Shen Y, Chen C, et al. A large-scale integrated transcriptomic atlas for soybean organ development. Mol Plant. 2025;
[17]Du J, Wang Y, Chen W, et al. High-resolution anatomical and spatial transcriptome analyses reveal two types of meristematic cell pools within the secondary vascular tissue of poplar stem. Mol Plant. 2023;
[18]Nobori T, Oliva M, Lister R, Ecker JR. Multiplexed single-cell 3D spatial gene expression analysis in plant tissue using PHYTOMap. Nat Plants. 2023;
[19]Fu Y, Xiao W, Tian L, et al. Spatial transcriptomics uncover sucrose post-phloem transport during maize kernel development. Nat Commun. 2023;
[20]Long KA, Lister A, Jones MRW, et al. Spatial transcriptomics reveals expression gradients in developing wheat inflorescences at cellular resolution. Plant Cell. 2026;
[21]Yan H, Mendieta JP, Zhang X, et al. A single-cell rice atlas integrates multi-species data to reveal cis-regulatory evolution. Nat Plants. 2025;
[22]Liu P, Li M, Ma P, et al. Spatiotemporal transcriptomic and metabolomic landscapes of wild soybean seed development reveal regulatory mechanisms of nutrient accumulation. Plant Commun. 2026;
[23]Liu Y, Li C, Han Y, et al. Spatial transcriptome analysis on peanut tissues shed light on cell heterogeneity of the peg. Plant Biotechnol J. 2022;
[24]You C, Yang H, Zhao Y, et al. Spatiotemporal Transcriptomic Atlas Reveals the Regulatory Mechanisms Underlying Early Inflorescence Development and Sex Differentiation in Spinach. Adv Sci (Weinh). 2025;
[25]Li X, Li B, Gu S, et al. Single-cell and spatial RNA sequencing reveal the spatiotemporal trajectories of fruit senescence. Nat Commun. 2024;
[26]Song X, Guo P, Xia K, et al. Spatial transcriptomics reveals light-induced chlorenchyma cells involved in promoting shoot regeneration in tomato callus. Proc Natl Acad Sci U S A. 2023;
[27]Zhao YL, Li Y, Guo DD, et al. Spatiotemporally transcriptomic analyses of floral buds reveal the high-resolution landscape of flower development and dormancy regulation in peach. Hortic Res. 2025;
[28]Reddy UK, Karnatam KS, Talavera-Caro A, et al. Uncovering the genetic architecture of pungency, carotenoids, and flavor in Capsicum chinense via TWAS-mGWAS integration and spatial transcriptomics. Hortic Res. 2025;
[29]Wei M, Hsieh JA, Dang JF, et al. Integrating scRNA-seq and snRNA-seq with spatial transcriptomics to unlock the xylem puzzle. Genome Biol. 2026;
[30]Qin N, Liu X, Li S, et al. Single-nucleus and spatial transcriptomics reveal the cell populations of intercalary meristems in bamboo. Proc Natl Acad Sci U S A. 2025;
[31]Jia J, Chen E, Tian Y, et al. Fine localization and functional differentiation of exocarp cell clusters during fruit senescence revealed by single-cell and spatial transcriptomics[J]. Postharvest Biology and Technology, 2025;
[32]Yang Y J, Zhang Z Y, Yang Y L, et al. Spatial transcriptomics provide insights into the secondary lateral rooting difficulties of tetraploid forsythia cuttings[J]. Industrial Crops and Products, 2025;
[33]Dong Y, Cheng Y, Lv Q, et al. Obstacles in sugar transportation lead to blank nut formation in Hazel (Corylus heterophylla)[J]. Industrial Crops and Products, 2025;
[34]Nobori T, Oliva M, Lister R, Ecker JR. Multiplexed single-cell 3D spatial gene expression analysis in plant tissue using PHYTOMap. Nat Plants. 2023;
[35]Liu Z, Kong X, Long Y, et al. Integrated single-nucleus and spatial transcriptomics captures transitional states in soybean nodule maturation. Nat Plants. 2023;
[36]Li Y, Dai J, Dong Z, et al. Host microenvironment in potato-Phytophthora infestans interaction revealed by single-cell spatiotemporal transcriptome. Nat Plants. 2026;
[37]Dong Z, Liu X, Guo X, et al. Developmental innovation of inferior ovaries and flower sex orchestrated by KNOX1 in cucurbits. Nat Plants. 2025.





 京公网安备 11011302003368号
京公网安备 11011302003368号