
卵巢癌仍然是最致命的妇科恶性肿瘤。
1、研究者通过全外显子组测序(WES)分析了来自77名单侧卵巢癌患者的122例新鲜冻存肿瘤组织(64个原发灶,41个转移灶和17个复发灶,其中原发灶中含有分别与转移灶和复发灶相匹配的样本)以及匹配的正常DNA(来自静脉血等)的突变情况。
结果:大多数germline和somatic突变出现在BRCA1/2(21%)和TP53(86%)基因中。通过比较同一个患者匹配的原发灶vs转移灶或者原发灶vs复发灶,发现已知癌症驱动基因突变,有77%从原发性肿瘤传递至转移性肿瘤,80%从原发性肿瘤保留至复发性肿瘤,表明在卵巢癌进展期间通常保留驱动突变。匹配的原发灶和转移性灶中的突变数目、突变频谱和突变特征非常相似,表明种植性转移是早期传播过程,而不是基于进化模型。

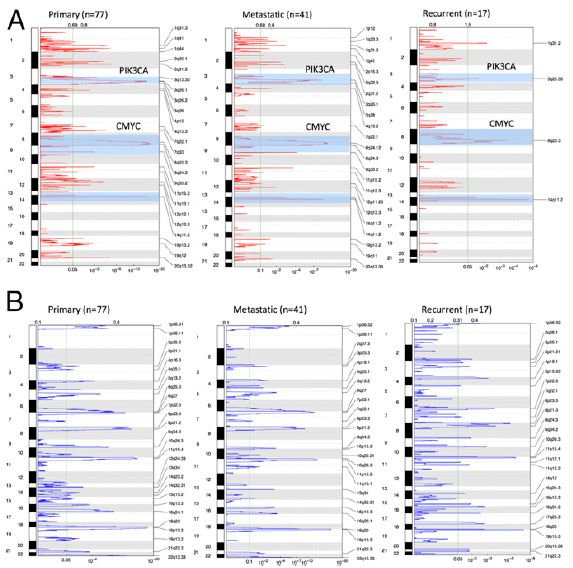
成对外显子测序数据SCNA分析表明,在原发灶与复发灶匹配的17名患者中,4名患者获得了PIK3CA扩增(3q26),2名患者在复发肿瘤中获得了c-MYC扩增(8q23-24)。GISTIC分析表明,PIK3CA和c-MYC扩增在样本间具有显著重现性,其频率在复发灶、转移灶和原发灶依次降低。
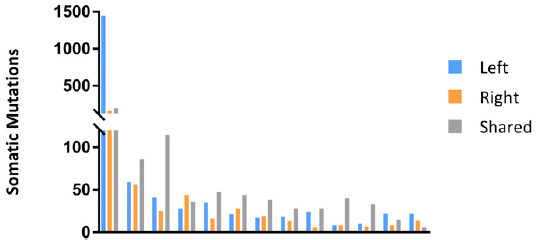
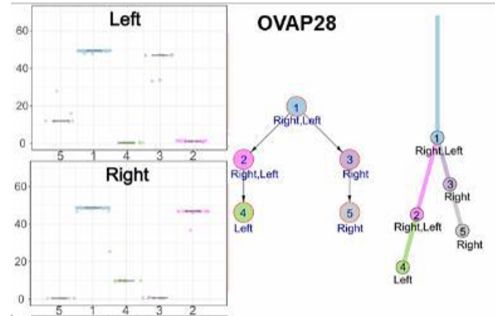
2、研究者也对13对双侧卵巢癌(synchronous bilateral ovarian cancer,SBOC)进行了测序,评估肿瘤克隆进化,以确定左右两侧肿瘤是否独立地作为2个不同的肿瘤,还是分别代表原发性和转移性肿瘤。分析表明,体细胞突变在2侧肿瘤广泛共享,所有病例中均显示2侧肿瘤起源于共同的祖先。
3、为了寻找治疗靶点,研究者评估了BET抑制剂GS-626510和JQ1对原发性肿瘤和携带c-MYC扩增的异种移植瘤的生物活性影响。源自化疗耐药肿瘤的原代细胞系和异种移植瘤对JQ1和GS-626510具有敏感性(P=0.01),表明口服BET抑制剂是一类具有复发/化疗抗性疾病患者的个性化治疗方案。且,新型BET抑制剂GS-626510在体内实验中比JQ1更有效(P=0.01)。
参考文献
Li C, Bonazzoli E, Bellone S, et al. Mutational landscape of primary, metastatic, and recurrent ovarian cancer reveals c-MYC gains as potential target for BET inhibitors[J]. Proceedings of the National Academy of Sciences, 2019, 116(2): 619-624.
如果您的科研项目有问题,欢迎点击下方按钮联系我们,我们将免费为您设计文章方案。






 京公网安备 11011302003368号
京公网安备 11011302003368号