近期,西北农林大学姜雨教授和奥胡斯大学房灵昭教授等联合团队在国际权威期刊Advanced Science发表研究成果:“Single-Cell Transcriptomic Atlases of Camels and Cattle Unravel Molecular Evolution of Digestive and Metabolic Systems”。

该研究测序策略:构建了涵盖骆驼(21个组织)与牛(33个组织)的单细胞/单核转录组图谱,并整合已发表的牛、羊、猪、小鼠及人多组织单细胞数据,开展跨物种比较分析。研究发现,骆驼不仅保留了与牛真胃同源的腺囊胃室,还演化出特有的血管平滑肌细胞,可能为其高效血压调节提供细胞基础。这项研究不仅为畜禽适应性进化提供新见解,也为人类代谢疾病研究提供了跨物种比较框架。百迈客生物为该研究提供了百创空间转录组BMKMANU S1000服务。
研究背景
对多腔胃哺乳动物进行细胞与分子特征分析,有助于深入理解消化与代谢系统的进化机制。骆驼进化出了一套独特的多室分布式消化策略,与牛的集中式消化模式形成鲜明对比。二者在消化与代谢系统中所展现的物种特异性细胞组成及分子特征差异,这引出了一个关键的科学问题:多腔胃动物适应性进化的细胞基础是什么?
研究结果
♦ 骆驼与牛的单细胞转录组图谱构建
该研究对骆驼的21种组织(160,682个细胞)和牛的33种组织(264,472个细胞)进行了单细胞RNA测序(scRNA-seq)或单核RNA测序(snRNA-seq),共注释出124种细胞类型,其中59种为骆驼和牛所共有。基于鉴定出的15,324个直系同源基因,研究者整合了两个物种的单细胞转录组数据进行分析。结果显示,肝细胞、内皮细胞、免疫细胞和上皮细胞在物种间表现出较高的相似性,而生殖细胞的相似性较低,这可能与其作为进化速率最快的细胞类型有关。本结果系统揭示了骆驼多种组织的细胞类型组成,并刻画了两种物种间对应细胞类型的保守性与异质性。
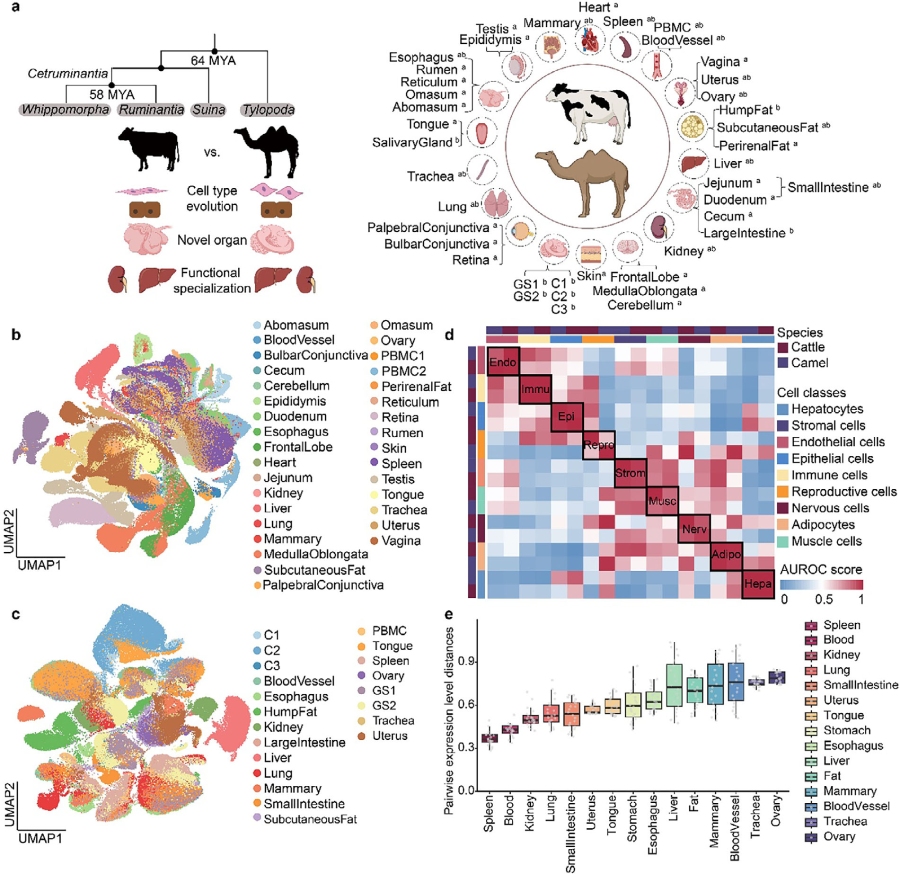
图1. 细胞图谱构建
♦ 多腔胃结构细胞的异质性分析
多腔胃是骆驼和牛高度特化消化道的标志性特征。为探究骆驼与牛胃腔中细胞类型组成及其基因表达模式的保守性与差异性,作者针对胃腔单细胞数据集进行分析,通过比较胃部结构性细胞,发现上皮细胞的聚类由组织来源决定,而非物种。
骆驼腺囊(GS)与第三胃室(C3)识别出一个独特的转录调节模块,其中包含SOX8、UNCX等调控因子,促进细胞增殖与迁移。骆驼GS与真胃具有共同起源,但已获得独特的特化特征。保守的细胞和分子特征使GS在发育过程中能够执行类似真胃的核心功能。同时,GS与C3中以高表达促增殖和迁移基因为特征的独特上皮亚型,代表了关键的谱系特异性创新。
因此,作者提出GS从共同的祖先胃结构演化而来,随后在骆驼中经历特定特化过程,这一过程可能由这些新型细胞类型驱动,以支持其独特的器官发生和功能维持。骆驼第一胃室(C1)上皮缺乏乳头结构,正向选择基因的细胞偏向性表达模式表明,自然选择在塑造骆驼和牛C1上皮细胞的特征。C1上皮的细胞类型具有保守性,且成纤维细胞是三种物种中形成C1上皮乳头状结构差异的主要细胞类型。
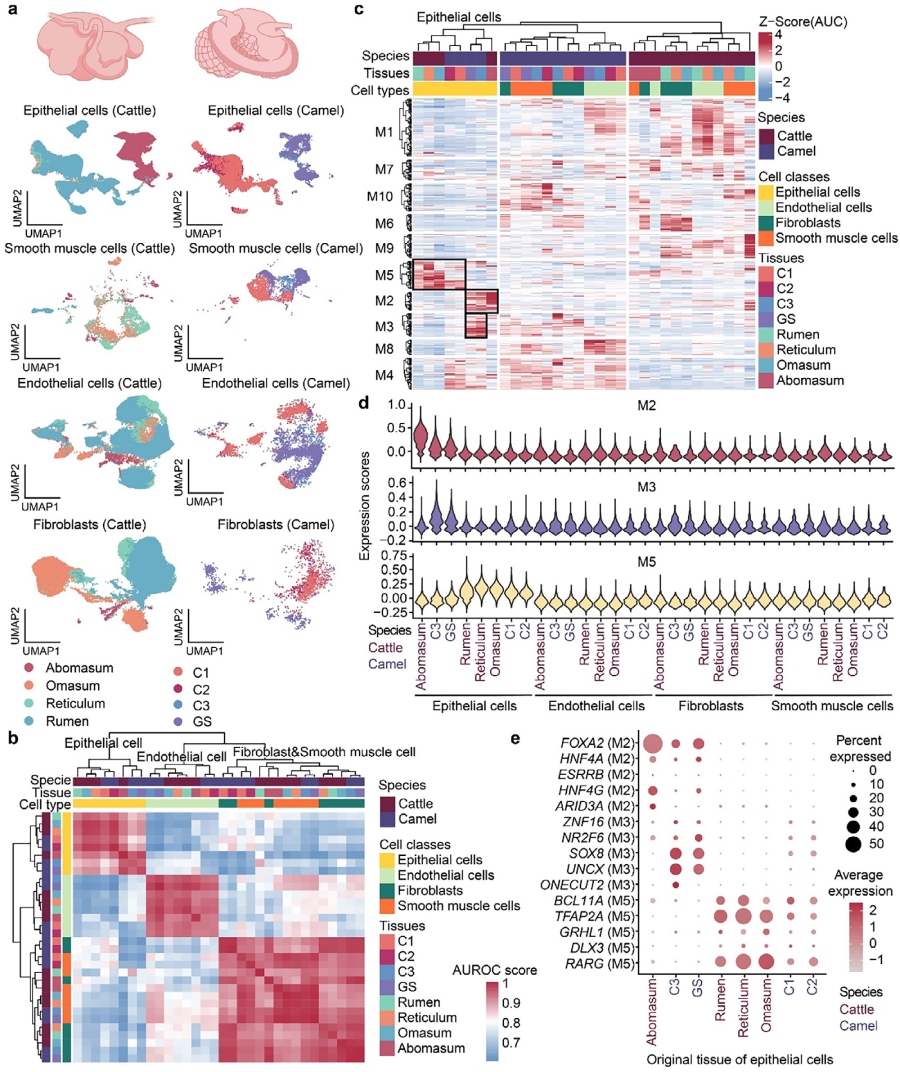
图2. 多室胃结构细胞的跨物种比较分析
♦ 骆驼与牛对营养吸收与代谢的偏好研究
为评估前胃特化对植物性饲料利用的影响,作者提取了骆驼和牛的小肠及肝脏单细胞转录组数据进行跨物种比较。
结果表明,骆驼肝细胞高表达脂酸代谢基因(如ACSL4、ACSL5、ACOX1)和PPAR信号通路相关基因,显示出更强的脂质转化与储存能力;而牛肝细胞则高表达药物代谢和淀粉蔗糖代谢基因,可能更适应饮食波动及饲料中的外源性物质处理。
在肠道方面,牛肠上皮细胞中有机盐转运基因上调,利于吸收瘤胃微生物产生的挥发性脂肪酸;骆驼肠细胞则高表达水通道蛋白基因,与其干旱适应机制相符。这些发现共同表明,骆驼与牛在营养吸收与代谢方面存在明显差异,且骆驼肝脏在长链脂肪酸代谢上更具优势,可能有助于避免过度脂肪沉积。
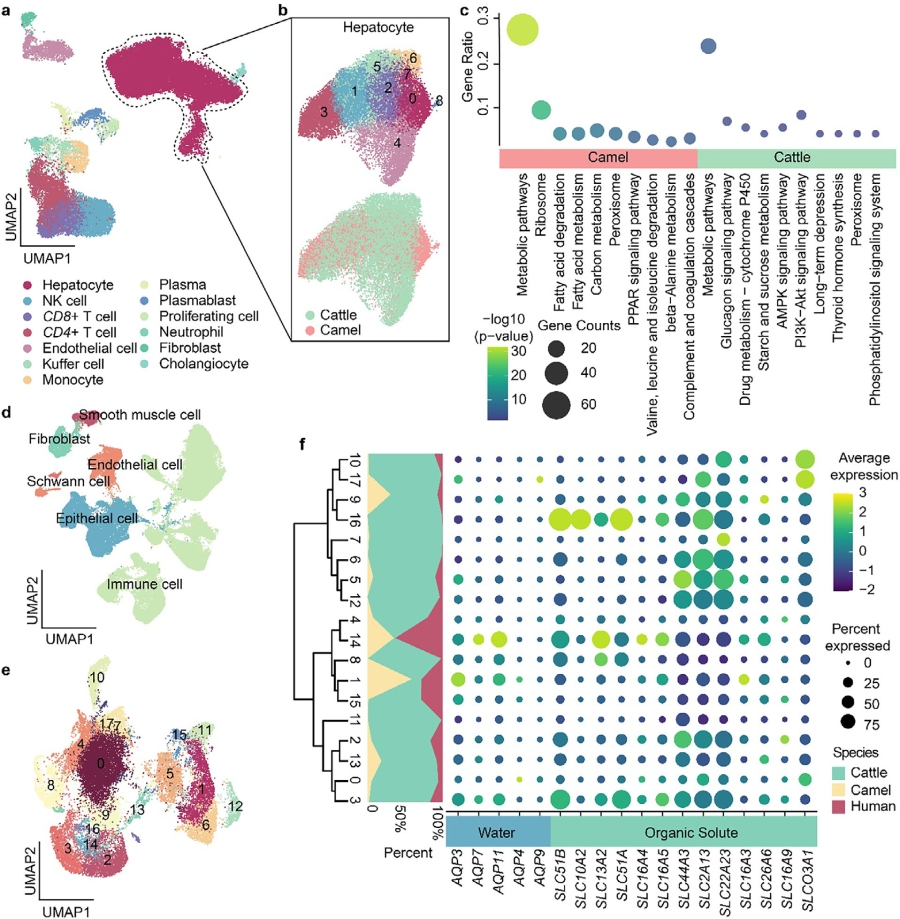
图3. 骆驼与牛肝脏、小肠单细胞转录组数据比较
♦ 肾脏血管平滑肌细胞(VSMCs)异质性分析
为探究与骆驼肾脏独特功能相关的主要细胞类型及其分子特征,作者聚焦于骆驼肾脏的单细胞转录组数据,鉴定出一类特殊的血管平滑肌细胞,并将其命名为S100A4+VSMCs。该细胞高表达血管紧张素II受体基因AGTR1,而收缩相关基因(如MYH11)表达较低。比较分析显示,S100A4+VSMCs未在小鼠、猪、牛及人等哺乳动物的肾脏中被发现,表明其可能为骆驼所特有。
作者进一步采集骆驼肾脏组织进行空间转录组学分析,证实了S100A4+VSMCs在肾脏中的实际存在,并发现其主要分布于肾小球的入球与出球小动脉区域。与典型的收缩型VSMCs相比,S100A4+VSMCs被预测具有更高的分化程度。通过受体‑配体共定位分析,研究提示这两类血管平滑肌细胞亚型之间存在直接相互作用,且可能通过DLK1‑NOTCH3信号轴介导。S100A4+VSMCs可能通过调节肾小球入球与出球小动脉对血管紧张素II的局部反应,在血压调节中发挥重要作用。
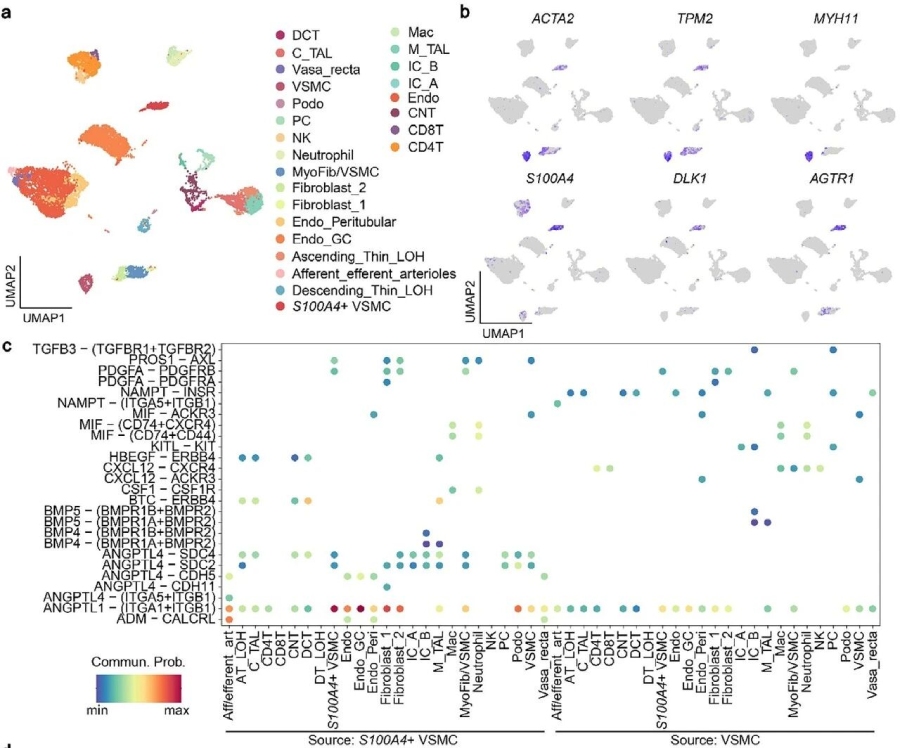
图4. 骆驼肾脏中S100A4+VSMCs的鉴定
研究总结
该研究构建了骆驼与牛的多组织单细胞转录组图谱,并提供了骆驼肾脏的空间转录组数据,为解析物种特异性生物学特征及其进化历程提供了重要资源。基于胃、肾脏及肝脏等关键消化代谢器官的跨物种比较,研究不仅验证了骆驼胃部的起源假说,还揭示了特定细胞类型的基因表达变化如何帮助骆驼肝脏避免过度脂肪沉积。
此外,作者在骆驼肾脏中发现了一类新型血管平滑肌细胞,该细胞可能在肾脏适应干旱、高盐环境的过程中发挥关键调节作用。综上所述,该研究从分子与细胞层面阐释了骆驼适应性进化的内在机制,为理解哺乳动物器官系统的进化与功能多样化提供了新的视角。






 京公网安备 11011302003368号
京公网安备 11011302003368号