2022年10月19日,北京大学医学部姜长涛团队联合美国国立卫生研究院、浙江大学医学院、复旦大学基础医学院和温州医科大学的研究团队在国际期刊《Nature》杂志在线发表了题为“Gut bacteria alleviate smoking-related NASH by degrading gut nicotine”的重磅研究。该研究解析了肠道尼古丁积累在非酒精性脂肪性肝炎进展中的作用,发现了人类肠道中一种能够代谢尼古丁的内源性细菌,并提出了一种可能的减少吸烟加剧NAFLD进展的途径。百迈客为该研究提供了宏基因组测序服务。

研究背景
吸烟是人类常见的不健康行为之一,世界卫生组织将吸烟列为可预防死亡的主要原因。戒烟是延长预期寿命的有效方法,但由于尼古丁的强大成瘾性和戒断症状,戒烟并不容易实现。尼古丁降解最近被认为是阻断尼古丁诱发的病理的一种策略。NAFLD(非酒精性脂肪肝病)包含广泛的病理,通常从简单的脂肪变性发展为 NASH(非酒精性脂肪性肝炎),然后在某些情况下发展为肝硬化和肝癌。由于肠道产生的代谢物在通过肠-肝轴的 NAFLD 进展中具有关键作用,因此建立肠道尼古丁积累、肠源性代谢物和NAFLD进展之间的关系可以为吸烟相关的肝脏疾病提供新的线索。
研究设计
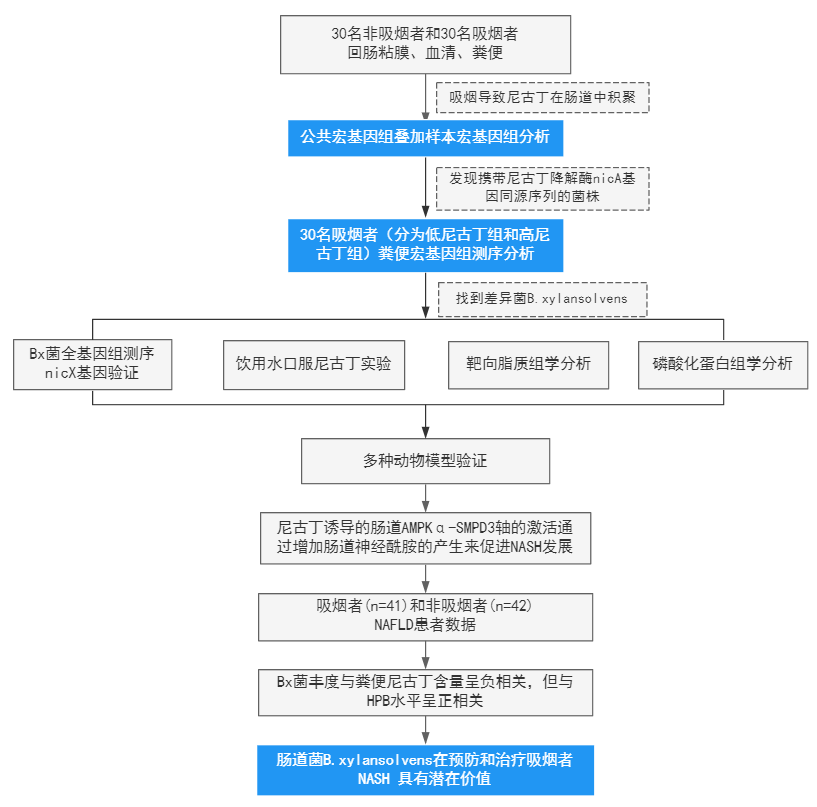
三个队列:
队列1:30名非吸烟者和30名吸烟者采集血清和粪便样本。
队列2:从41名确诊为NAFLD的吸烟者身上采集了血清和粪便样本。
队列3:42名经活检确诊为NAFLD的非吸烟者的血清和粪便样本。
研究结果
1.肠道细菌降解回肠中尼古丁
在吸烟或使用尼古丁贴剂期间,人体唾液和胃液中可检测到高水平的尼古丁,表明其在消化道中积累,在消化道中可能产生病理性作用。为了确认吸烟期间尼古丁是否在肠道中积聚,研究者收集了 30 名非吸烟者和 30 名吸烟者的回肠末端黏膜活检、血清和粪便样本。在吸烟者的回肠粘膜组织中检测到高水平的尼古丁,表明在吸烟期间尼古丁会在肠道中积聚(图 1a)。进一步评估了通过三种先前描述的给药方法(即烟雾暴露,口服和皮下)。在上述小鼠模型中始终观察到回肠尼古丁积累(图 1b、c 补充图1a)。这些结果表明,吸烟期间的尼古丁水平在肠道中积累的程度相对较大,这可能具有病理生理学意义。
在尼古丁饮用水输送模型中,无菌(GF)小鼠的回肠内容物和回肠组织中的尼古丁浓度都高于SPF小鼠,这表明内源性肠道细菌有助于尼古丁的降解(图1C)。为了确定特定的人类内源性尼古丁降解肠道菌群,研究者从公共宏基因组数据库中筛选携带已知尼古丁分解代谢基因的潜在菌株。在几个菌株中发现了nicA(一种已知的尼古丁降解酶)的同源序列,表明这些菌株具有降解尼古丁的潜力(补充图1B)。对30名吸烟者的粪便样本进行了宏基因组学分析,以确定与回肠尼古丁浓度降低最相关的物种。根据回肠尼古丁水平,参与者被定义为低尼古丁(LN)或高尼古丁(HN)(扩展数据图1C)。值得注意的是,LN组和HN组之间在吸烟史(包括吸烟年限和每天吸烟数量)方面没有显著差异(补充表1和2)。在两组之间没有发现α-和β-多样性的差异;但是,几个菌株在LN和HN组之间显示了不同的丰度(图1D)。在宏基因组数据库和宏基因组学的基础上,发现B.xylansolvens可能含有尼古丁分解代谢基因,并被鉴定为与LN和HN组之间的分离相关的主要驱动因素(图1D)。
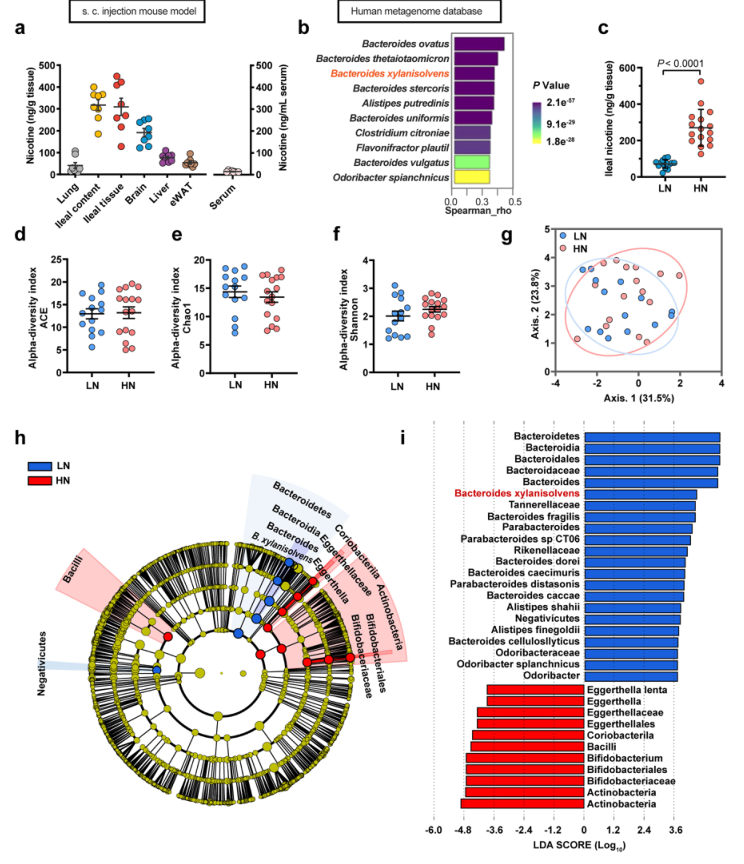
扩展数据图 1.高尼古丁和低尼古丁吸烟者的肠道菌群组成差异
研究者进一步对B.xylansolvens进行了体外实验,发现在培养基中添加尼古丁对菌的生长速度没有影响;然而,B.xylansolvens有效地降解了添加到培养基中的尼古丁。为了检测B.xylansolvens中尼古丁的降解代谢产物,进行了B. xylanisolvens 的发酵实验,并用层析法分离了尼古丁代谢物。用核磁共振对代谢产物进行了进一步的表征,鉴定为4-羟基-1-(3-吡啶)-1-丁酮(HPB),可在B.xylansolvens菌的培养基中检测到。为了验证B.xylansolvens在体内对尼古丁的降解特性,将该细菌定植到通过上述三种递送策略给予尼古丁的SPF小鼠体内,发现可以在体内降解尼古丁,并伴随着HPB的增加(图1E)。
接下来,研究者对B.xylansolvens进行了全基因组测序,并研究了B.xylansolvens中尼古丁分解代谢的生物合成基因。在由这些测序基因编码的潜在的尼古丁分解代谢蛋白中,nicX蛋白(由nicX基因编码)具有类似于已知的尼古丁降解酶nicA的计算模型的预测核心结构,nicX可在体外降解尼古丁。
为了进一步验证nicX的尼古丁降解能力,将NicX导入大肠杆菌或在B.xylansolvens中敲除。与野生型(WT)大肠杆菌相比,nicX-knockin大肠杆菌在体内外获得了降解尼古丁和产生HPB的能力(图1F和扩展数据图2J)。此外,B.xylansolvens中的nicX缺乏导致其尼古丁降解能力的丧失(图1G和补充图2K)。WT和nicX基因敲除的B.xylansolvens的生长曲线没有发现显著变化(扩展数据图2L)。综上所述,结果表明尼古丁在不同的给药途径中在肠道中积累,B.xylansolvens在nicX存在的情况下具有降解尼古丁的能力。
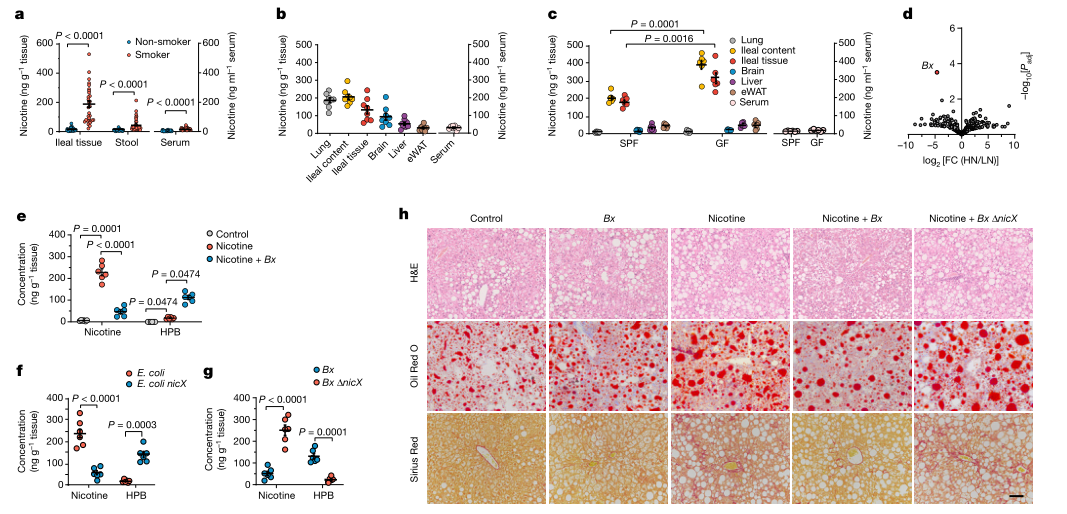
图 1.鉴定肠道尼古丁积累和肠道细菌介导的的肠道尼古丁降解。
2.尼古丁降解延缓NAFLD进展
通过饮用水口服尼古丁是研究尼古丁相关慢性代谢性疾病的一个广泛使用的模型。为了确定肠道尼古丁积累的作用以及B. xylanisolvens对其降解在NAFLD进展中的影响,用PBS(对照组)、B. xylanisolvens、尼古丁水、B. xylanisolvens加尼古丁水或nicX基因敲除B.xylansolvens加尼古丁水处理SPF鼠20周。WT和nicX基因敲除B. xylanisolvens成功地在HFHCD(高果糖高胆固醇饮食)喂养的SPF小鼠中定植(扩展数据图3A)。然而,尼古丁的降解只在被B. xylanisolvens定植的组中观察到(扩展数据图3B)。各组之间没有观察到明显的体重的变化(扩展数据图3C,d)。
肝肿块、血清丙氨酸氨基转移酶水平与对照组相比,尼古丁处理组小鼠的肝脏质量、血清丙氨酸氨基转移酶(ALT)和天冬氨酸氨基转移酶(AST)水平以及肝脏甘油三酯水平都较高(扩展数据图3E-I)。两组间血清甘油三酯、肝脏和血清胆固醇酯及血清非酯化脂肪酸水平无显著差异(扩展数据图3j-m)。根据苏木精伊红(H&E)、油红O和天狼星红染色,在HFHCD喂养条件下,水中补充尼古丁加速了NAFLD的进展,这种加速伴随着更严重的肝脏脂肪变性、炎症和纤维化(图1H和扩展数据图3n-r)。此外,涉及肝脏脂肪代谢、促炎细胞因子产生和胶原合成的mRNAs的相对表达在添加尼古丁的水处理中被诱导(扩展数据图3s-u),而这些Nash指标通过WT B.xylansolvens的定植而得到改善,但与nicX缺乏的b.xylansolvens无关(图1H和扩展数据图3c-u)。
这些数据表明,尼古丁降解菌的定植可以减少尼古丁诱导的NASH,并且这种作用依赖于nicX的表达。
3.尼古丁激活肠道AMPKα-1
与之前的研究一致,研究者发现尼古丁处理以剂量依赖的方式诱导回肠器官中AMPKα在Thr172磷酸化(扩展数据图4A,b)。此外,吸烟在回肠末端激活了回肠AMPKα,这种作用的强度与吸烟者组织中的尼古丁水平呈正相关(图2A)。此外,在所有三种尼古丁暴露的SPF小鼠模型中,回肠中的磷酸化AMPKα(p-AMPKα)均增加(扩展数据图4C-e)。AMPKα有两种亚型,即AMPKα1和AMPKα2)。研究者建立了肠上皮特异性AMPKα1(Prkaa1ΔIE)和AMPKα2(Prkaa2ΔIE)基因敲除小鼠系(扩展数据图4F)。
在没有肠道AMPKα1的情况下,尼古丁完全失去了激活AMPKα1的能力,而在没有肠道AMPKα2的情况下,尼古丁诱导的p-AMPKα的增加仍然发生,这表明AMPKα1是尼古丁在肠道中的主要靶点(扩展数据图4F)。B.xylansolvens的定植抑制尼古丁诱导的AMPKα在回肠的磷酸化(扩展数据图4G)。与B.xylansolvens相似,nicX-knockin大肠杆菌在体内能够抑制尼古丁诱导的回肠AMPKα的磷酸化(扩展数据图4H)。然而,在没有nicX的情况下,没有观察到B.xylansolvens介导的抑制作用(扩展数据图4I)。因此,B.xylansolvens在nicX存在下减轻了尼古丁诱导的回肠p-AMPKα的激活,这得到尼古丁分解代谢物HPB不能激活回肠p-AMPKα的支持(扩展数据图4J)。
关于肠道AMPKα1在尼古丁加速的非酒精性脂肪肝进展中的作用,进一步发现肠道上皮AMPKα1的缺失有助于改善尼古丁加速的NASH小鼠模型的肝脏脂肪变性、炎症和纤维化(图2B-f和扩展数据图5a-m)。
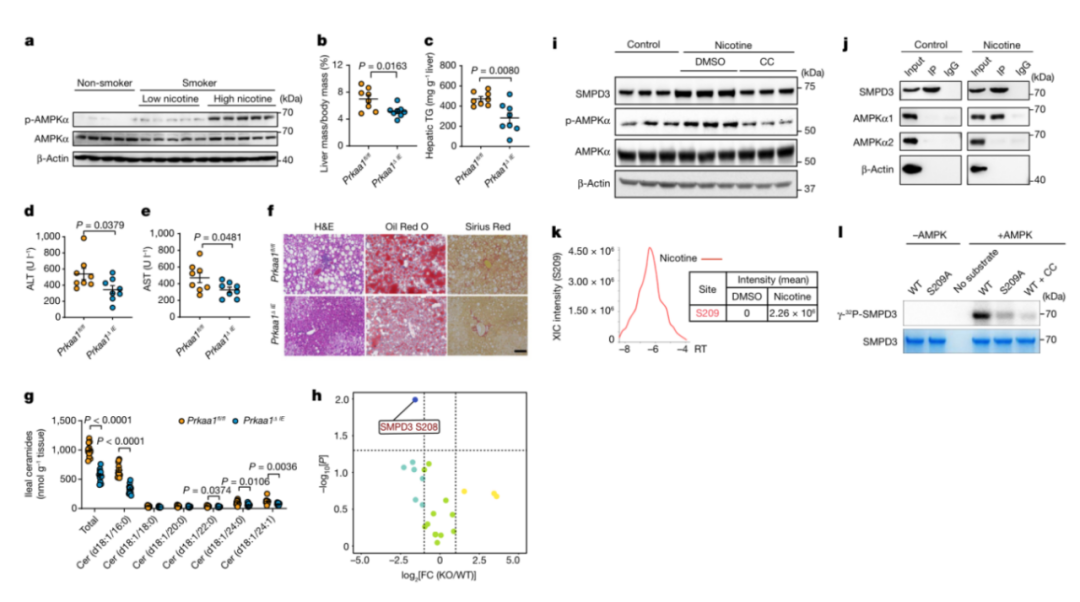
图 2.尼古丁诱导的 NAFLD 进展中肠 AMPKα-SMPD3 轴的激活
4.P-AMPKα使SMPD3在Ser208/20处磷酸化
脂质被认为在 NAFLD 进展中具有重要作用,因为它们是该病理学中肠道和肝脏之间串扰的关键介质。研究者进一步对回肠进行了靶向脂质组学分析,并确定神经酰胺是导致Prkaa1基因敲除(KO)和对照(WT)肠上皮在尼古丁治疗下基于聚集分化的主要代谢物(扩展数据图5n,o)。在尼古丁饮用模型中没有肠道 AMPKα1 的情况下,回肠神经酰胺谱较低(图 2g)。基于尼古丁饮用模型回肠上皮的磷酸化蛋白质组分析(扩展数据图 5p),肠上皮AMPKα1的缺失显著降低了SMPD3的Ser208位的磷酸化(图2H和扩展数据图5Q)。
在回肠器官中,尼古丁处理没有改变SMPD3的mRNA水平。然而,用AMPK激酶活性抑制剂或表达激活域突变体都可以缓解尼古丁诱导的SMPD3蛋白水平的增加(图2I),这表明尼古丁对SMPD3的影响是翻译后的。发现在尼古丁处理下,SMPD3与AMPKα1结合(图2J)。使用蛋白质翻译后修饰磷酸化位点预测工具GPS 2.0分析预测Ser208(小鼠)是AMPK最有可能的磷酸化位点(扩展数据图6C)。SMPD3中包括Ser208(人类中的Ser209)在内的多肽满足AMPK的磷酸化底物基序,并且在进化上高度保守(扩展数据图6D)。据报道,SMPD3的稳定性受5个保守的丝氨酸位点的磷酸化调节。在尼古丁治疗组检测到Ser209磷酸化增加(图2K和扩展数据图6E)。SMPD3(WT)可被AMPKα1直接磷酸化,当Ser209突变或给予AMPK抑制剂时,这种磷酸化几乎消失了(图2L)。
为确定SMPD3在Ser209位的磷酸化是否影响SMPD3蛋白的稳定性,将WT、S209A(缺失磷酸化突变体)和S209D(持续磷酸化突变体)SMPD3分别导入SW480细胞,并用尼古丁和放线菌酮(CHX)处理。发现Ser209的磷酸化保护SMPD3蛋白不被降解(图3A)。在尼古丁饮用模型中分离的有机化合物中,观察到缺乏肠上皮AMPKα1的小鼠的有机化合物中SMPD3的降解速度更快(扩展数据图6F)。
此外,在尼古丁处理的SW480细胞中,SMPD3在Lys103处的去泛素化程度显著高于DMSO处理的细胞(图3B和扩展数据图6G)。通过免疫沉淀,我们发现泛素化的SMPD3(Lys103)主要包含经典的Lys48-连接Ub链(Lys48-Ub),而不是Lys63-Ub,后者被尼古丁处理减少(图3C,d和扩展数据图6h)。S209A突变逆转了尼古丁诱导的SMPD3 Lys48-Ub的减少,K103R突变进一步缓解了这一下降(图3e和扩展数据图6i)。此外,开发了抗p-SPMD3(S209)和抗Ub-SMPD3(Lys103)抗体(扩展数据图6J,k),并证实尼古丁诱导的总SMPD3蛋白的增加是由于SMPD3磷酸化水平升高,随后泛素化减少(图3F)。
这些发现表明,尼古丁激活的AMPKα在Ser209位磷酸化SMPD3,这反过来又抑制SMPD3上Lys103的泛素化和随后的Lys48-Ub降解途径,从而提高SMPD3蛋白的稳定性及其蛋白水平(图3G)。进一步检测到尼古丁诱导的SMPD3在Ser208位的磷酸化,同时在Lys103位的SMPD3泛素化减少,这可以通过在NicX存在下B.xylansolvens的定植来缓解(图3H)。吸烟者回肠的磷酸化和总SMPD3蛋白水平也高于非吸烟者,这与回肠尼古丁含量有关;而泛素化的SMPD3蛋白水平在非吸烟者、LN和HN组依次降低(图3I)。
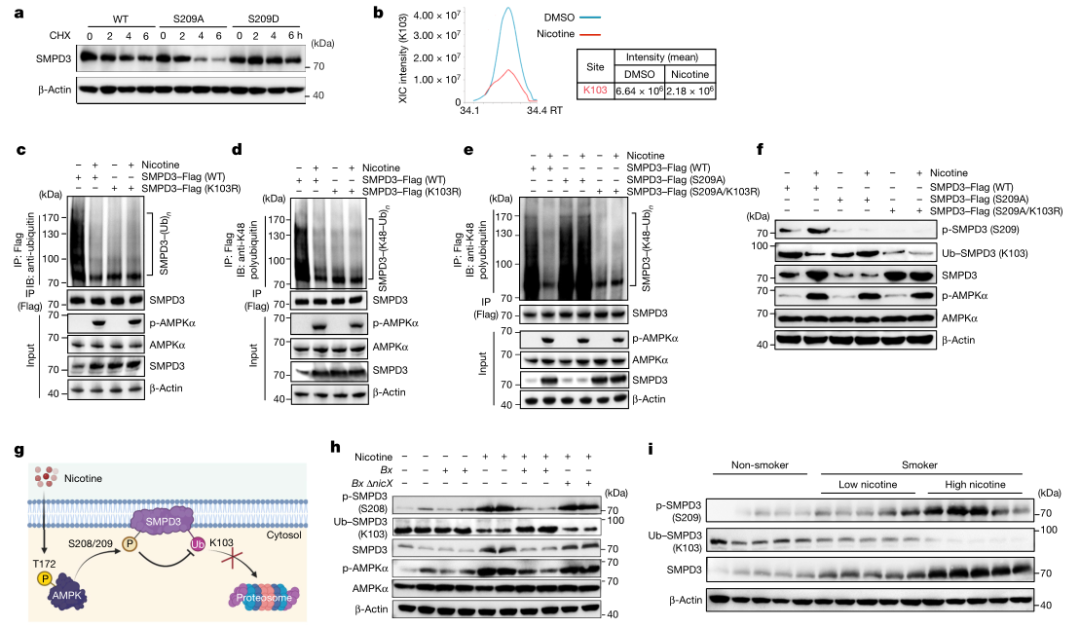
图3.由于泛素化介导的降解减少,磷酸化的SMPD3更稳定
5.P-AMPKα-SMPD_3-神经酰胺轴与NASH
SMPD3被认为是代谢性疾病的病理加速器。将SMPD3抑制剂GW4869应用于有机化合物以抑制SMPD3活性。GW4869降低了尼古丁处理下类器官及其上清液中的神经酰胺水平。慢病毒表达的SMPD3被用于从尼古丁饮用模型恢复Prkaa1基因敲除的回肠器官中SMPD3的表达。正如预期的那样,SMPD3的过表达逆转了由于回肠器官中AMPKα1缺乏而导致的神经酰胺水平的降低。在尼古丁加速的NASH小鼠模型中,在B. xylanisolvens存在的情况下,被B.xylansolvens定植的SPF小鼠回肠神经酰胺减少,这是由于肠道p-AMPKα-SMPD3轴被抑制所致。
在尼古丁加速的NASH小鼠模型中,为了证实神经酰胺谱的调节是否与肠上皮细胞AMPKα1缺乏所致的NASH改善有关,研究者通过每日腹腔注射神经酰胺(D18:1/16:0)。神经酰胺给药可逆转AMPKα1对肠上皮遗传破坏引起的肝脏脂肪变性、炎症和纤维化的保护作用。此外,口服GW4869降低了回肠神经酰胺的水平,并且在尼古丁饮用模型中伴随着较低的NAFLD严重程度。
总之,尼古丁诱导的肠道AMPKα-SMPD3轴的激活通过增加肠道神经酰胺的产生来促进非酒精性脂肪肝的进展,因此抑制SMPD3是一种潜在的缓解肝脏脂肪变性、炎症和纤维化的策略。
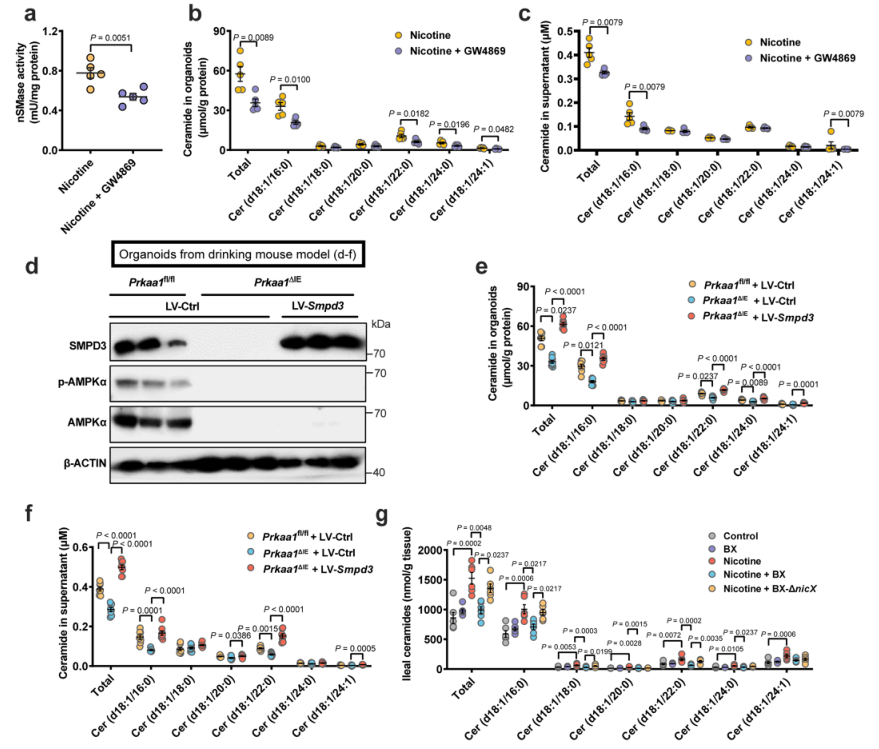
扩展数据图 7. p-AMPKα和SMPD3在肠道神经酰胺产生中的相互作用
6.B. xylanisolvens与临床非酒精性脂肪肝
为了阐明我们的发现与人类NAFLD进展之间的相关性,我们收集了83名经活检证实的NAFLD患者的数据,这些患者被分为吸烟者(n=41)和非吸烟者(n=42)。在吸烟者中,NAFL、Borderline NASH和Defined NASH在烟草吸烟史(包括吸烟年限和每天吸烟数量)方面没有显著差异。然而,我们发现B.xylansolvens水平与NAFLD严重程度呈负相关,随着NAFLD的进展,粪便中尼古丁水平逐渐增加,粪便中尼古丁降解产物HPB相应地随着NAFLD的进展而减少(图4C,d)。在吸烟者中,B.xylansolvens丰度与粪便尼古丁含量呈负相关,但与HPB水平呈正相关(图4e,f)。
在代谢指标方面,粪便中B.xylansolvens和HPB的存在与血清ALT和AST水平呈负相关,而尼古丁浓度呈正相关(图4G)。这些结果表明,B.xylansolvens介导的尼古丁降解可能保护吸烟者的肝功能。NASH患者的血清神经酰胺水平,尤其是主要来自肠道的神经酰胺(D18:1/16:0)水平显著高于NAFL患者(图4H),并与B.xylansolvens的丰度呈负相关(图4I)。
然而,在非吸烟者中,没有观察到B.xylansolvens的丰度与NAFLD严重程度之间的相关性。综上所述,这些数据证实了肠道尼古丁蓄积是吸烟者临床NAFLD进展的危险因素,同时也表明具有尼古丁降解活性的B.xylansolvens具有保护作用。
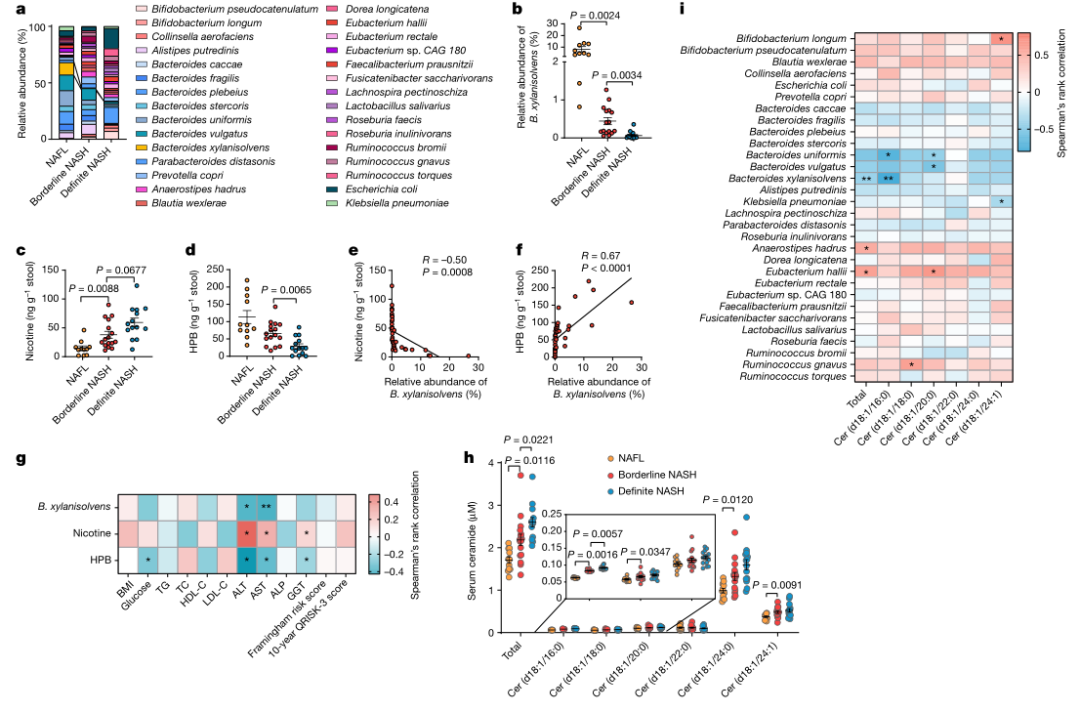
图 4. B. xylanisolvens介导的尼古丁降解与临床 NAFLD 进展呈负相关。
总结
该研究发现尼古丁在吸烟期间在肠道中积聚并加速NAFLD的进展,但它可以被人类共生菌B. xylanisolvens 有效降解。揭示了了肠道尼古丁积累的病理影响,并确定了一种内源性尼古丁降解肠道细菌,该细菌对预防和治疗吸烟者的 NASH 具有潜在价值。
姜长涛教授、Frank Gonzalez研究员、虞朝辉教授、李洋研究员、郑明华教授为本文的共同通讯作者。北京大学医学部基础医学院博士后陈博、美国国立卫生研究院博士后孙露露、北京大学医学部基础医学院博士研究生曾广易、浙江大学医学院第一附属医院沈哲教授、北京大学医学部基础医学院博士后汪锴、复旦大学基础医学院博士研究生尹利敏为本文的共同第一作者。百迈客生物可提供Illumina二代宏基因组、ONT三代宏基因组、PacBio全长微生物多样性、二代微生物多样性、微生物绝对定量等全套测序分析服务,如果您对我们的服务感兴趣,欢迎点击下方按钮联系我们,我们将免费为您设计文章思路方案。






 京公网安备 11011302003368号
京公网安备 11011302003368号