大量研究表明,肿瘤微环境(TME)的各种免疫细胞类型会影响癌细胞的进展和转移。TME的密度、位置和功能状态,被确定为与预后和免疫治疗反应相关的重要参数。单细胞RNA测序(scRNA-seq)技术加速了对肿瘤内不同细胞群和表型状态的识别,为揭示不同癌症类型的TME差异提供了机会。例如,肝细胞癌(HCC)和结直肠癌(CRC)中CD8+耗竭T细胞(Texs)的比例远高于肺癌。因此,不同的癌症类型具有不同的TME特性,了解TME形成的内在和外在因素至关重要。2022年4月北京大学生命科学学院研究团队在《Cancer Cell》上发表了一篇结直肠癌与肝转移之间TME研究的文章,下面,小编就为您带来这篇文章的解析。
 研究背景
研究背景
本研究对来自肝转移性结直肠癌的样本进行了单细胞分析,以解释了影响TME的因素。通过对不同组织中的CD45+细胞分析,发现M型T细胞表型与恶性肿瘤相关,而N型表型与生态位相关。树突状细胞(DC3s)和SPP1+巨噬细胞的一个亚群也是M型,在肝转移中占优势,表明其具有促转移的作用。本研究将原发性和转移性肿瘤的免疫表型联系起来,从而有助于了解肿瘤特异性。
研究材料
材料:结直肠癌患者17例,其中女性6例,男性11例。患者手术切除来自原发性肿瘤和肝转移的新鲜肿瘤和邻近正常组织样本(距匹配的肿瘤组织至少2 cm)
方法:单细胞转录组测序
研究成果
1、CRLM、HCC和CRC的数据收集和不同的免疫特征
从101个匹配的CRLM样本中分选出CD45+细胞,包括原发性结直肠癌(Pri.CT)、邻近结肠(Adj.Col)、肠系膜淋巴结(MLN)、肝转移(Liv.Mets)、邻近肝脏(Adj.Liv) 和17名初治患者的外周血(图1A),分别获得323,444和5,004个高质量细胞,包括CD4+和CD8+ T细胞、单核细胞、巨噬细胞、自然杀伤T(NKT)细胞、NK细胞、γδ T细胞、DC、肥大细胞、B细胞、3型先天性淋巴细胞(ILC3)和少量 CD45-细胞,此外,共鉴定出78个免疫细胞亚群(图1B和1C)。由于原发性HCC/CRC和CRLM肿瘤同时分析TME 形成过程中的相互作用至关重要,因此本研究结合了来自18名未接受治疗的非转移性CRC患者的49个样本和51个样本的scRNA-seq数据集。
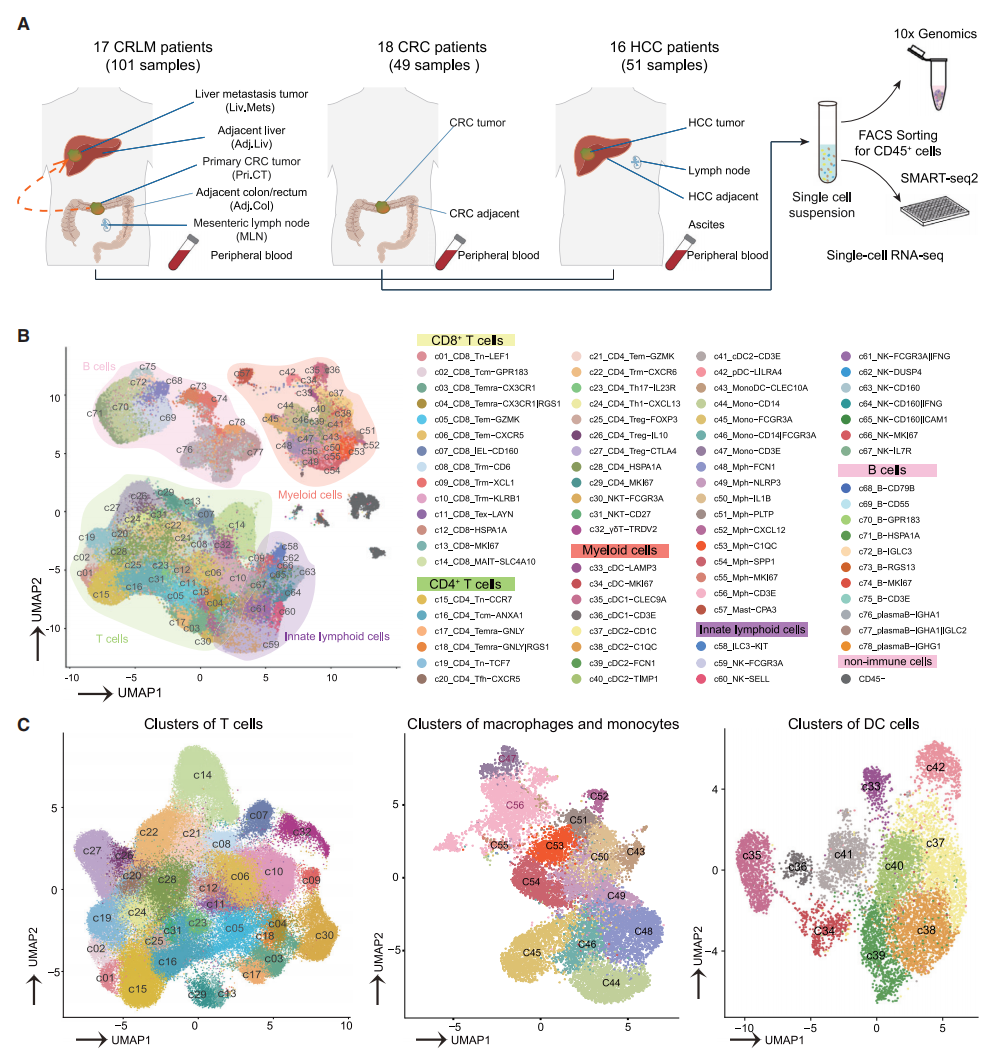
图1 CRLM、HCC和CRC不同的免疫特征
仅对来自原发性HCC/CRC的正常和肿瘤数据进行ANOVA分析,发现 CD4_Treg-CTLA4、CD8_Tex-LAYN和Mph-C1QC是肿瘤相关的前三个簇(p < 0.001,ANOVA检验;图2A),并且在HCC和CRC肿瘤相应的邻近部位(图2B),这表明这些细胞可能受到恶性肿瘤状态的影响。此外,与Adj.Cols和HCC肿瘤相比,Mph-SPP1在CRC肿瘤中富集(图2B)。KLRB1+组织驻留记忆(Trm)CD8+ T和MAIT细胞在HCC肿瘤和Adj.Livs中占优势,而上皮内淋巴细胞(IEL)和Mph-NLRP3在CRC肿瘤和Adj.Cols中表现出更高的丰度(图2A),这表明这些细胞可能受到所在组织的影响。
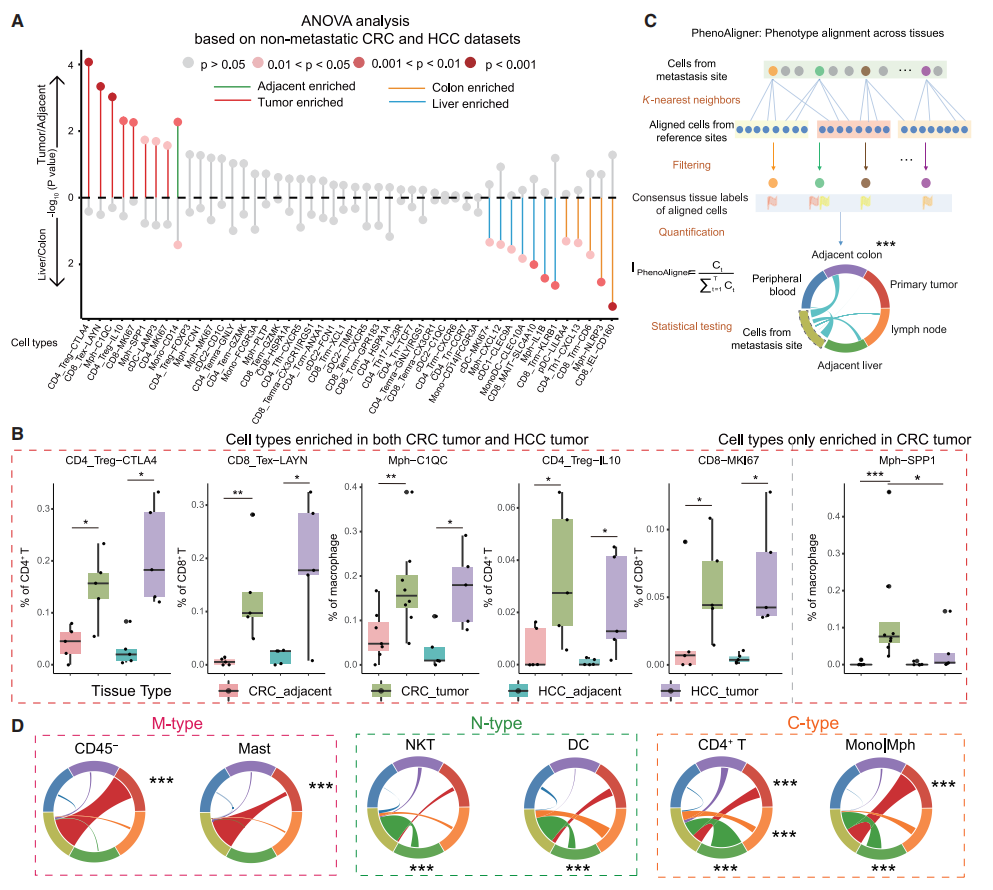
图2 使用表型比对分析癌细胞和宿主器官对TME的影响
2、通过PhenoAligner解开癌细胞和宿主器官对TME的影响
使用来自Pri.CT、Adj.Col、MLN、Adj.Liv和血液的单个细胞作为参考,并将来自 Liv.Mets的每个免疫细胞与参考对齐,以识别其相邻的组织类型(图2C)。对于Liv.Mets中的特定簇,具有高PhenoAligner指数的组织类型可能表明Liv.Mets中的高比例细胞在所识别的组织类型中具有相似的居住位。
在主要免疫区室水平中,PhenoAligner显示Liv.Mets中81% CD45–细胞与Pri.CT中的细胞对齐(r>0.5,Pearson相关性;p<0.05,置换检验)(图2D)。来自原发性肿瘤的肥大细胞被称为“恶性肿瘤相关”(因此称为“M型”);Liv.Mets中的NKT和NK细胞与Adj.Liv的免疫微环境密切相关,但与其他组织无关,被表征为“生态位相关”(因此称为“N型”),同样,DC和γδ T细胞被鉴定为N型;此外,Liv.Mets中的单核细胞和巨噬细胞与Pri.CT和Adj.Liv具有显著联系,其表型被表征为“组合相关”(因此称为“C型”)(图2D)。
3、CD8+ Texs与恶性肿瘤相关
尽管Liv.Mets中的CD8+ T细胞被指定为N型,但基于PhenoAligner分析(图3 A和3B),它们的子集显示出不同的模式。在所有CD8+ T簇中,Tex-LAYN和Tex-MKI67被鉴定为M型(图3A)。Tex-MKI67与Tex-LAYN共享多个T细胞受体(TCR)克隆型和相似的基因表达。因此,Texs主要受恶性细胞的影响。
从10×5′ VDJ数据中获得了TCR信息,以识别Liv.Mets和Pri.CT之间的共享TCR,在Pri.CT和Liv.Mets中分别检测到的172和149种TCR克隆型中,42种在两个肿瘤部位共享(图3C和3E),表明Tex表现出恶性肿瘤排他性并包含可能识别肿瘤抗原的TCR。另外,Pri.CT和Liv.Mets之间共享的Texs TCR克隆型也可以在血液中的效应记忆T细胞(Temras)中检测到,这表明血液中的Temra克隆可能会渗入Pri.CT和Liv.Mets。效应记忆T细胞(Tems)和Texs之间观察到更高程度的TCR共享。RNA速度分析发现Temras和Tems之间的双向流动(图3F)。这些观察表明,Tems表现出高度可塑性和中间性质,Tems的这种中间转变可能是CD8+ T细胞肿瘤浸润过程中的一个重要桥接步骤,并且可以为先前提出的癌症-免疫周期增加新的见解(图 3 G)。
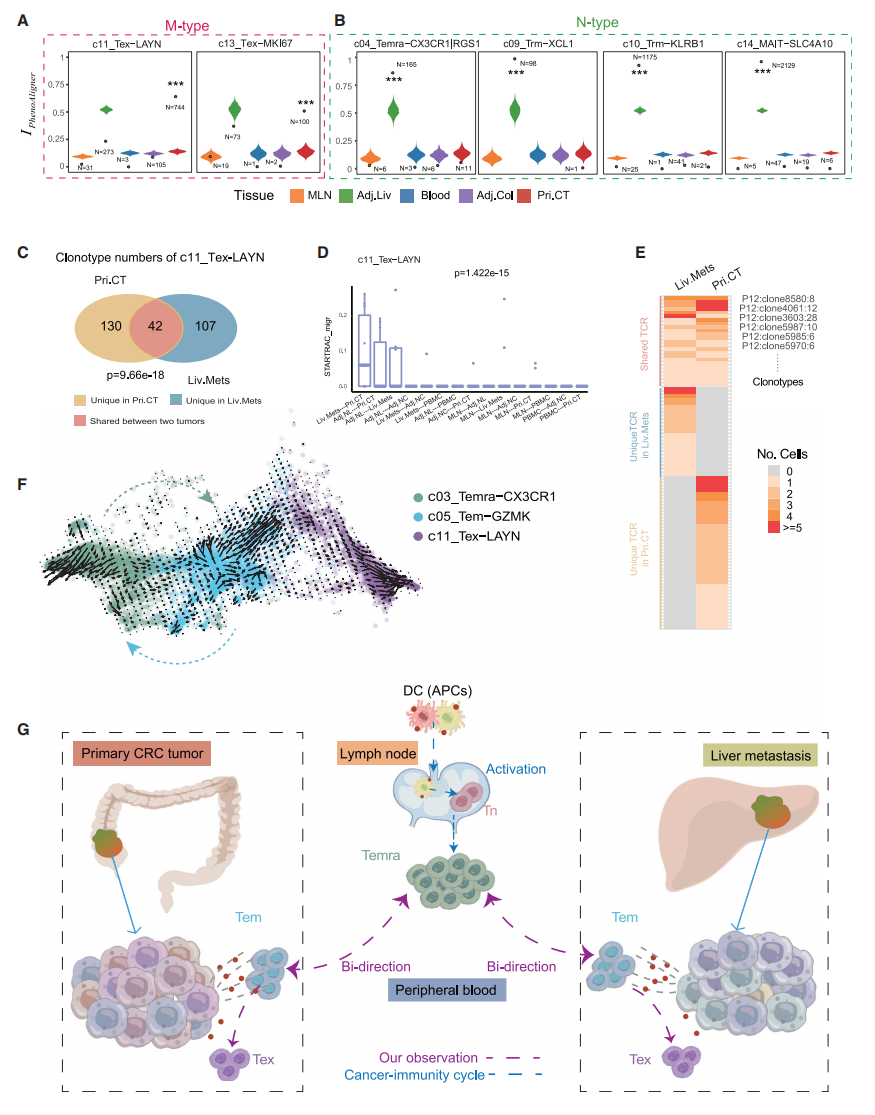
图3 CD8+耗竭T细胞与恶性肿瘤相关且依赖于TCR
4、结直肠恶性肿瘤和肝脏生态位对CD4+ T细胞亚群有不同的影响
对CD4+ T细胞进行了类似的分析,并观察到Th17、Th1、Treg-IL10和Treg-CTLA4被表征为M型(图4A和4B)。在组织富集的Treg群体中,Treg-IL10高度表达肠道常驻Treg标志物,包括IL10、IL23R和IL1R1(图4 C);Treg-CTLA4高表达基因包括LAYN、CCR8和TIGIT(图4C)。此外,与非转移性CRC肿瘤相比,CRLM患者Pri.CT中Treg-IL10和Treg-CTLA4的比例显著增加(图4D),表明与非转移性CRC肿瘤相比,具有Liv.Mets的原发性CRC肿瘤可能表现出更强的免疫抑制生态位。
Treg-CTLA4和Th1细胞中的TCR在Pri.CT和Liv.Mets之间显著共享(图4F和4E)。在所有CD4+ T细胞簇中,只有Treg-CTLA4在Pri.CT和Liv.Mets之间的STARTRAC-migr指数高于肿瘤和其他组织之间的指数(图4H)。此外,RNA速度分析显示从Treg-FOXP3到Treg-CTLA4的转变方向(图4I),表明血液中静止的Tregs可能迁移到两个肿瘤部位,然后在TME中被激活和扩张。Treg-IL10和Th17的TCR在Pri.CT和Liv.Mets之间表现出互斥模式(图4G)。这些观察表明,Liv.Mets中Treg-IL10和Th17的表型可能是由类似于肠道相关环境的组织生态位诱导的。
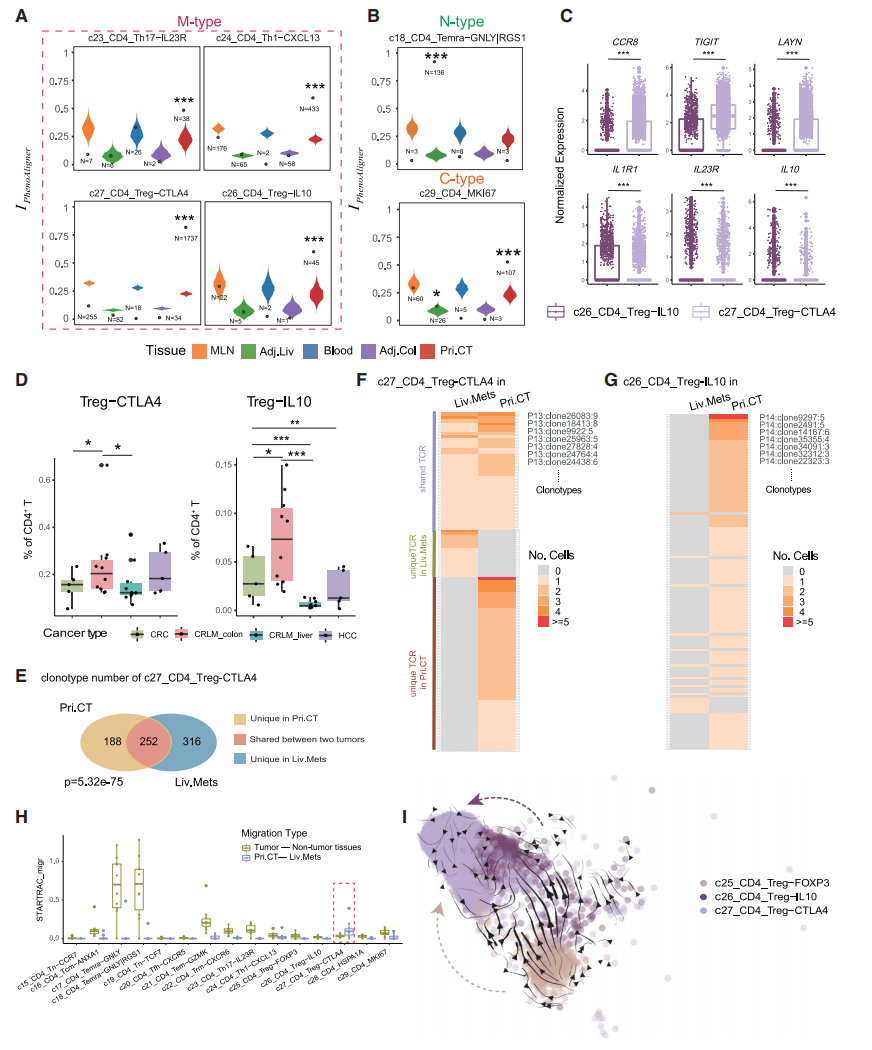
图4 不同生态位对CD4+ T细胞亚群的影响
5、SPP1+ TAMs在Liv.Mets中的作用
对巨噬细胞的异质性进行分析。得到14个亚群,大多数被表征为N型或C型,只有3个TAM簇被表征为M型(图5A)。虽然SPP1+ TAM的表达特征通常存在于非转移性CRC hM13_TAM_SPP1中,但这种特征在非转移性HCC巨噬细胞中基本上不存在(图5B),可SPP1+ TAMs在Liv.Mets中占主导地位(图5C)。使用bulk RNA-seq数据(GEO:GSE14297)证实,SPP1基因在Liv.Mets中高表达(图5D)。IHC也证实了该TAM亚群在 Liv.Mets(图5H)中。
接下来评估了这3个M型TAM亚群的血管生成和吞噬特性。SPP1+ TAMs显示出*高的血管生成评分,而C1QC+ TAMs显示出*高的吞噬作用评分(图5G)。结果证明了SPP1+主要存在于Liv.Mets中以及C1QC+的增殖特征,暗示它们在转移过程中的重要作用。
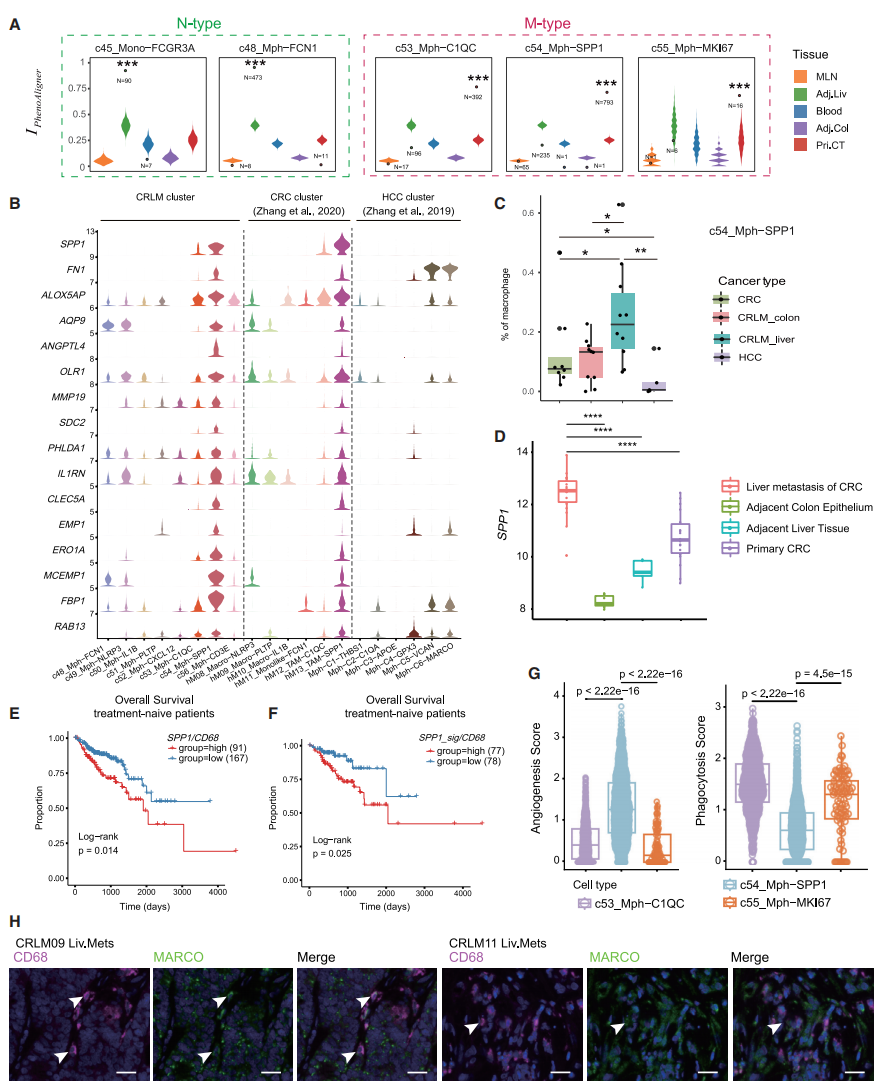
图5 SPP1+肿瘤相关巨噬细胞的作用
6、促炎性DC3在表型上由CRLM中的癌细胞形成
在CRLM患者中鉴定了10个DC亚群,并根据ROGUE指数计算了它们的纯度(图6A)。Liv.mets中的cDC2- C1QC细胞被表征为M型,而Liv.mets中的cDC2-TIMP1细胞被表征为C型,因为它们与Adj.Liv和MLN相关(图6B),这些观察表明这两个cDC2可能在Liv.Mets中具有不同的功能。基于差异表达分析,cDC2-C1QC表现出更高的C1QA、CD68、CD163和CD14表达(图6C和6E)。cDC2-TIMP1高度表达成熟标志物,如CCR7 和血管生成相关基因,包括EREG、CREM和VEGFA(图6D和6E)。
最后,比较了CRLM、HCC和CRC数据集之间DC的差异(图6F)。与Liv.Mets和非转移性CRC肿瘤相比,DC3在CRLM的Pri.CT中显示出更高的频率(图6G)。基于对 TCGA、COAD和READ队列的生存分析,cDC2中DC3的比例与预后不良相关(图6H)。IHC进一步证实了DC3s的存在(图6I和6J)。
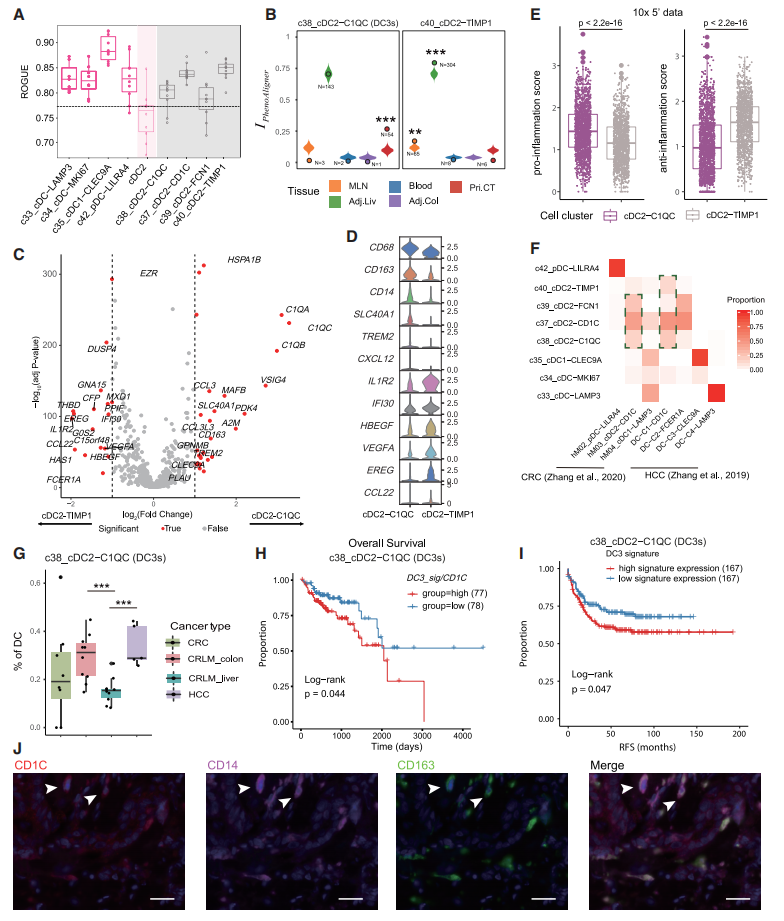
图6 SPP1+肿瘤相关巨噬细胞的作用
研究结论
- 描述了结直肠癌和肝转移的免疫细胞表型
- 恶性肿瘤相关的耗竭和调节性T细胞表现出不同的TCR依赖性
- SPP1+TAMs与恶性肿瘤相关并与肝转移有关
- DCs主要与宿主器官相关
欢迎点击下方按钮联系我们,我们将免费为您设计文章研究思路方案






 京公网安备 11011302003368号
京公网安备 11011302003368号