
研究目的
目前人肝细胞癌(HCC)的治疗策略效果有限,免疫治疗成为治疗该疾病的有效方法。文章从提供人源化小鼠(humice)模型出发,以便了解人类癌症与免疫系统之间的相互作用,特别是针对人类特异性药物的测试。
研究设计
在NOD-scid Il2rg – / – (NSG)小鼠注射人类造血干细胞(HSCs)构建人源化的humice模型,通过植入与I型人白细胞抗原(HLA-I)相匹配的HCC肿瘤组织,建立患者衍生的异种移植肿瘤HCC-PDX。研究肿瘤和免疫应答的纵向变化以及免疫检查点抑制剂的功效。
研究结果
与临床结果类似,我们模型中的人源免疫系统受到肿瘤的刺激,并表现出衰竭表型,如白细胞数量显着下降,衰竭标志物上调以及人类促炎性细胞因子的减少。值得注意的是,与其他细胞类型相比,细胞毒性免疫细胞下降得更快。与外周血T细胞相比,肿瘤浸润的T细胞具有更高的衰竭标志物表达和更低的细胞因子产生。此外,发现肿瘤相关巨噬细胞和骨髓衍生抑制细胞在肿瘤微环境中高度富集。有趣的是,肿瘤在免疫应答过程中通过上调免疫检查点配体来改变基因表达谱。最重要的是,与NSG模型相反,文章中的模型显示了免疫检查点抑制剂pembrolizumab和ipilimumab的疗效和副作用。
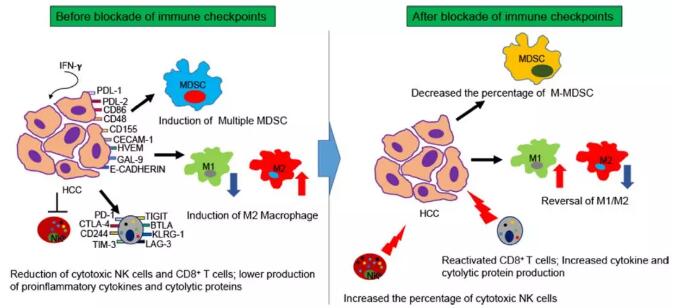
参考文献:Development of a new patient-derived xenograft humanised mouse model to study human-specific tumour microenvironment and immunotherapy. Gut. 2018 Mar 30.
最近文章






 京公网安备 11011302003368号
京公网安备 11011302003368号