2025年12月20日,中国农业科学院饲料研究所周志刚团队在iMeta在线发表研究论文,题为“Host-driven hepatic conversion of gut microbiota-derived putrescine to spermidine mediates mannose’s protective effects against hepatic steatosis in zebrafish”。

该研究揭示甘露糖富集的Cetobacterium somerae能将日粮中的精氨酸在肠道内转化为腐胺,并由肝脏进一步代谢为亚精胺,从而发挥减轻高脂日粮诱导的肝脂蓄积的作用,这一发现不仅阐明了肠道微生物与宿主之间跨界协同产生有益代谢物的全新机制,也为理解肠肝轴在代谢健康中的作用提供了突破性视角。百迈客生物为该研究提供了全长微生物多样性测序服务。
研究背景
最新研究发现肠-肝轴涉及两个器官间的相互作用,能通过多种微生物代谢物实现的双向交流,表明肠道来源的细菌代谢物可能对肝脏健康产生正向或负向影响。为探究肠-肝相互作用,高脂饮食(HFD)模型是最成熟的实验方法之一,肠道、微生物群与宿主肝脏之间的这种特殊相互作用表明肠道微生物可能产生许多尚未表征的代谢物,这些代谢物可循环至肝脏以影响肝功能。然而,迄今为止尚未发现任何肠道微生物代谢物经肝脏代谢后转化为有益于肝脏健康的成分。
研究结果
甘露糖补充缓解斑马鱼高脂饮食诱导的脂肪肝
因为已有报道表明甘露糖可改变肠道菌群组成并缓解小鼠脂肪肝,为了确定通过甘露糖富集或选择肠道菌群是否能改善肝功能,进行了添加甘露糖的HFD喂养实验。喂养试验后, HFD组斑马鱼的体重增长和肝脏三酰甘油(TAG)含量较正常脂肪饮食(NFD)组显著增加,表明成功建立了营养性脂肪肝模型。与HFD组相比,NFD、5M(5 g/kg)和10M(10 g/kg)组通过降低肝脏脂合成相关基因的表达,肝脏TAG含量显著降低,血清丙氨酸氨基转移酶(ALT)和天冬氨酸氨基转移酶(AST)水平显著下降。H&E染色显示,相比HFD组,5M和10M组肝脏的空泡数量和损伤评分明显减少。5M和10M组肝脏促炎因子相关基因的表达也有所降低,总体而言,还观察到HFD添加甘露糖后在形态学和分子水平上改善了斑马鱼的肠道健康。
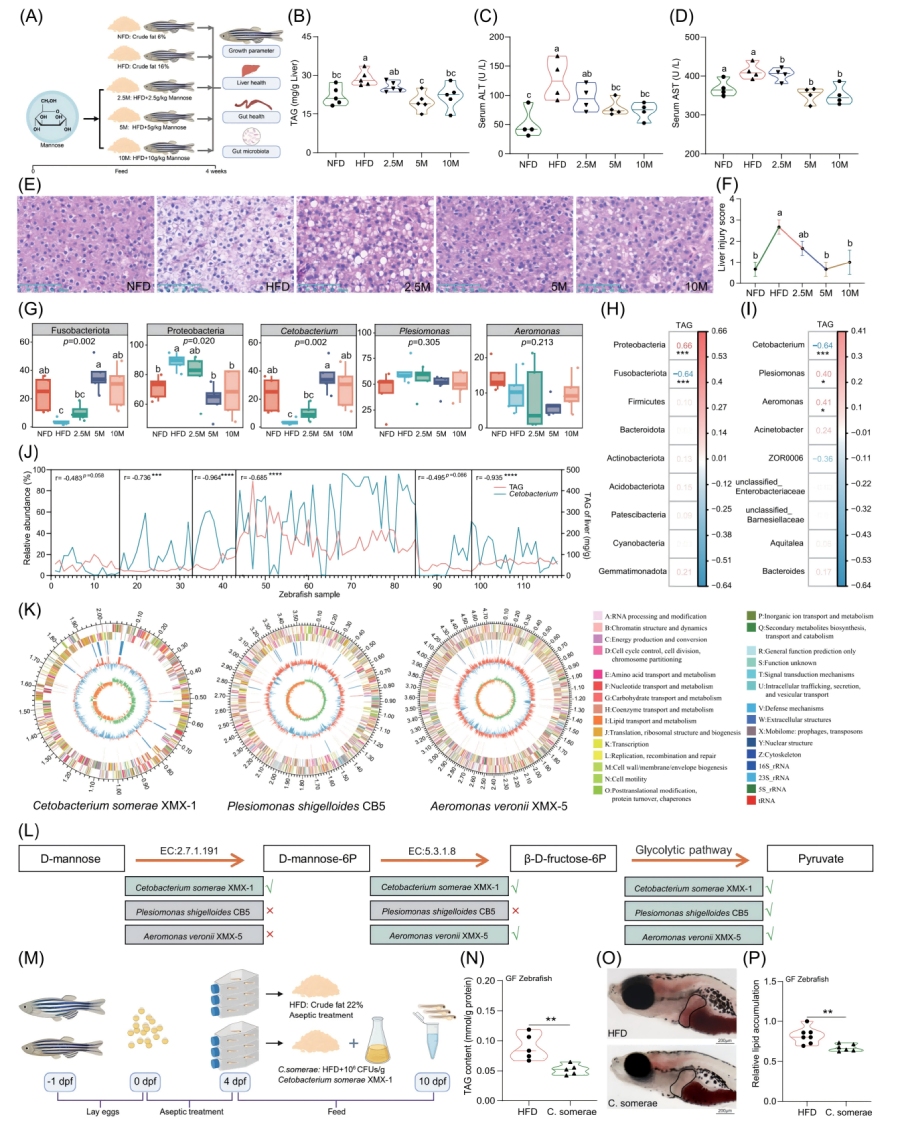
图1-甘露糖补充不能直接缓解HFD诱导的肝脏脂肪变性,但会促进C.somerae的生长
甘露糖补充改变肠道微生物群并选择性富集CETOBACTERIUM
与HFD组相比,5M组和10M组中变形菌门(Proteobacteria)的相对丰度显著降低,而梭杆菌门(Fusobacteriota)的相对丰度显著增加。与HFD组相比,5M组和10M组中梭杆菌属(Cetobacterium)的相对丰度显著增加。肠道微生物群的α多样性指数(Chao1和Shannon)在各组间无显著差异。LEfSe分析显示,5M组斑马鱼肠道中梭杆菌属(Cetobacterium)高度富集。梭杆菌属(Cetobacterium)是梭杆菌门(Fusobacteriota)的一个属,在鱼类中仅由单一物种C. somerae代表,该菌通常栖息于多种鱼类的肠道中。
此外,PCoA显示HFD组和5M组的肠道微生物群完全分离,表明甘露糖补充显著改变了斑马鱼的肠道微生物群组成。Spearman相关性分析显示,变形菌门及其包含的近缘单胞菌属(Plesiomonas)和气单胞菌属(Aeromonas)的相对丰度与TAG含量呈显著正相关,而梭杆菌门(Fusobacteriota)和梭杆菌属(Cetobacterium)的相对丰度与肝脏甘油三酯含量呈显著负相关。为了进一步验证Cetobacterium、Plesiomonas和Aeromonas的丰度与肝脏TAG含量的关系,收集了斑马鱼和鲤鱼的公共数据集。Spearman相关分析显示,Cetobacterium与肝脏TAG含量呈一致的显著负相关,而Plesiomonas和Aeromonas则没有。
对C. SOMERAE的基因组与生长分析揭示其代谢甘露糖的能力
为探究甘露糖补充后肠道中这些不同细菌类群丰度变化的原因,该团队对斑马鱼肠道中选定的菌株进行了全基因组测序分析,包括C. somerae XMX-1, Plesiomonas shigelloides CB5 和Aeromonas veronii XMX-5。结果证实这些菌株存在显著的功能差异。
首先,三种菌株的基因组结构存在明显差异。由于甘露糖喂养的斑马鱼肠道中Cetobacterium相对丰度较高,进一步比较了这三种细菌对单糖代谢途径的差异。结果显示,只有C.somerae具有代谢甘露糖的能力,进一步的生长实验证实C.somerae可利用甘露糖作为其生长的主要碳源。相比之下,当甘露糖作为主要碳源时,P.shigelloides CB5和A.veronii XMX -5均未观察到生长。
肠道C. SOMERAE可减少斑马鱼肝脏脂肪蓄积
为明确甘露糖或C. somerae是否能减少肝脏脂肪积累,研究了甘露糖对无菌(GF)斑马鱼肝脏脂肪积累的直接影响。结果证实,补充甘露糖的饮食并未减少肝脏脂肪积累,且与脂质代谢和炎症因子相关的基因表达未出现显著变化。
然而,甘露糖改善的肠道菌群可减少斑马鱼肝脏脂肪积累。随后,为直接验证C. somerae补充对降低肝脏脂质积累的影响,在喂食HFD的GF斑马鱼幼体中添加了浓度为106 CFUs/g的C. somerae。与HFD组相比,补充C. somerae的组别肝脏TAG含量和油红染色显著降低。C. somerae对宿主的保护作用已在脂质代谢和炎症相关基因中得到证实。
此外,团队评估了P. shigelloides CB5或A. veronii XMX-5对肝脏降脂效果,证实这些菌株不影响斑马鱼肝脏脂肪含量。最后,发现C. somerae可改善斑马鱼肝脏脂肪积累和肠道健康。
代谢组与基因组分析揭示了C. SOMERAE中精氨酸-腐胺通路的存在
为探究C. somerae可HFD下改善宿主肝脏健康的机制,结合基因组学和代谢组学分析以及同位素示踪方法,来确定C. somerae参与降低肝脏脂肪含量的活性成分。代谢组分析显示,无菌培养基和C. somerae上清液中的代谢物显著分离,且组内差异性较低。差异代谢物分析表明,腐胺是C. somerae上清液中最丰富的代谢物之一。随后团队基于C. somerae的基因组序列注释了腐胺代谢途径中的主要酶,并发现C. somerae拥有编码精氨酸脱羧酶的基因,以及胍丁胺脱亚胺酶和N-氨甲酰腐胺酰胺酶的基因,从而从胍基丁胺中产生腐胺,这与其他细菌的研究结果一致。
此外,C. somerae的全谱代谢组分析显示,该细菌可利用精氨酸产生胍基丁胺并进一步产生腐胺。进一步的靶向代谢组分析表明,精氨酸在48小时被C. somerae完全利用,腐胺含量达到2.22 μmol/mL。为验证该代谢途径在C. somerae中的存在,我们在培养基中添加了外源性同位素标记的13C6 15N4-精氨酸。结果显示,C. somerae的上清液和细菌沉淀中均检测到13C4 15N2-腐胺。最后,通过向培养基中补充D8-腐胺,验证C. somerae是否能进一步代谢腐胺生成亚精胺。结果表明,C. somerae的上清液和细菌沉淀中均检测到D8-腐胺,但未发现标记的亚精胺。综合分析表明,C. somerae可通过精氨酸代谢途径产生腐胺,该代谢物可能具有降低肝脏脂质的潜在作用。
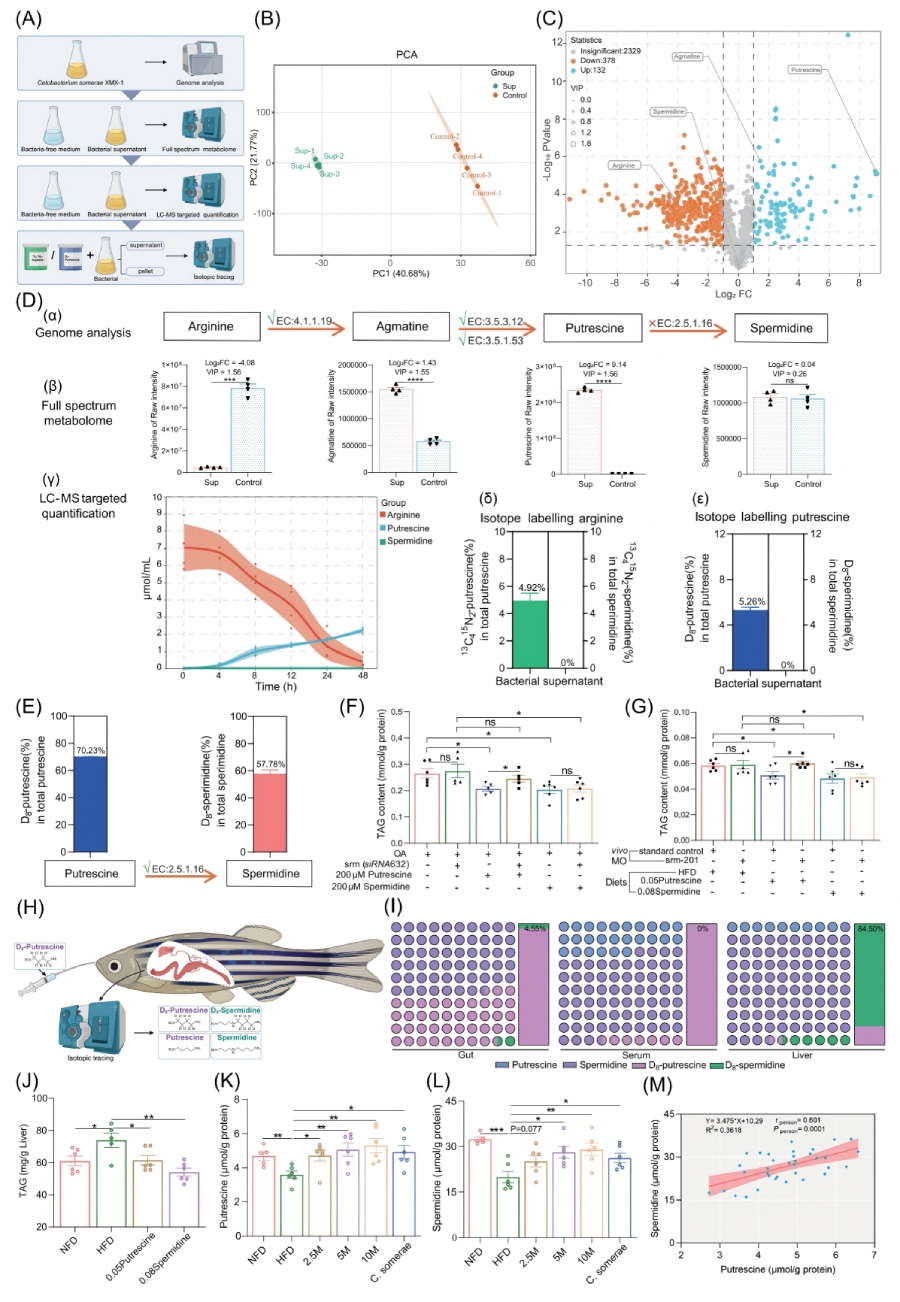
图2-亚精胺是改善HFD诱导性肝脂肪变性的效应分子
腐胺对肝功能无直接影响,但其下游宿主代谢产物精脒可缓解脂肪肝病理改
亚精胺作为腐胺的下游代谢产物,已被证实可缓解肝脏脂肪变性,但未在C.somerae基因组中发现亚精胺合成酶(srm)基因,且在细菌上清液中也未检测到该酶。此外,在C.somerae培养物的任何组分中均未检测到13C415N2-亚精胺到D8-亚精胺。检测了斑马鱼基因组,发现其确实存在可将腐胺代谢为亚精胺的亚精胺合成酶(EC:2.5.1.16)基因。采用斑马鱼肝脏(ZFL)细胞模型进行的同位素示踪实验显示, ZFL 细胞中检测到总亚精胺中有57.78%为D8-亚精胺,表明 ZFL 细胞能够将D8-腐胺代谢D8-亚精胺。
随后研究团队通过ZFL的HFD模型验证腐胺和亚精胺是否会影响肝脏脂质代谢。与对照组相比,腐胺和亚精胺处理的 ZFL 细胞内细胞内甘油三酯含量显著降低。为验证亚精胺对肝功能的影响,在ZFL细胞和斑马鱼幼体中敲低了亚精胺合成酶。沉默亚精胺合成酶后,腐胺处理组的降脂效果消失,而亚精胺处理组仍保持该效应。
HFD斑马鱼中腐胺-亚精胺交叉对话的发现
为验证肠道微生物产生的腐胺是否可转运至肝脏作为亚精胺合成的前体,体内同位素示踪实验显示:肠道中的D8-腐胺可通过血液转运至肝脏,且肝脏可将84.50%的D8-腐胺代谢为D8-亚精胺,肝脏中亚精胺含量显著高于腐胺。通过斑马鱼HFD模型进一步验证了腐胺与亚精胺的降脂作用:与HFD组相比,腐胺和亚精胺处理组的肝脏甘油三酯含量均显著降低;两组肝脏中腐胺与亚精胺水平均恢复至正常水平。补充甘露糖和C. somerae的实验组亦证实此结果,表明肝脏是腐胺转化为亚精胺的主要代谢场所。
研究总结
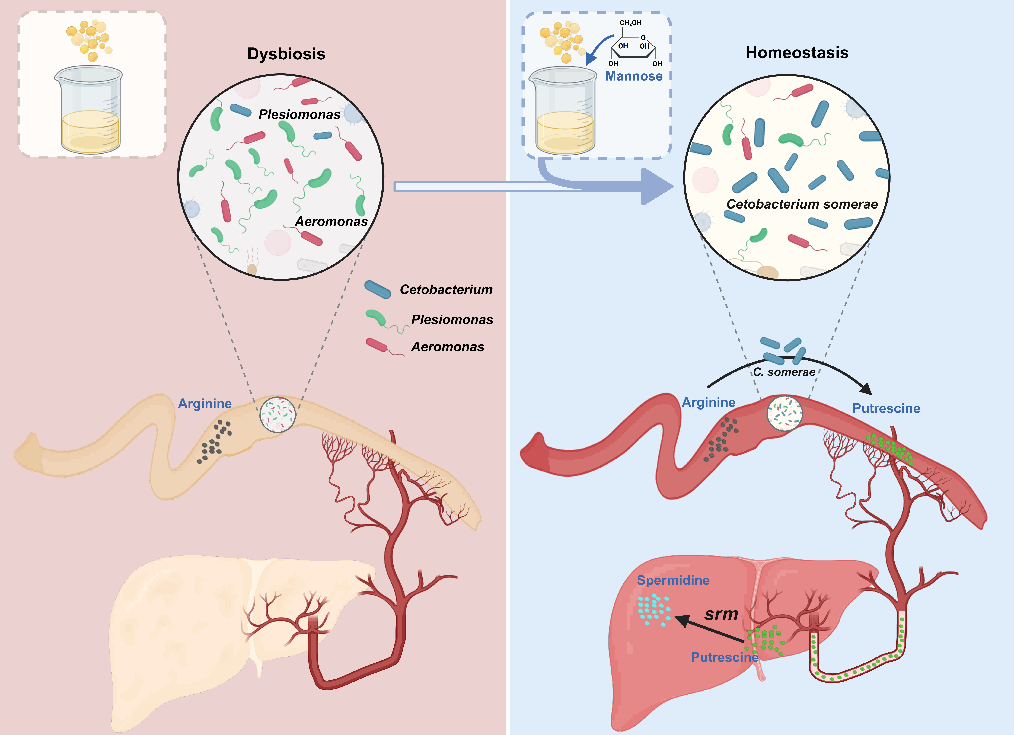
该研究发现了一种涉及精氨酸-腐胺-亚精胺级联代谢途径的新机制,该机制通过肠道C. somerae与宿主肝脏的协同作用改善肝脏脂肪变性。关于肠道-肝脏轴中微生物-宿主代谢相互作用产生有用代谢物亚精胺的新发现,提出了肠道-肝脏轴中宿主-微生物交叉对话的新概念。






 京公网安备 11011302003368号
京公网安备 11011302003368号