英文题目:Long-read sequencing reveals the complex splicing profile of the psychiatric risk gene CACNA1C in human brain
发表杂志:Mol. Psychiatry,2020年1月
影响因子:11.973
研究背景
在人脑中,与精神分裂症相关的基因组区域富集了在神经发育过程中表现出不同异构体使用的基因,RNA剪接是将遗传变异与精神疾病联系起来的关键机制。剪接图谱在大脑中特别多样,很难准确识别和量化。短读长RNA-Seq方法不能准确地重建和定量大多数转录物和蛋白质异构体,为解决这一挑战,本文将long-range PCR和nanopore全长转录组测序与一种新的生信分析流程结合。
CACNA1C是一种精神危险基因,编码电压门控钙通道CaV1.2,CACNA1C基因很大而且很复杂,至少有50个注释外显子和31个预测的转录本。它的大小和复杂性使得用标准的基因表达方法准确鉴定和量化转录本变得极其困难,本文在人脑中鉴定了CACNA1C的全长编码转录本,识别了38个新的外显子和241个新的转录本,对异构体多样性的详细了解对于将精神病学基因组发现转化为病理生理学见解和新的精神药理靶点至关重要。
研究方法
样本:来自利伯脑发育研究所储存库的三名成年捐赠者的尸检脑组织(提取小脑、纹状体、背外侧前额叶皮质、扣带回、枕叶和顶叶皮质的RNA,并进行逆转录)
测序方法:使用PCR扩增CACNA1C全长CDS,使用MinION进行测序
分析流程:https://github.com/twrze/TAQLoRe
研究结果
1、CACNA1C有很多外显子和异构体
由于CACNA1C的复杂性,本文使用了两种互补的方法来鉴定转录本:外显子水平和剪接位点水平的分析,分析流程见补充图2。该方法共鉴定了251种存在于人脑中独特的CACNA1C转录异构体,其中241种是新的,包括使用新的外显子,新的剪接位点和连接。
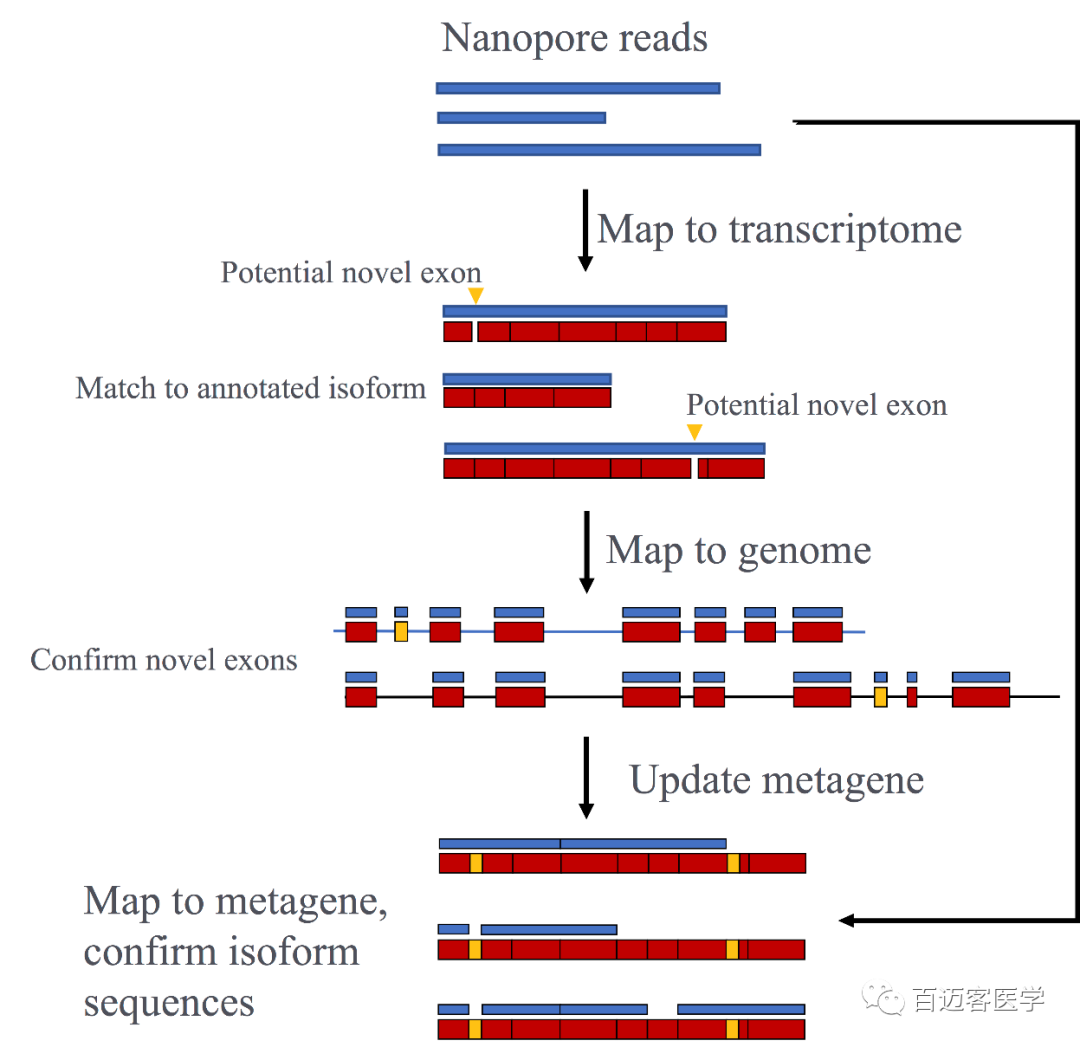
补充图2
在CACNA1C基因座内总共注释了39个潜在的新外显子,其中38个在至少2个人或组织中被识别,并在每个文库中得到至少5条nanopore reads的支持(图2A)。通过PCR和Sanger测序确认了新的外显子与其周围的注释外显子之间的剪接连接,从而验证了四个新的外显子。这种新的外显子的成功验证提供了很高的可信度,即通过纳米孔测序鉴定的新的外显子是真实的,并且被整合到CACNA1C转录本中。表达量最高的10条转录本中,有9条是新的且其中有8条被预测保持CACNA1C阅读框架,这表明这些最丰富的新转录本中有一些编码功能不同的蛋白质异构体(图2B,C)。这些结果表明,新的CACNA1C转录本表达丰富,数量也很多,目前的注释缺少许多最丰富的CACNA1C转录本。
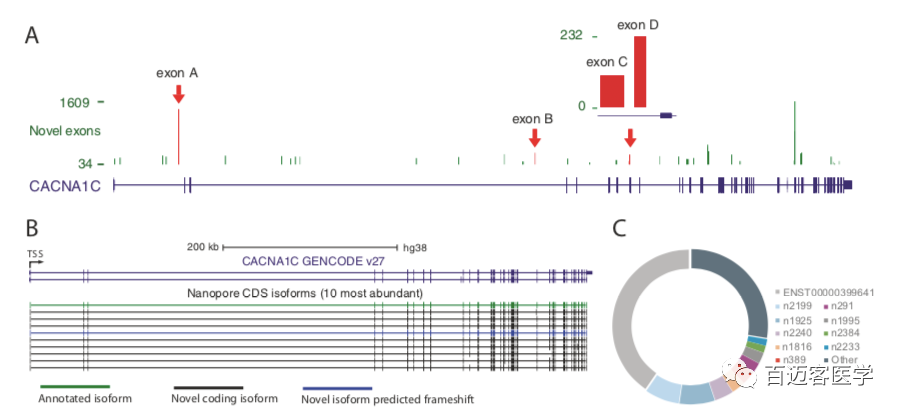
图2
通过设置转录本的高置信度,在6个大脑区域确定了90个高可信的CACNA1C转录本,包括7个先前注释的(GENCODE V27)和83个新的(补充图3)。7个新的高置信度转录本包含新的外显子,而其余76个包含以前未描述的连接和连接组合。
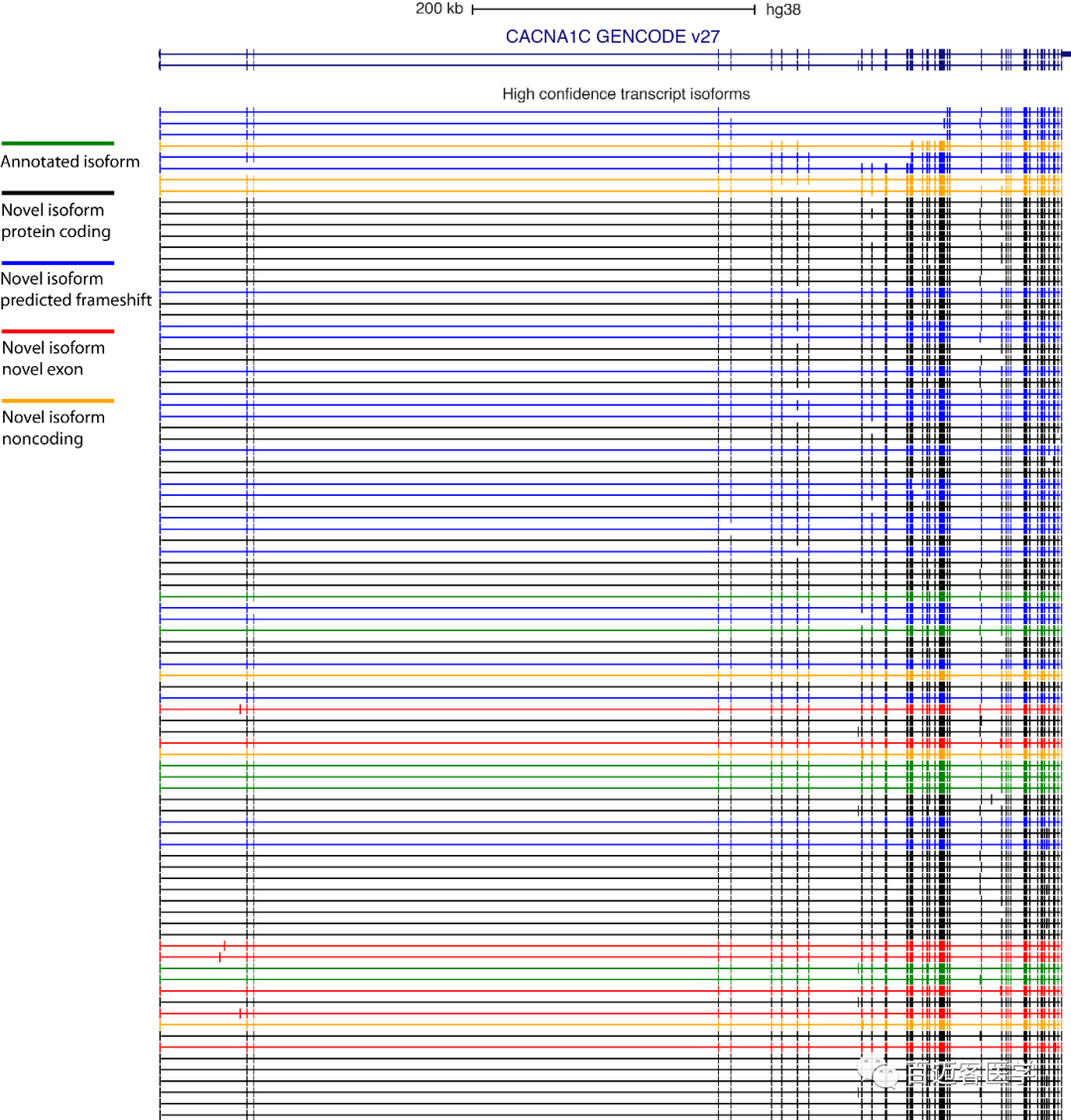
补充图3
上述外显子水平的转录本鉴定方法为鉴定新的外显子和表征全长转录本结构提供了稳健和保守的手段。使用了更为保守的依赖于连接处无错误映射所支持的连接的识别,以及规范剪接位点的方法,确定了497个新的剪接位点,其中393个由至少10条reads支持,这些剪接位点,在筛选了至少24条reads支持的转录本后,鉴定了195个转录本,其中111个被预测为编码的。
2、CACNA1C亚型在不同脑区的表达谱不同
小脑、纹状体与皮质等组织观察到了CACNA1C转录本差异,但在不同个体之间的表达是相似的。在小脑中观察到了明显的转录本表达转换;在小脑之外,ENST00000399641是主要的转录本,而在小脑中,ENST00000399641和CACNA1C n2199的表达水平相似。
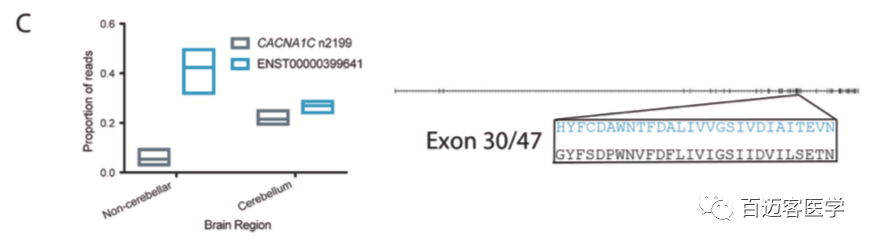
图3 C
3、预测新isoforms对CaV1.2蛋白模型的影响
CACNA1C编码CaV1.2 的主要成孔亚基。钙孔由24个跨膜重复序列组成,由细胞内环连接成4个结构域(I-IV)(图4A)。在我们鉴定的83个新的外显子水平的转录本中,51个可能编码功能性的CaV1.2通道。灰色方框表示新的、框架内的插入和删除的位置(值表示包含每个isoforms的reads的平均比例)。使用两种分析方法(外显子水平和剪切连接水平)鉴定变体的情况,外显子水平计数用于得出丰度(红色文本);仅使用剪接位点水平方法鉴定的变体用蓝色文本表示。包含三个微缺失的蛋白质异构体的数量:(I)在I-II接头中,(Ii)在IV4-5接头中,以及(Iii)在IV3-4接头中先前报道的微缺失(图4B)。
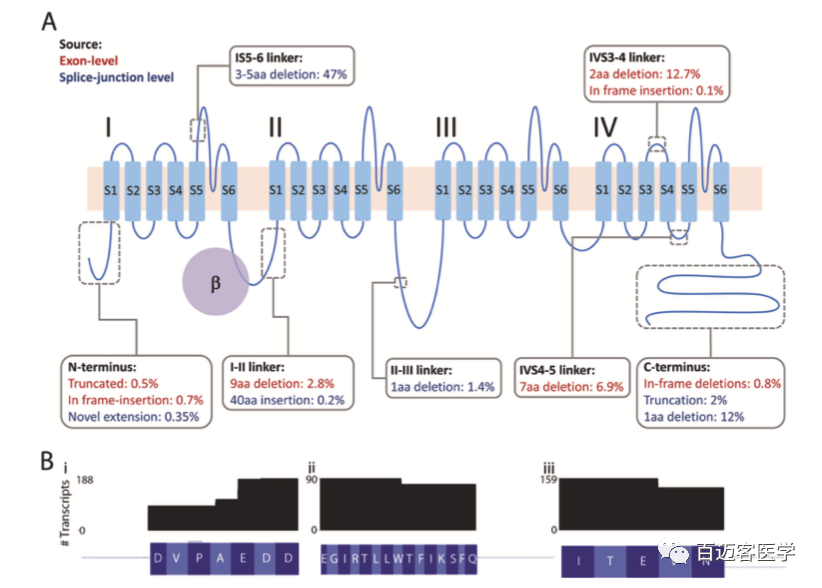
图4
总结
长读长测序技术的快速发展为准确获得转录多样性提供了可能,因为每一条read都包含一个完整的转录本。这对于具有复杂模型的基因尤其重要。由于CACNA1C剪接产生的CaV1.2蛋白对现有的钙通道阻滞剂表现出不同的敏感性,因此有可能选择性地针对疾病相关的CACNA1C亚型和/或那些在大脑与外周差异表达的CACNA1C亚型,提供既更有效又更无外周副作用的新型精神药物。综上,这些观察结果证明了ONT长读长测序对于准确描述转录本结构和选择性剪接的重要性。
参考文献:
Clark Michael B,Wrzesinski Tomasz,Garcia Aintzane B et al. Long-read sequencing reveals the complex splicing profile of the psychiatric risk gene CACNA1C in human brain.[J] .Mol. Psychiatry, 2020, 25: 37-47.






 京公网安备 11011302003368号
京公网安备 11011302003368号