组织送样量要求
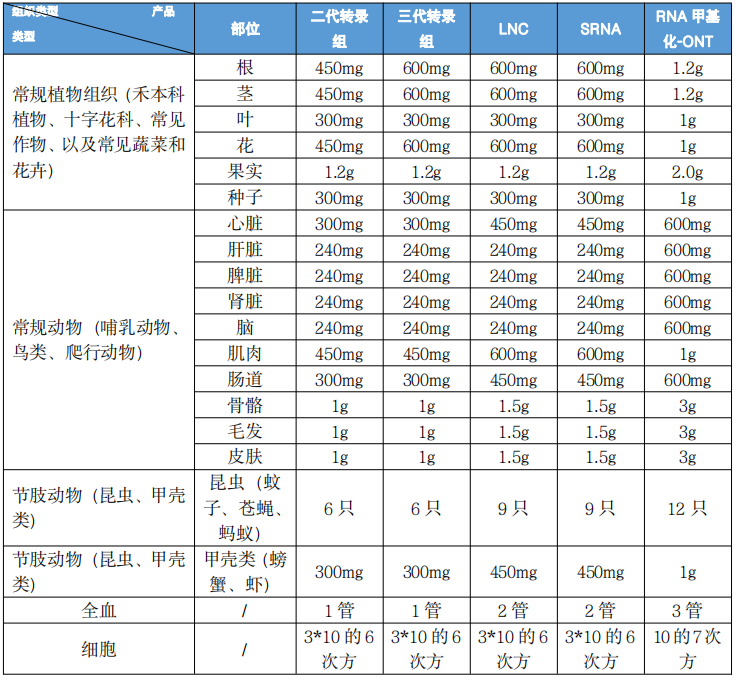
核酸送样量要求
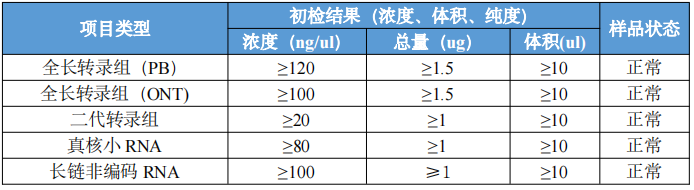
注:如果您开展的实验项目为 miRNA 的相关实验,并且提供的是总 RNA 的样本,请务必确认您采用的总 RNA 的提取方法保留了小 RNA(包括 miRNA)
样品制备保存指南
细胞
1.贴壁细胞
一次 RNA 提取反应所需细胞数≤1 X 10^7 个,以 3 X 10^6-1 X 10^7 个为宜,可以将细胞经裂解液裂解后冻存运输。
- 从培养箱中取出贴壁培养的细胞,显微镜下观察细胞,确定生长状态良好(正常细胞融合度在 80 %左右);
- 弃去培养基,向细胞培养瓶或培养皿中加入 5 mL PBS(RNase free,室温), 清洗一次;
- 弃尽 PBS,加入适量细胞裂解液,反复吸打数次;直至看不见成团的细胞块,使之充分溶解于裂解液中形成清亮不粘稠的液体;
- 将裂解好的细胞转移至 1.5 mL 旋盖尖底离心管(RNase free)中,置于-80 ℃或液氮中长期保存;
运输方式:干冰运输。
*注:判断裂解液加入量是否合适的标准可以根据细胞溶解物的黏度来判断。在细胞刚溶解时,可以发现有丝状物出现,若裂解液加入量合适,吹打几次后,丝状物会消失,液体黏稠性下降;若裂解液的量过少,丝状物往往一直存在,液体黏稠性大,应继续补加裂解液。裂解液加入量过少,会导致抽提的 RNA 降解。
TRIzol 裂解法:
离心收集的细胞迅速溶于 TRIzol 裂解,参考用量为每 5 X 10^6 个细胞加 1 mL TRIzol;细胞溶于 TRIzol 后,如出现成团,需用吸头将细胞团吹打散,或者激烈震荡混匀,使细胞完全溶于 TRIzol 中充分裂解,室温静置 5min,之后转移至-80℃低温保存,送样时选择干冰运输寄送。
液氮速冻法:
离心收集的细胞直接液氮速冻,速冻 2h 后转移至-80℃低温保存,送样时选择干冰运输寄送。
2.悬浮细胞
一次 RNA 提取反应所需细胞数≤1 X 10^7 个,以 3 X 10^6-1 X 10^7 个为宜,可以将细胞经裂解液裂解后冻存运输。
- 确定细胞生长状态良好;离心得到细胞沉淀(依据客户实验室细胞离心步骤,注意细胞离心要适度,不要使细胞离心过实而造成裂解液不能充分渗透,4 度离心机,转速 3000g
为宜);
- 弃去培养基,加入 1 mlLPBS(RNase free,室温),轻轻将细胞沉淀悬起, 转移至 2mL 旋盖尖底离心管(RNase free)中;
- 离心(依据客户实验室细胞离心步骤,注意细胞离心要适度,不要使细胞离心过实而造成裂解液不能充分渗透,4 度离心机,转速 3000g 为宜)得到细胞沉淀,弃去 PBS,液氮速冻 2h 之后转移至-80℃低温保存,送样时选择干冰运输寄送。
运输方式:干冰运输。
TRIzol 裂解法:
离心收集的细胞迅速溶于 TRIzol 裂解,参考用量为每 5 X 10^6 个细胞加 1 mL TRIzol;细胞溶于 TRIzol 后,如出现成团,需用吸头将细胞团吹打散,或者激烈震荡混匀,使细胞完全溶于 TRIzol 中充分裂解,室温静置 5min,之后转移至-80℃低温保存,送样时选择干冰运输寄送。
全血
1.PAXgene 血液 RNA 管:
用于从 PAXgene Blood RNA Tube 中收集的 2.5 ml 人全血中纯化总 RNA。该过程很简单,可以使用手动或自动程序进行。PAXgene Blood RNA Tubes 含有基于 RNA 稳定技术的试剂组合物。该试剂组合物最大程度的保护 RNA 分子降低被 RNase 的降解,并使基因表达的离体变化最小化。如果 PAXgene 血液 RNA 管为唯一的抽血管,则将血液抽入 PAXgene 血液 RNA 管之前应先抽血入“废弃管”内,使抽血过程中所用的采血器内能被预灌注;否则PAXgene 血液 RNA 管应为抽血程序中的最后一只试管。确保血液已停止流入试管再从持针器上取下试管(PAXgene 血液 RNA 管内的负压设计可向管内抽 2.5ml 的血)采血后,立即轻轻颠倒 PAXgene 血液 RNA 管 8-10 次,使添加剂和血液充分混合均匀。

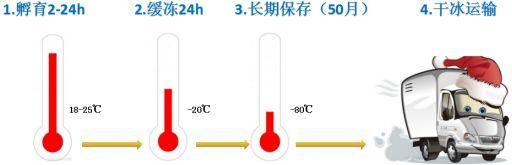
将 PAXgene 血液 RNA 管竖直置于室温(18-25℃)静置 2-24 小时,之后可贮藏于-20℃或更低温度;若试管要贮藏于低于-20℃的温度,先在-20℃冷冻 24 小时,然后再将其转移到-70℃或-80℃,可保存至少 50 个月。大体积干冰运输。
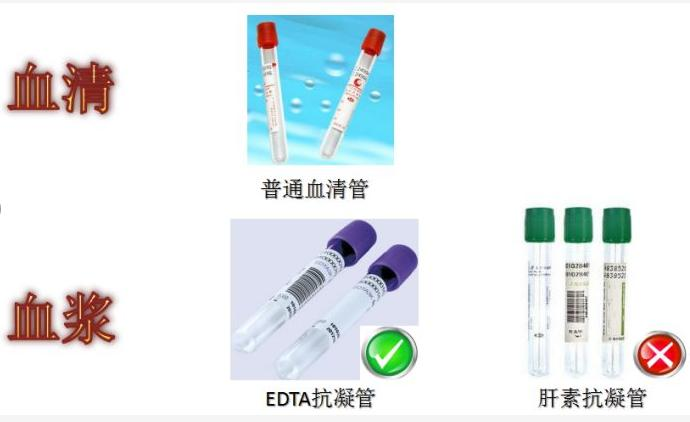
2.EDTA 管采集
要求为全血样本,使用 EDTA 抗凝的采血管采集样品(由于会影响后续建库实验,禁止使用肝素抗凝),采集血液时,必须经过抗凝,避免出现凝结成块。新鲜采集好的抗凝血液,用移液器转移到 2mL 离心管中,液氮速冻 2h,干冰寄送。注意:由于 EDTA 抗凝采血管大多为玻璃易碎材质,切勿使用采血管原管寄送,以防采血管在运输转移途中破裂,造成样品污染、损失。(使用抗凝管采集好的抗凝血液用移液器吸取 500ul 转移到 2mL 离心管中加入 1000ulTRIzol,振荡仪振荡 30-60s,室温孵育 5min 后转到-80 冰箱保存),每个样本建议送两管。
动物组织(不含水产类、昆虫类)
1.液氮速冻法详细流程:
1)提前准备好冷冻组织的足量液氮,预装样品的冻存管,并在做好标记(尽量不使用汉字命名,命名字符控制在 5 个以内)
2)活体取下新鲜组织,立即剔除结缔组织等非研究所需的组织类型。对肿瘤组织的取材,应尽可能准确地判定肿瘤和正常组织,肿瘤组织应将周围的正常组织切除干净(正常组织也应将周围的肿瘤组织切除干净),肠道组织一定要把内容物清洗干净;
3)迅速用预冷的 PBS 溶液(RNase free)或 0.9%生理盐水将组织表面的残留血液冲洗干净
4)如果组织体积较大,将组织切成长宽高均≤0.5 mm 的小块(即黄豆大小)
5)将冻处理好的组织样本混合均匀后保存于 2 mL 或更大体积的螺口冻存管(RNase free)中,标注编号
5)立即(20s 内)置于液氮中冷冻 3~4 h,然后转移至-80 °C 长期保存
6)干冰运输
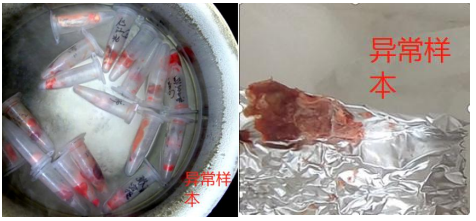
2.TRIzol 法:
1) 如果使用 TRIzol 裂解液保存送样,请务必先进行液氮研磨破碎,样品量取参考标准送样量的 1/3,然后溶于 TRIzol 中,组织样品切勿过量;
2) 震荡混匀,常温裂解 5 min 后,使用低温离心机 12000g 离心 10min,将上清液转至新的 2.0ml 离心管中(拍质控照片,方便核查),转移至-80℃低温保存,运输时选择干冰寄送。

3.RNAlater® Tissue Collection 保护液法:
1、用 RNAlater® Solution 保存组织之前,需要将组织切割成长宽高均≤ 0.5 mm 的小块。
2、如果组织带血液或其他体液,需要过夜后更换一次 RNAlater® Solution;不要将刚浸入RNAlater Solution 中的样本立即冷冻,需将样本置于 4 °C 保存过夜(使 Solution 充分浸润组织样本),然后转移至-20 °C 或-80 °C 长期保存;
3、RNAlater® Solution 不会影响组织结构,可以把已保存的组织从 RNAlater® Solution 中取出,切下实验所需的用量,把剩余的组织再放入到原来的保存液中继续保存;
4、保存于 RNAlater® Solution 中样本,-20 °C 存放时,样本不会结冻,但可能会有晶体析出,这并不影响后续的 RNA 提取工作;-80 °C 存放时,样本会结冻, 在进行 RNA 提取前,需置于冰上融化再进行后续操作,解冻后的样本可再次放入-80 °C 保存;
5、一般来讲,生物样本保存于 RNAlater® Solution 中,37 °C 可存放 1 天,25 °C(室温)可存放 1 周,4 °C 可存放 1 个月,-20 °C 或-80 °C 可长期保存。但鉴于生物样本的特殊性及实验可重复性,建议所有保存于 RNAlater® Solution 中样本,都要置于-20 °C 或-80 °C 长期保存。
植物组织样品制备指南(不含藻类)
较老组织 RNA 含量低,而且次生代谢物含量相对较高,用于 RNA 提取的成功率低。因此在不影响实验设计的前提下,须选择健康、幼嫩的组织新鲜组织样采样流程如下:
1)提前准备好冷冻组织的足量液氮,预装样品的冻存管,并在做好标记(尽量不使用汉字命名,命名字符控制在 5 个以内)
2)植物材料取材后用清水将材料表面的灰尘及泥土冲洗干净,吸干表面水渍,再从植物体上取下新鲜组织。注:如果是需要进行处理,请在活体上进行处理后再取样。
3)如果组织体积较大,将组织剪切成 50-100 mg 小块,约黄豆大小的小块,放入提前准备好的冻存管中;
5)立即(20s 内)置于液氮中冷冻 3~4 h,然后将单个样本放于自封袋中,转移至-80 °C 长期保存;
运送方式:干冰运输。
注:植物组织不建议使用组织保护液保存。对于一些需要剥去种皮处理的,因样品速冻后无法准确剔除,如有需要剥去种皮的老师须自行操作。

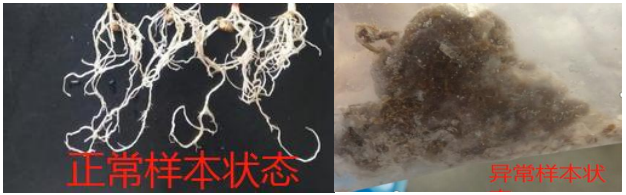
水产类样品制备指南
水产类包括淡水鱼类、海水鱼类、贝类、藻类。送样需要选择新鲜采集的样本,海水类物种需要进行淡化处理。
取样注意事项
优先选用新鲜采集的样品送样,稀有样本可酌情选取冻存组织。采集样品时应选取核酸含量较多的部位。样品采集时建议活体取材后用预冷的 0.9%生理盐水进行漂洗,以去除血渍和污物,将样品分割成 50 mg 左右的小块(约黄豆大小,组织块越小,保存效果越好),样品分割和处理时应尽量在冰上进行,防止样品降解。避免装样太满以至冻裂,造成样品污染。藻类样本:大型藻类送样量(干重)不少于 3g,单细胞藻类(干重)不少于 1g。注:水产类样品需尽量保证为新鲜个体。尽量避免寄送保存时间较长或经过反复冻融的组织样品。针对软体动物可先使用 75%的乙醇进行漂洗,漂洗干净后液氮冷冻,干冰运输;针对刺胞动物,可去除头部和肠道等部位,保留肌肉外壁用于提取。

昆虫类样品制备指南
1)昆虫样本,需进行表面微生物的清洗,较大个体的选取不带肠道部分的组织,对于较小个体只能用整个个体的,应进行适当的饥饿处理(注意保证昆虫的活性)。
2)提前准备好冷冻组织的足量液氮,预装样品的冻存管,并在做好标记(尽量不使用汉字命名,命名字符控制在 5 个以内)
3)个体大的,如毛毛虫,取得活体组织后,用清水清洗,以去除污物,吸干表面液体。将组织样品分割成约 50 mg 的小块(约黄豆大小),液氮速冻后,放入干净的带螺纹旋盖保存管中;
4) 转移至-80℃低温保存,送样时选择干冰运输寄送。
注:小型昆虫组织务必在信息单中备注微量样本需液氮交接防止降解。同时该类样本因只满足一次或低于常规一次提取用量,我们无法保证 100%提取合格。
微生物类样品制备指南
(一)酵母菌
一次反应所需酵母菌的量需≤1 X 10^7 个,以 5 X 10^6-1 X 10^7 个为宜。单次送样量满足 3 次以上提取,建议分装送样,每管满足一次提取量,即 3 X 1 X 10^7 个。显微镜下观察酵母菌生长状态,收集对数期生长旺盛的酵母菌将适量体积的酵母菌液转移至将 2 mL 旋盖尖底离心管(无菌,无核酸酶)中,于室温下14000 X g 离心 1 min,弃尽培养基,将酵母细胞沉淀迅速置于液氮中冷冻 3~4 h,然后转移至-80 °C 或液氮中长期保存干冰运输。
(二)真菌
显微镜下观察真菌生长状态,根据菌类的生长规律,收集生长旺盛的菌体。真菌样本在进行RNA 提取前,需要进行称重,一次反应所需的真菌量为 50 ~100mg(由于不同真菌得率差异较大,所以建议送样量尽量多或根据客户经验得率送满足 3 次的量)真菌取样方式以客户实验室经验操作即可,要求取样后到速冻前时间短,菌处于快速生长的活跃期取样后的真菌置于预冷的离心管或冻存管中,迅速置于液氮中冷冻 3~4 h,-80 °C 长久保存干冰运输。
注:请勿直接寄送培养平板,低温保鲜寄送的真菌培养平板,无法保证菌体的生长状态。为了提高真菌菌体 RNA 的提取成功率,应将生长旺盛的菌体收集到 2 mL 旋盖尖底离心管(无菌,无核酸酶)中,迅速置于液氮中冷冻 3~4 h,然后转移至-80℃或液氮中长期保存。
样品制备注意事项
核酸提取质量与物种及组织部位、采集方法及保存状态、提取方法及操作、实验器材及环境等因素均有密不可分的联系,尤其是三代超长提取对样本的质量、总量要求更高,望知悉及理解,并做好样本备份。为了保障获得高质量的核酸,请务必按照送样手册所规定的准备样本。对珍贵样本或者微量样本,建议自行提取。
1) 组织速冻时间:组织离体后,胞内核酸便开始降解,尤其是 RNA,故采集时,目的组织离体后,需立即速冻,建议 3min 内完成,越快越好。
2) 组织送样量:建议送样量适用于 95%的物种组织,少部分组织因胞内核酸量较低,需适当增加送样量,比如动物皮肤、毛发,植物果实、根等。请严格按照上方组织送样量要求送样,送样量过少或过多均不利于提取实验。采样量较少会导致提取的 RNA 总量、浓度不合格,采样量过多反而会造成速冻不彻底、提取取样困难、冻融降解等危险。
3) 组织保存管的选择:所有组织样品务必使用离心管或螺纹管保存,切勿直接装入密封袋(低温冻脆易破裂,导致样品泄露,交叉污染)保存。
4) 组织样品保存方法选择:首选液氮速冻;没有液氮条件的,可直接放入-80℃冰箱冻存;环境条件限制的,可使用商组织保护液保存(这试剂对动物组织可起到一定的效果,植物、菌类、细胞,微量样品不可以使用),并严格按相应试剂说明操作。
5) 冻融组织: 组织冻存后,一旦冻融,RNA 降解概率大于 80%,几乎不可能提取成功,此类组织不建议送样。请各位老师送样前注意组织保存状态, 确保组织未发生过冻融情况。
6) 长年保存的组织:保存时间超过一年的组织不建议送样。
7) 组织分离要求:正常组织样本中不能含有病变组织,而病变组织样本中也不可以夹带有正常组织(如目的部位为叶片,就不能含有茎),提取实验时无法精确取样,无法称重。组织量过多的不能全部取样,只随机选取适量组织提取。
8) 对于同一个组织样品需要同时提取 DNA 和 RNA 的,请务必分成两管分批次送样。
9) 样本的特殊处理:样本的特殊处理包括:盐处理、温度处理、药物处理、病毒侵染、伤害处理、干旱处理等胁迫处理方式,不同程度的处理对样本的 RNA 质量会造成不同程度的影响,常见的会导致 RNA 的降解或者得率降低。因此,经过特殊处理的样本,在送样时,务必请在样本信息单中进行详细的备注,以便尽量提高提取的成功率和避免样本的浪费。
核酸质量判定标准
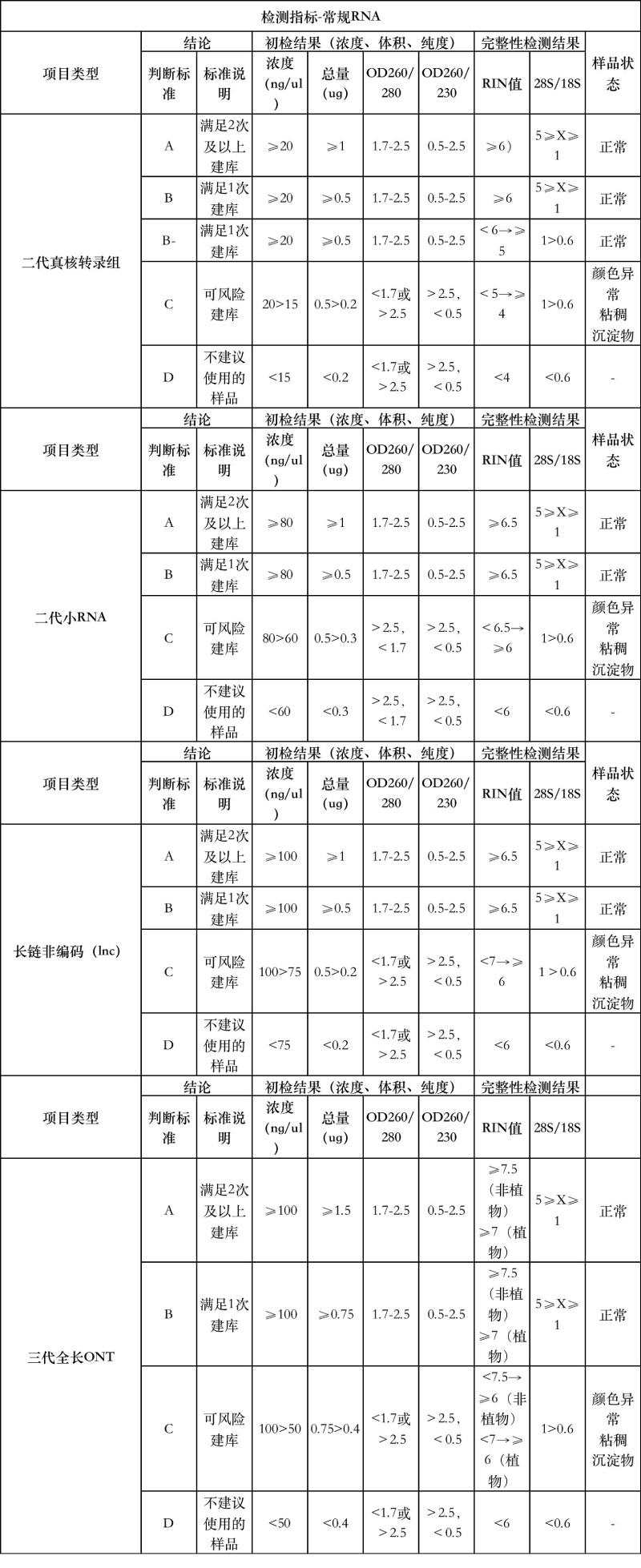
常规 RNA 质量判定标准
备注:
1、对于昆虫、软体动物等特殊物种,完整性检测已基线为准
2、以上均是单个文库的总量要求,如果样品做多个文库按(小 RNA>LNCRNA>转录组 RNA)判。总量不足的文库有样品判 C 不通过,无不合格原因,根据二次提取的总量判定。无样品根据剩余总量判判定下一文库。
样本制备不足、降解可能存在的风险
(一)总量不足或浓度过低存在风险
1) 文库构建失败
2) 文库产量低不能上机测序或测序数据量不足
3) 导致 RNA-seq 数据随机性异常
(二)降解样本
1) 建库失败
2) 导致 RNA-seq 数据 duplication 比例高、随机性差
3) 导致 Small RNA rRNA 比例高,影响有效数据,文库片段异常
(三)目标 RNA 含量低
1) 总 RNA 达到要求,但由于样本特异性,small RNA 含量低于正常样本,导致建库失败
2) 总 RNA 达到要求,但由于处理或组织部位的特异性,mRNA 降解或含量低,导致建库失败或者测序数据中 rRNA 数据比例高
(四)蛋白或其他杂质污染
1) 可能影响 Small RNA 电泳分离,造成切胶不准,影响问题质量
2) 可能影响 RNA-seq 磁珠分离导致建库失败,或即使达到上机要求也可能导致文库随机性差等问题






 京公网安备 11011302003368号
京公网安备 11011302003368号