近几年国家自然科学基金资助项目中,免疫调控项目占比年年创新高,从2022年国自然公布的情况来看,免疫调控依旧是国自然的重点、热点领域。机体用来防御感染和疾病的免疫系统在免疫调节过程中,通过免疫器官、免疫细胞细胞、免疫活性物质以及其它系统之间组成复杂的调控网络机制,来维持机体的稳定,免疫系统的紊乱与调节机制也就成为了医学和生命科学研究中的热门领域。
免疫系统分为固有免疫和适应性免疫,固有免疫是机体在发育和进化过程中形成的天然免疫防御功能,也称为非特异性免疫;与此相对应的是适应性免疫,指出生后通过与抗原物质接触所产生的一系列防御功能,包括B细胞介导的体液免疫应答和T细胞介导的细胞免疫应答,免疫应答主要依赖于B细胞受体(B Cell Recptor, BCR)和T细胞受体(T Cell Recptor, TCR)识别多种多样的抗原分子,发挥功能清除病原体或体内肿瘤细胞,BCR和TCR基因中产生巨大的序列变异,可以创造大量的具有不同免疫受体和抗原特异性的淋巴细胞。因此在单细胞水平分析免疫微环境细胞组成、表达模式、生物学功能及细胞间相互作用模式等特征,可以更深入了解免疫系统调节机制,而单细胞免疫组库技术就是在解析免疫微环境特征的同时,还能揭示T/B淋巴细胞抗原受体多样性,为适应性免疫应答过程的探索提供更清晰的视角。
研究进展
免疫学是现代医学的一个主要领域,是许多重要科学的研究热点和医学突破的前沿,免疫细胞参与人体多器官疾病的发展,对免疫信号传导、免疫细胞迁移和免疫组库的详细了解有助于开发新的治疗方法来对抗各种疾病,识别与这些疾病发生密切相关的免疫细胞,可以进一步发现这些疾病的分子机制。利用单细胞免疫组库技术,基于大量的单细胞基因表达和克隆型的多样性数据,可以提供细胞表达特征聚类、亚群表达特征的分析、标志物筛选等方面的分析,揭示免疫组库克隆性、多样性、抗原特异性和细胞微环境[1],目前已广泛应用在基础免疫学研究、自身免疫性疾病、移植与免疫重建、肿瘤免疫与治疗、传染病及疫苗研发等研究领域。
1)利用单细胞免疫组库技术,追踪适应性免疫系统的发育与建立,如探究胸腺器官发育图谱、解析不同发育时期V(D)J重组特征;探索健康和疾病状态下免疫系统的基本生物学,重新定义免疫细胞类型和分子特征,解析疾病进展中免疫失调特征;
2)利用单细胞免疫组库技术,理解肿瘤与免疫的相互作用,寻找恶性肿瘤免疫治疗的潜在靶点;揭示移植体抗宿主病背后的生物学机制,为免疫调节治疗提供潜在方向;破译错误导向免疫应答的机制,解析免疫耐受机制与免疫应答动态调节之间的复杂相互作用;
3)利用单细胞免疫组库技术,表征肿瘤患者对免疫检查点阻断的应答,筛选获益人群;改造T细胞开发新的癌症免疫治疗策略(CAR-T、TCR-T细胞疗法);了解疫苗接种后的抗体应答,助力疫苗开发…..
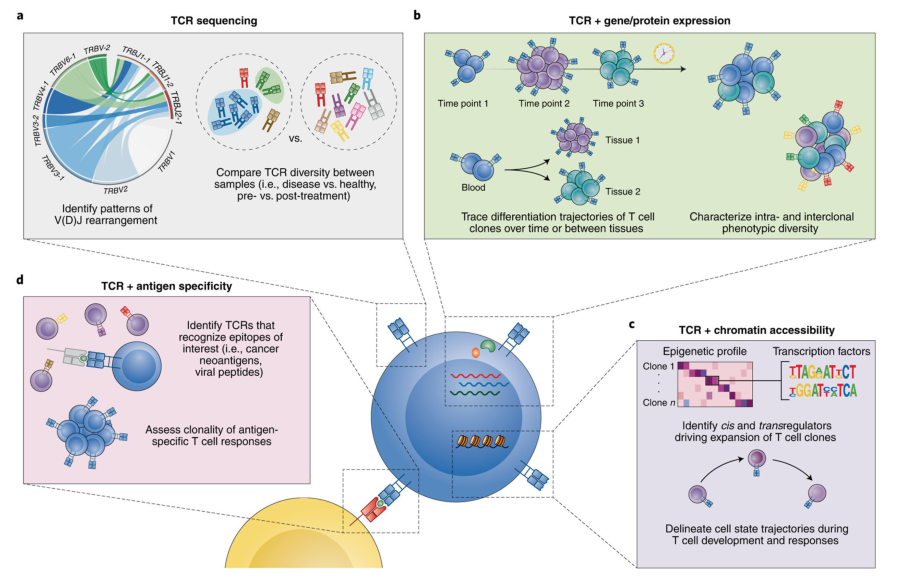
图1 T细胞免疫组库多样性测序研究进展[1]
免疫调控应用案例
利用单细胞免疫组库技术,探索健康和疾病状态下免疫系统的基本生物学,鉴定人体内的免疫细胞身份、功能和组织,并应用到免疫学的各个领域,包括分析新兴病原体、开发疫苗、开发免疫肿瘤学疗法、认识自身免疫疾病及实施安全的器官移植等。
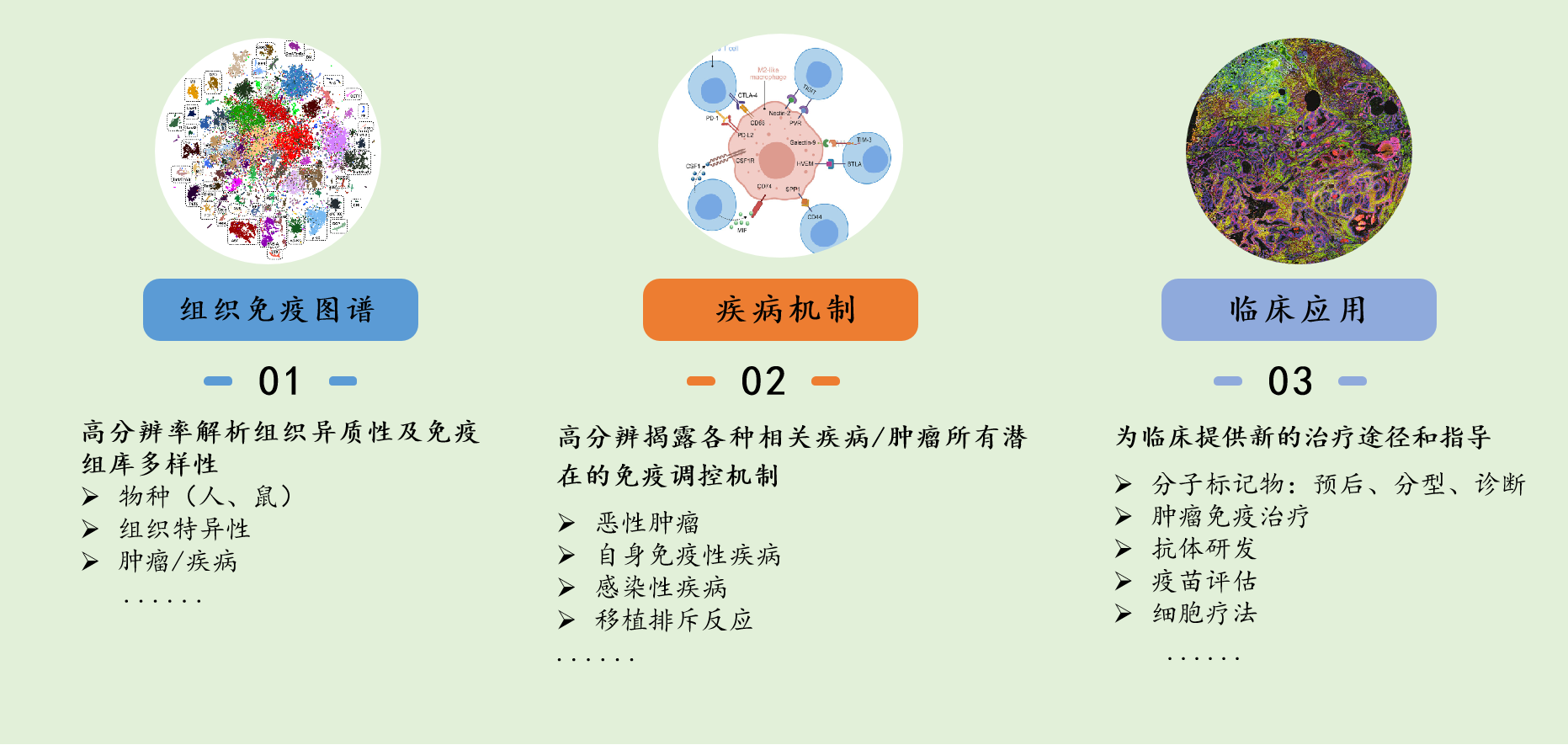
01、绘制组织免疫图谱
免疫调控应用案例1、单细胞免疫组库分析揭示人组织特异性免疫特征[2]
标题:Cross-tissue immune cell analysis reveals tissue-specific features in humans
期刊名称:Science
影响因子:63.714
发表时间:2022年5月
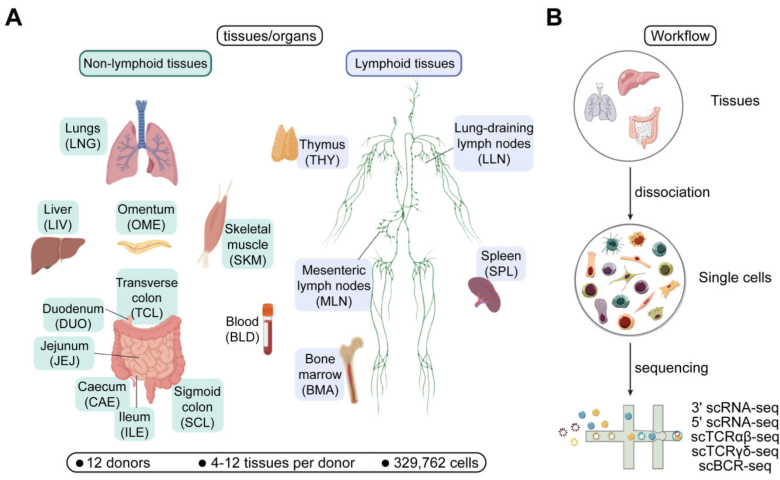
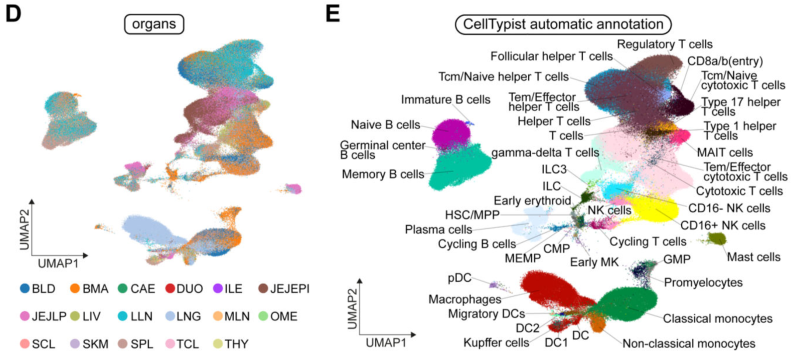
样本设计:2个成人捐献者的16份组织样本,分别进行scRNA、scTCR、scBCR,实验中采集的组织样本包括初级淋巴器官(骨髓)和次级淋巴器官(脾、肺引流和肠系膜淋巴结)、粘膜组织(肠和肺)以及血液和肝脏等非淋巴组织,还包括胸腺、骨骼肌和网膜。
研究内容:目前对于人体组织中免疫细胞的分型仍知之甚少,无法快速精准地对免疫细胞进行分型。本研究通过单细胞免疫组库测序对16份组织类型样本进行分析,得到了357,211个单细胞数据,其中329,762个细胞都是免疫细胞,确定了43个细胞特异性的细胞亚群,构建了人类跨组织的免疫细胞图谱,揭示了已知免疫细胞类型在不同组织微环境中的分布情况,并解析了人类免疫系统的组织特异性以及丰富的T细胞和B细胞克隆型,同时开发了CellTypist细胞类型自动注释平台。
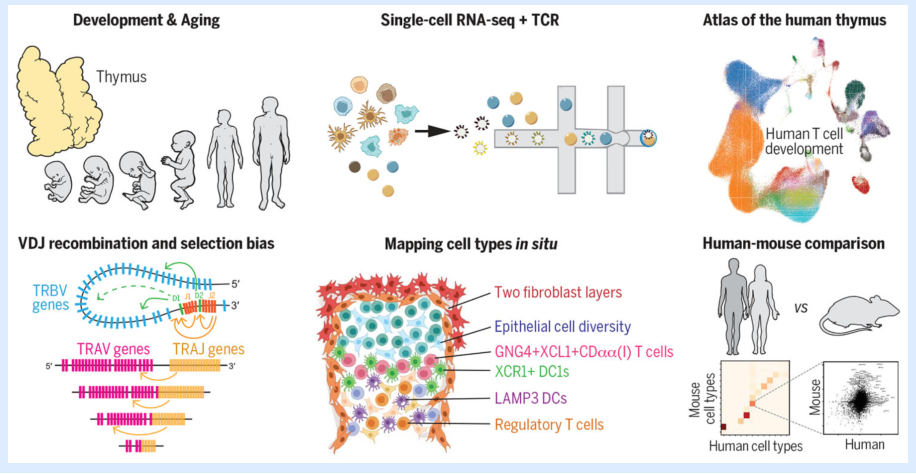
免疫调控应用案例2、人类胸腺发育细胞图谱揭示了T细胞组库的形成[3]
标题:A cell atlas of human thymic development defines T cell repertoire formation
期刊名称:Science
影响因子:41.845
发表时间:2020年2月
样本设计:共采集了15个胎儿胸腺(从7-17孕周)和9个出生后至成人期的胸腺样本,4、8和24 w孕周小鼠胸腺样本,并根据CD45、CD3和EpCAM表达对分离的流式分选富集免疫细胞和非免疫细胞、T细胞、上皮细胞,进行scRNA-seq + scTCR-seq。
研究内容:胸腺是T细胞发育和TCR形成的重要器官,塑造了机体的适应性免疫,T细胞的胸腺内发育有空间协调性,受胸腺微环境多种细胞类型的精细调节,但目前尚缺少一份完整的人类胸腺图谱帮助理解人体免疫系统。本研究绘制了胸腺单细胞时空图谱,描绘了胸腺来源T细胞的多样性以及构成胸腺微环境的细胞空间定位;在单细胞分辨率下重建T细胞发育轨迹,揭示了人 TCR 免疫组库形成和选择的偏倚特征,提示了人体如何应对不同的抗原挑战;最后,提供了人类和小鼠胸腺细胞图谱之间的系统比较。
02、解析疾病机制
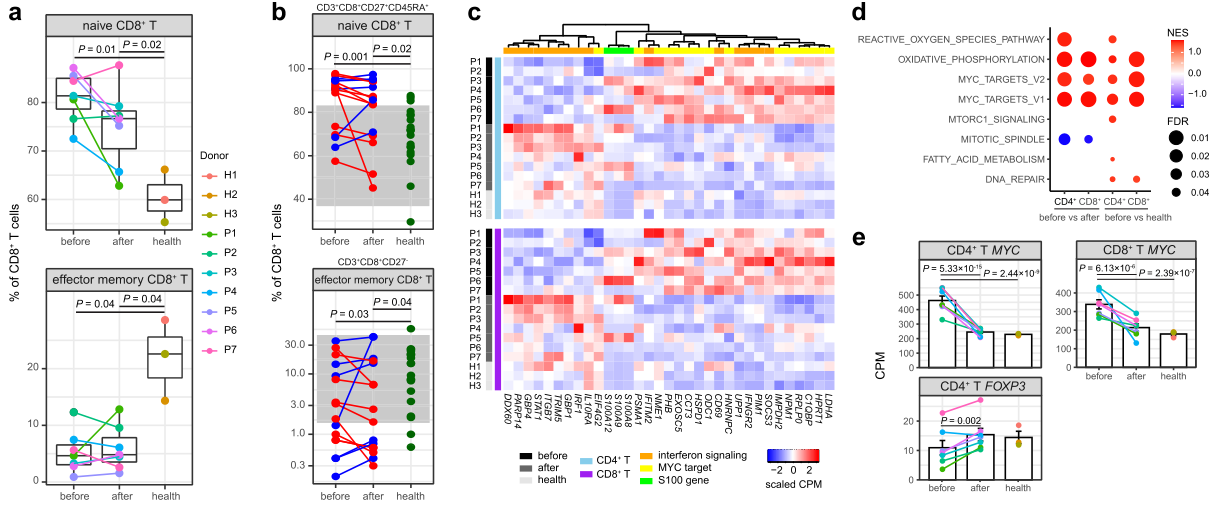
免疫调控应用案例3、单细胞免疫组库揭示了川崎病发病和治疗过程中外周免疫细胞动态变化[4]
标题:Single-cell RNA sequencing of peripheral blood mononuclear cells from acute Kawasaki disease Patients
期刊名称:Nature Communications
影响因子:17.694
发表时间:2021年9月
样本设计:7名急性KD患者接受静脉注射免疫球蛋白(IVIG)治疗前、后,3例年龄匹配的健康对照,取新鲜外周血PBMC样本,进行scRNA+scTCR+scBCR测序。
研究内容:川崎病(KD)是一种急性全身性发热性疾病和儿童期血管炎,可导致冠状动脉病变,已成为许多发达国家儿童获得性心脏病的常见原因。尽管已经报道了免疫细胞的功能和表型变化,但对急性KD全局免疫反应的理解尚不清楚。本研究通过对IVIG治疗前后的KD患者PBMC样本进行单细胞免疫组库测序,发现了CD8+T细胞在治疗后的特异性克隆扩增,提示是常规抗原而非超抗原可能是KD发病机制的原因,CD8+T相关细胞的比例是川崎病的重要风险因素;研究绘制了川崎病外周血单细胞免疫图谱,揭示了川崎病治疗前后及对照中PBMC各类型免疫细胞比例、基因表达、免疫反应、生物学功能以及细胞表面受体的变化。
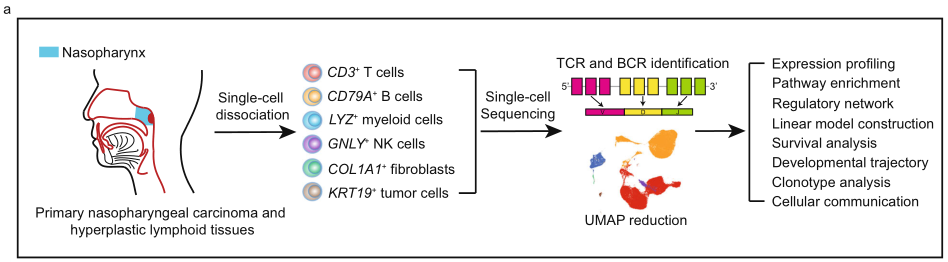
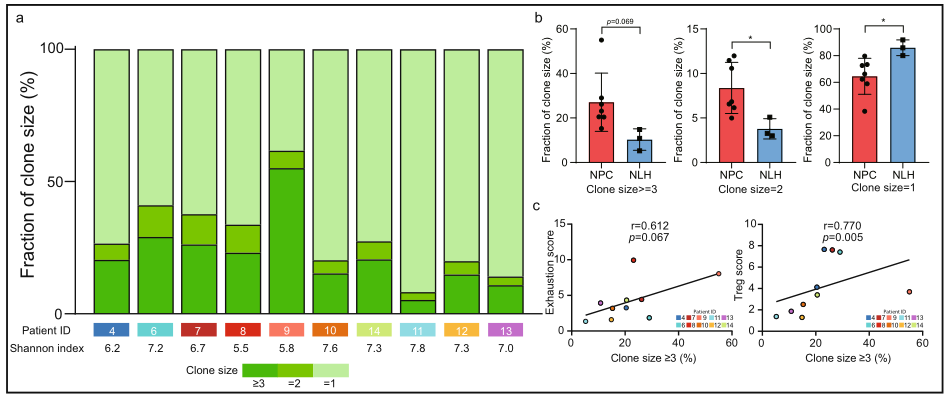
免疫调控应用案例4、单细胞免疫组库揭示鼻咽癌微环境中基质细胞与肿瘤细胞特征[5]
标题:Comprehensive single-cell sequencing reveals the stromal dynamics and tumor-specific characteristics in the microenvironment of nasopharyngeal carcinoma
期刊名称:Nature Communications
影响因子:17.694
发表时间:2021年9月
样本设计:11例鼻咽癌患者的肿瘤样本和3例非恶性鼻咽淋巴增生的样本,进行scRNA+scTCR+scBCR测序。
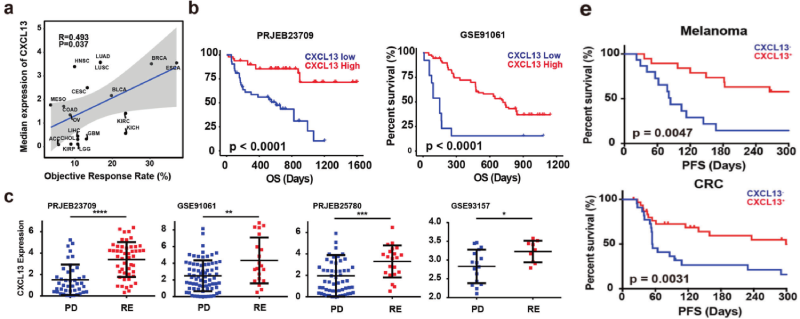
研究内容:鼻咽癌的病理学特征表现为肿瘤内部和附近经常被成分复杂的免疫细胞所浸润,这种微环境特征在理论上表明了免疫治疗在鼻咽癌中具有极高的潜力。然而在I期和II期临床试验中,鼻咽癌患者对免疫疗法的反应率仅有 20%-30%,表明鼻咽癌微环境中细胞异质性和动态功能需要进一步精准解析,从而优化针对鼻咽癌的精准治疗。本研究利用单细胞免疫组库技术系统地对比了鼻咽癌肿瘤微环境和非恶性鼻咽微环境的构成和功能状态,发现初始B细胞、记忆性B细胞和效应B细胞和鼻咽癌患者的预后呈显著正相关,双阴性B细胞则和鼻咽癌患者的预后呈显著负相关,成为预测鼻咽癌患者预后的潜在生物标记物;耗竭T细胞高度表达 CXCL13,可能是招募 CXCR5+ B细胞并促进三级淋巴结构形成的重要分子机制,可能是影响B细胞在鼻咽癌肿瘤微环境中浸润程度的因素之一;该研究发现了与鼻咽癌患者预后相关的特征基因和细胞亚群,从而为研究鼻咽癌微环境中的分子机制和优化鼻咽癌精准治疗提供了分子生物学上的依据。
免疫调控应用案例5、单细胞免疫组库揭示多发性硬化症新机制[6]
标题:Bone marrow hematopoiesis drives multiple sclerosis progression
期刊名称:Cell
影响因子:66.850
发表时间:2022年6月
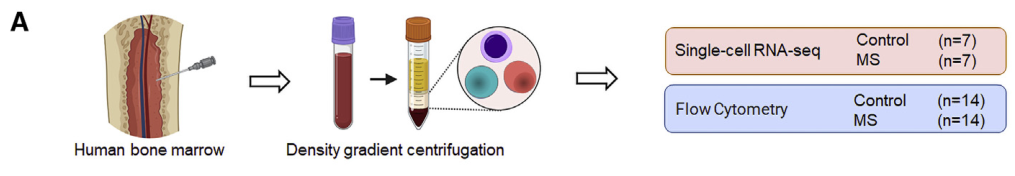
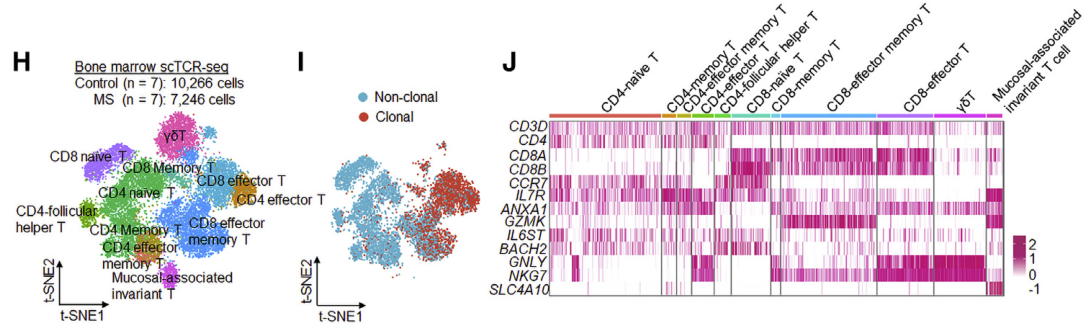
样本设计:MS患者及健康对照各7例,取骨髓样本,进行scRNA-seq+scTCR-seq。
研究内容:多发性硬化症(MS)是一种T细胞介导的中枢神经系统自身免疫性疾病,也是一种伴随终生的神经退行性疾病,T细胞失去自身免疫耐受是MS症状的核心机制,骨髓作为中枢免疫器官和造血器官,对维持外周和中枢的免疫稳态具有重要作用,但其对MS疾病进展的影响还不清楚。本研究利用单细胞免疫组库测序、流式细胞术及谱系追踪分析了MS患者在疾病活动期骨髓造血系统的特征,与健康对照组相比,MS患者的造血干细胞、祖细胞及髓系细胞数量显著增加,骨髓T细胞克隆数量和多样性明显增加;MS小鼠模型骨髓微环境的趋化因子CXCL12驱动自身反应性T细胞大量进入骨髓,在到达骨髓后高度表达趋化因子CCL5,从而引起髓系增生,为治疗MS提供了新思路–通过再平衡骨髓造血系统,回归免疫系统稳态,从而减轻神经系统炎症损伤。
03、临床应用
免疫调控应用案例6、单细胞免疫组库揭示肾透明细胞癌组织驻留T细胞与免疫治疗疗效[7]
标题:Single-cell sequencing links multiregional immune landscapes and tissue-resident T cells in ccRCC to tumor topology and therapy efficacy
期刊名称:Cancer Cell
影响因子:38.585
发表时间:2021年5月
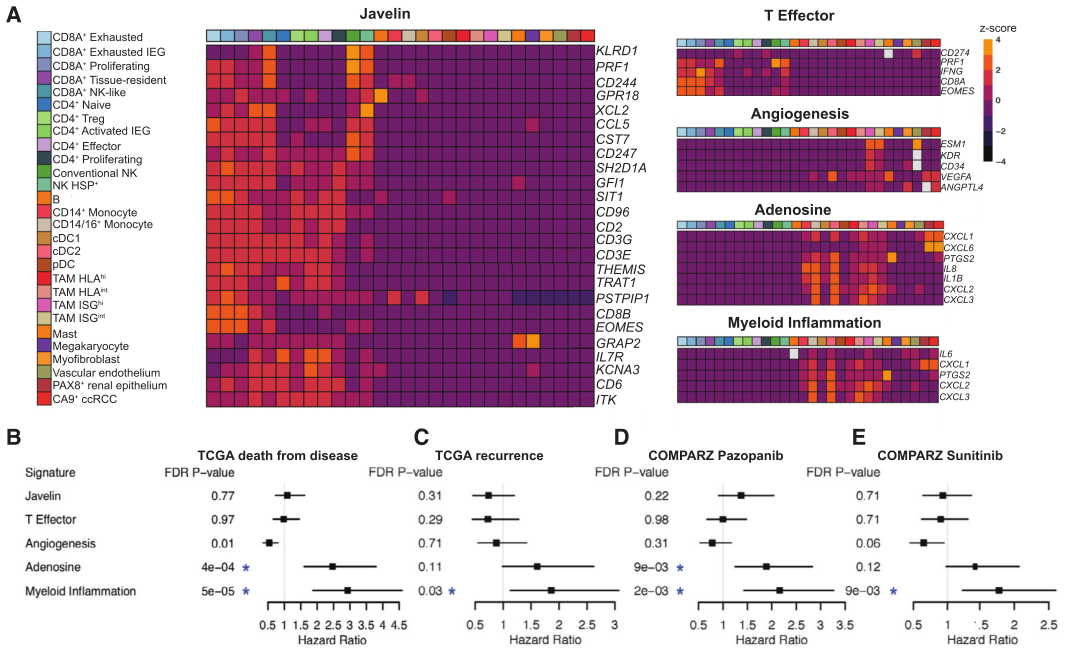
样本设计:6例接受和未接受ICB治疗的肾透明细胞癌(ccRCC)患者癌组织、淋巴结、癌旁组织和血液PBMC,共29个样本,进行scRNA-seq + scTCR-seq。研究内容:ccRCC具有高度免疫浸润性,免疫检查点阻断(ICB)治疗和联合方案显著提高ccRCC患者的生存率,但免疫异质性对于鉴定更有效的ccRCC治疗靶标及预测响应水平的生物标志物产生了干扰。本研究针对免疫治疗前后ccRCC组织和PBMC样本分别进行单细胞免疫组库测序分析,构建了167,283个细胞基因表达图谱和43,828个细胞的TCR克隆型图谱,共鉴定到28个细胞亚群;构建了167,283个细胞基因表达图谱和43,828个细胞的TCR克隆型图谱,共鉴定到28个细胞亚群,绘制ccRCC的多区域免疫异质性图谱;TCR克隆序列相似性分析,发现ICB耐药组高扩增克隆型间克隆序列存在高度相似性;TCR分化轨迹分析,发现在ICB响应组CD8+组织驻留T细胞与NK样细胞存在相互转化轨迹;结合TCGA多队列免疫治疗数据分析,验证了CD8+组织驻留T细胞的预后价值,能够一定程度上预测免疫治疗的疗效。
免疫调控应用案例7、单细胞免疫组库技术发现潜在的SARS-CoV-2中和抗体[8]
标题:Potent Neutralizing Antibodies against SARS-CoV-2 Identified by High-Throughput Single-Cell Sequencing of Convalescent Patients’ B Cells
期刊名称:Cell
影响因子:36.216
发表时间:2020年5月
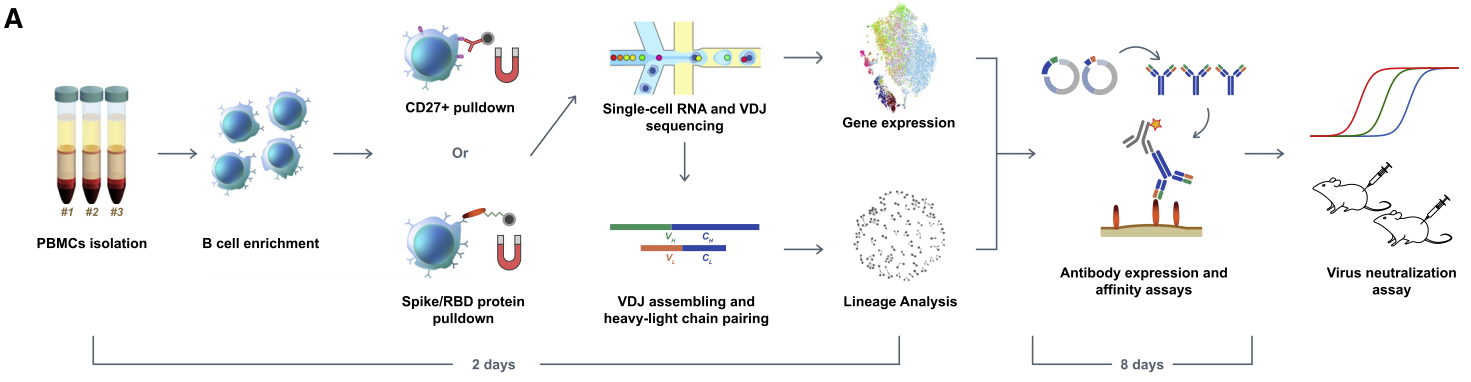
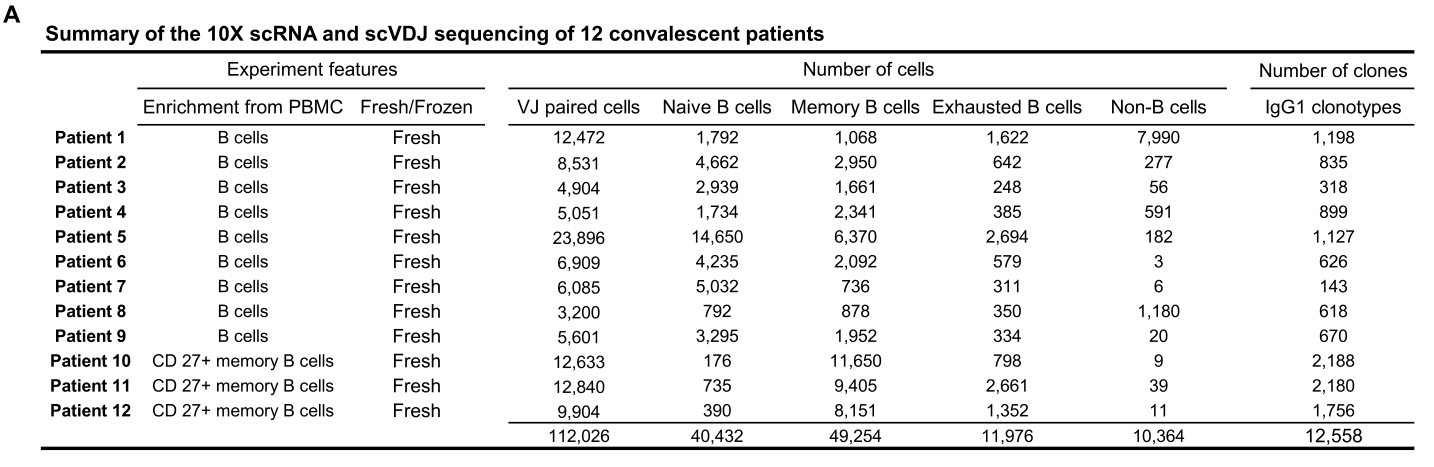
样本设计:从12个COVID-19康复患者的外周血单核细胞PBMC中分离B细胞,对B细胞和CD27+记忆B细胞进行scRNA-seq + scBCR-seq,获得IgG1亚型抗体,并进行抗体体外检测和筛选。
研究内容:针对新冠病毒人源单克隆抗体的分离鉴定的方法,如单个记忆 B 细胞的克隆扩增,通常用于从异质B细胞群体中获得免疫球蛋白轻重链RNA序列,以产生单克隆抗体,但由于耗时的孵化和筛选步骤,使该技术至少需要几个月才能完成成功的筛选。本研究利用单细胞免疫组库技术对60名新冠病毒感染恢复期患者富含抗原的B细胞进行分析,从8,558种抗原结合 IgG1+克隆型中鉴定出了14种有效的中和抗体,其中强效的BD-368-2在SARS-CoV-2感染的 hACE2转基因小鼠中也显示出强大的治疗和预防功效;研究证明了通过B细胞的单细胞高通量测序技术可以大大缩短抗体的筛选周期,有效发现人源中和单克隆抗体,为新冠病毒以及未来大流行病的抗体疫苗研发提供了非常重要的科学和实用价值。
免疫调控应用案例8、单细胞转录组联合TCR-seq解析了肿瘤抗原特异性T细胞及生物标志物鉴定[9]
标题:Defined tumor antigen-specific T cells potentiate personalized TCR-T cell therapy and prediction of immunotherapy response
期刊名称:Cell Research
影响因子:46.297
发表时间:2022年6月
样本设计:通过scRNA-seq、scTCR-seq和体外新抗原刺激,对肿瘤及其邻近组织中的T细胞进行了全面解析。
研究内容:针对肿瘤特异性抗原(TSA)的个性化免疫疗法可以在不损害正常组织的情况下产生有效和安全的抗肿瘤免疫反应,尽管新抗原疫苗已在临床试验中显示出治疗效果,但从肿瘤突变中预测新抗原仍然具有挑战性,宿主抗肿瘤免疫反应选择并激活识别肿瘤抗原的T细胞;因此用来自患者体内这些天然存在的肿瘤抗原特异性T(Tas)细胞的T细胞受体改造的T细胞将靶向患者肿瘤中的TSA。本研究揭示了Tas 细胞的特点是肿瘤富集、肿瘤特异性克隆扩增和新抗原特异性;评估了肿瘤中Tas细胞标记物CXCL13的表达水平可能比来自免疫周期早期步骤的标志物(如TMB)更jing q 地预测对ICB 的反应;并将CD200和ENTPD1分别鉴定为CD4+和CD8+Tas细胞的表面标志物。
百迈客项目经验
免疫器官可分为中枢免疫器官和外周免疫器官,免疫器官分为中枢免疫器官和外周免疫器官,前者包括胸腺和骨髓,是免疫细胞形成和分化成熟的场所;后者包括淋巴结、脾脏、扁桃体、阑尾、肠集合淋巴结、呼吸道和消化道黏膜下层等淋巴组织,是T/B淋巴细胞定居、增殖的场所及发生免疫应答的主要部位。两者则主要是通过血液循环及淋巴循环相互联系,从目前发表的10x单细胞免疫组库文章样本类型数目统计来看,外周血和相关免疫器官的免疫多样性特征研究是主要聚焦方向。
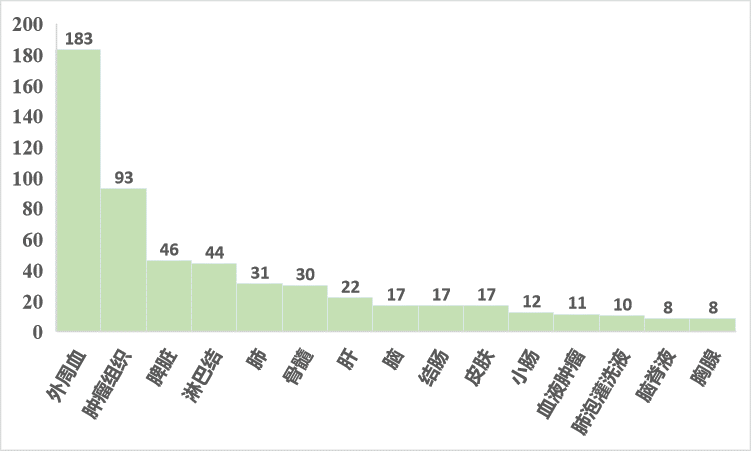
图2 10x单细胞免疫组库文章样本类型分布(来源于10x官网)
百迈客自2019年推出单细胞免疫组库测序服务后积累了大量的项目经验,目前累计已完成1000+个样本的分选富集,包含25+种组织类型,涉及疾病类型超40+种,包含结直肠癌、白血病、皮肤病、肺癌、乳腺癌、肝癌、卵巢癌、胃癌、宫颈癌、鼻咽癌、黑色素瘤等。
与图2展示的类似,百迈客实测项目中血液样本数量很多,占比超60%;血液样本相较于组织样本,无需进行细胞解离,能够避免细胞解离引起的细胞活性受损、细胞类型丢失等问题;尤其是临床样本,往往涉及到组织样本获取难度大的问题,患者治疗后肿瘤组织取样更是很多老师的困扰,因此取配对的血液样本就成了一个合适的替代方案,在临床监测、标志物诊断方面更是具有巨大的优势。
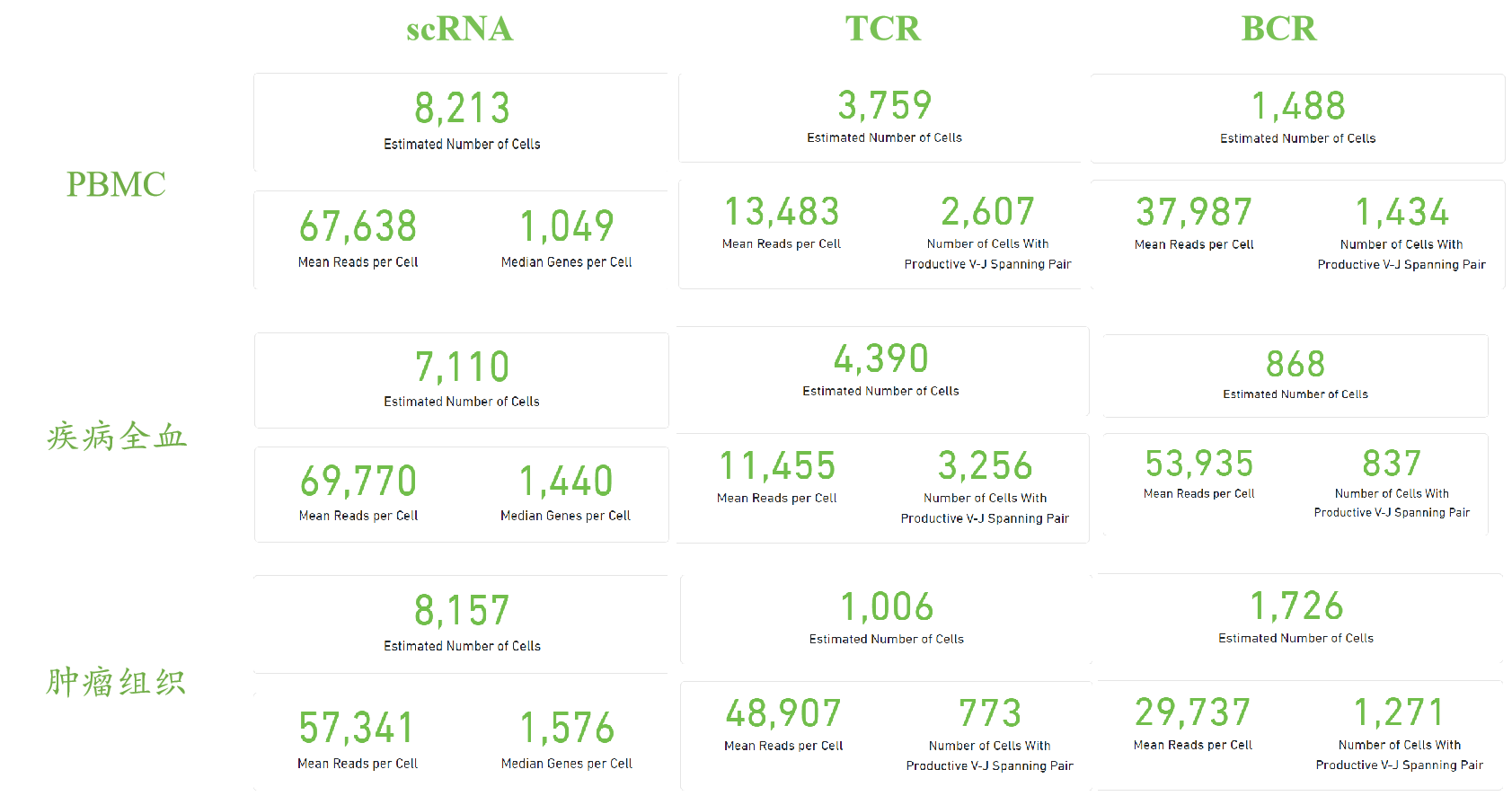
图3 百迈客实测数据表现
Tips:对于血液样本,送样量2-3mL即可,推荐选择上门服务;如果需要寄送,可用EDTA紫色抗凝管保存,24h内寄送到百迈客实验室分离PBMC上机;或者分选完PBMC后加细胞冻存液梯度冻存,干冰寄送。
小结
通过单细胞免疫组库测序,构建组织/疾病高分辨率细胞异质性图谱,全面解析基因表达及免疫组库多样性,挖掘与疾病发生发展相关的关键细胞亚群和信号通路变化、克隆型扩增,为鉴定预后诊断分子标记物、优化升级癌症免疫治疗疗法、开发抗体/疫苗等临床应用提供强有力的基础。
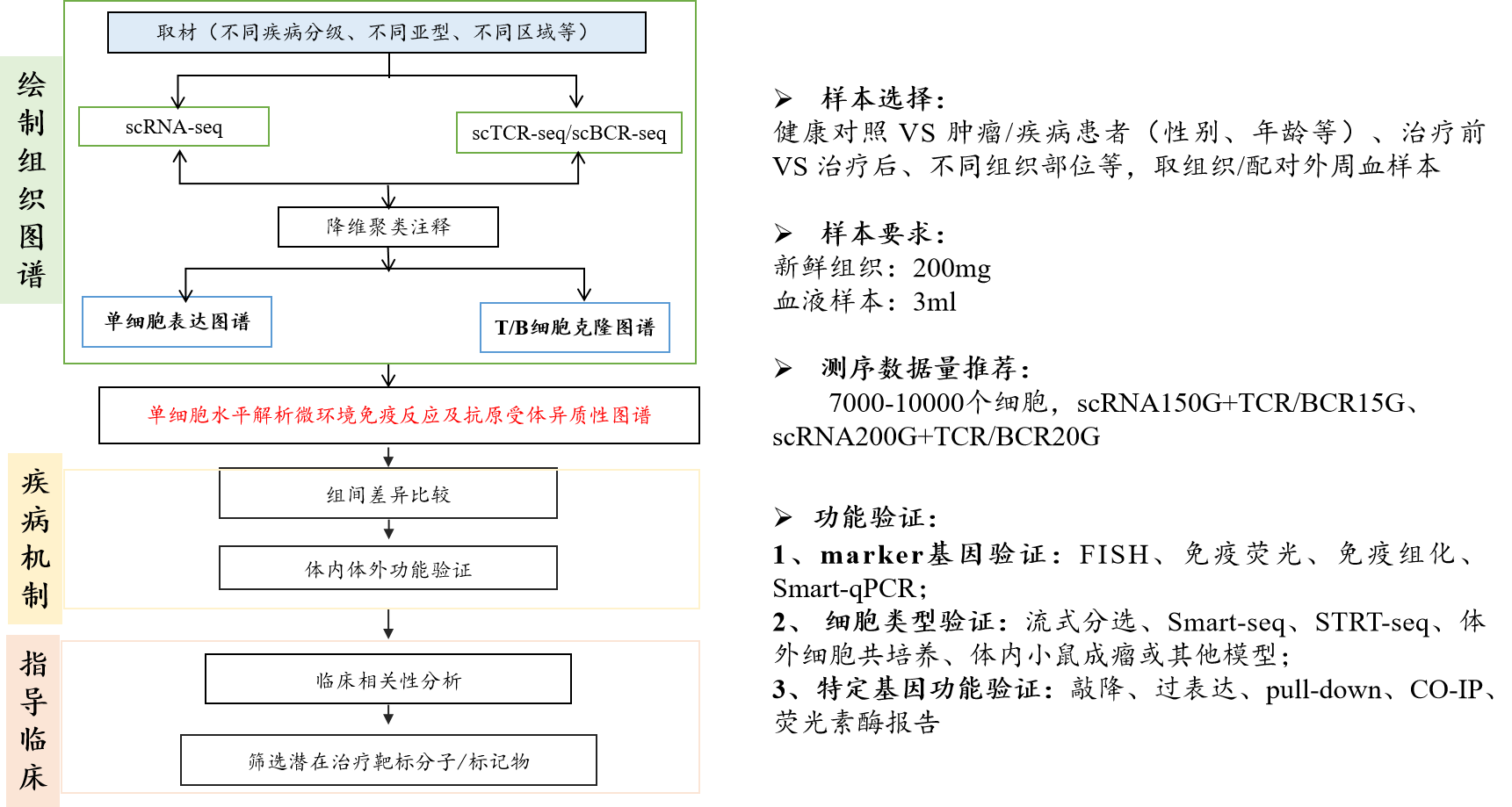
图3 单细胞免疫组库研究方案设计
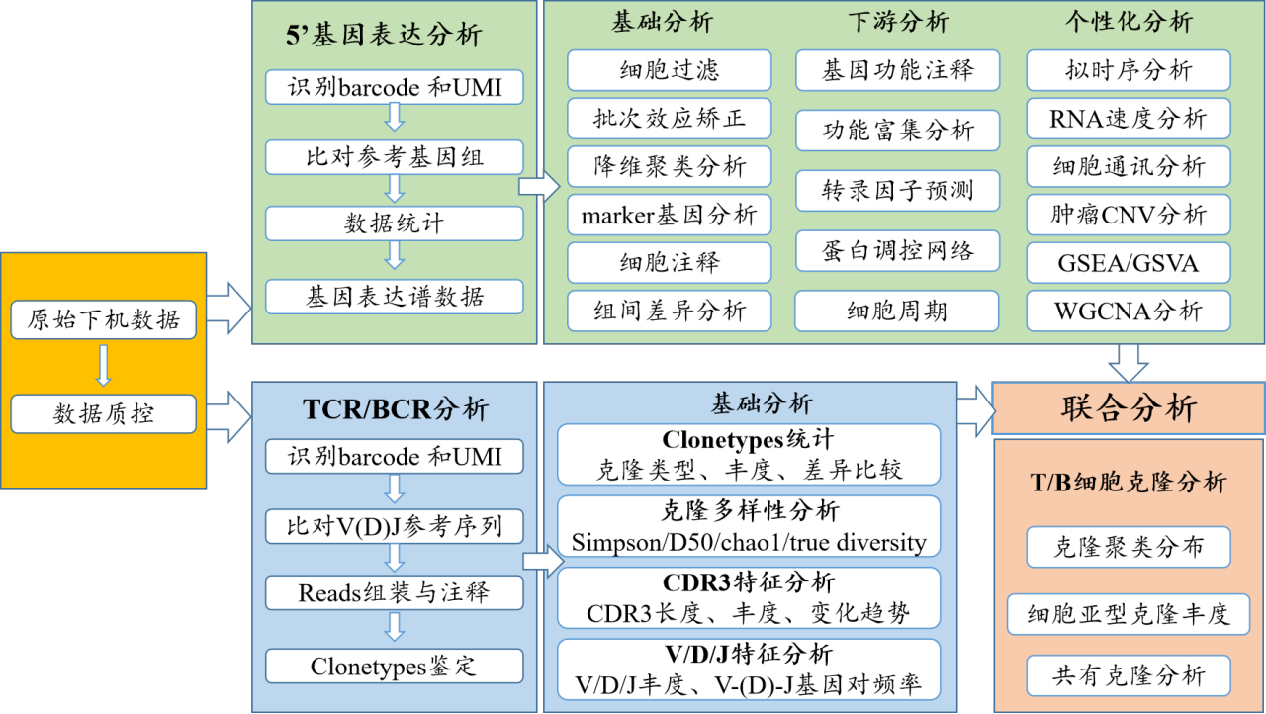
图4 百迈客单细胞免疫组库测序分析内容
百迈客单细胞空间多组学平台
百迈客同时具有百创DG1000和10x Genomics单细胞测序服务平台、百创S1000和10x Genomics空间测序服务平台,百创S1000空间测序技术更是“亚细胞级分辨率”和“微孔”结合的原位捕获空间测序技术,其独立设计的Spatial Barcode还可以高度适配Oxford Nanopore Technologies(ONT)平台,助力国产化空间测序技术进入新的时代。
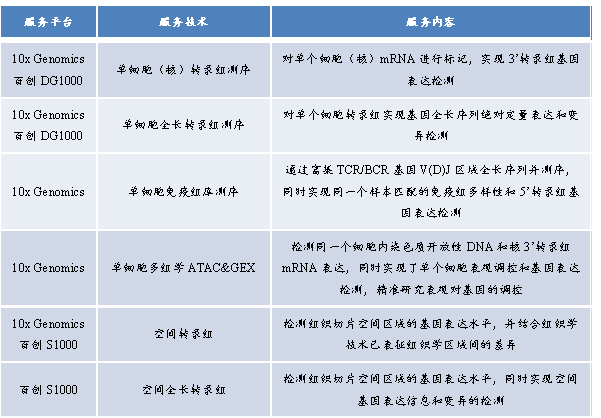
表1 百迈客单细胞空间多组学技术服务列表
如果您对我们的测序服务及平台感兴趣,欢迎点击下方按钮联系我们,我们将免费为您设计文章思路方案。
参考文献
- Pai JA, Satpathy AT. High-throughput and single-cell T cell receptor sequencing technologies. Nat Methods. 2021;18(8):881-892. doi:10.1038/s41592-021-01201-8
- Rubio-Perez C, Planas-Rigol E, Trincado JL, et al. Immune cell profiling of the cerebrospinal fluid enables the characterization of the brain metastasis microenvironment. Nat Commun. 2021;12(1):1503. Published 2021 Mar 8. doi:10.1038/s41467-021-21789-x
- Park JE, Botting RA, Domínguez Conde C, et al. A cell atlas of human thymic development defines T cell repertoire formation. Science. 2020;367(6480):eaay3224. doi:10.1126/science.aay3224.
- Wang Z, Xie L, Ding G, et al. Single-cell RNA sequencing of peripheral blood mononuclear cells from acute Kawasaki disease patients. Nat Commun. 2021;12(1):5444. Published 2021 Sep 14. doi:10.1038/s41467-021-25771-5.
- Gong L, Kwong DL, Dai W, et al. Comprehensive single-cell sequencing reveals the stromal dynamics and tumor-specific characteristics in the microenvironment of nasopharyngeal carcinoma. Nat Commun. 2021;12(1):1540. Published 2021 Mar 9. doi:10.1038/s41467-021-21795-z.
- Shi K, Li H, Chang T, et al. Bone marrow hematopoiesis drives multiple sclerosis progression. Cell. 2022;185(13):2234-2247.e17. doi:10.1016/j.cell.2022.05.020.
- Krishna C, DiNatale RG, Kuo F, et al. Single-cell sequencing links multiregional immune landscapes and tissue-resident T cells in ccRCC to tumor topology and therapy efficacy. Cancer Cell. 2021;39(5):662-677.e6. doi:10.1016/j.ccell.2021.03.007.
- Cao Y, Su B, Guo X, et al. Potent Neutralizing Antibodies against SARS-CoV-2 Identified by High-Throughput Single-Cell Sequencing of Convalescent Patients’ B Cells. Cell. 2020;182(1):73-84.e16. doi:10.1016/j.cell.2020.05.025.
- He J, Xiong X, Yang H, et al. Defined tumor antigen-specific T cells potentiate personalized TCR-T cell therapy and prediction of immunotherapy response. Cell Res. 2022;32(6):530-542. doi:10.1038/s41422-022-00627-9.







 京公网安备 11011302003368号
京公网安备 11011302003368号