肝脏在人类生理中起着至关重要的作用,其具有独特的再生能力可以修复急性损伤以维持其正常生理功能。然而肝功能障碍可能导致多种危及生命的疾病,肝癌是全球癌症死亡率第二高的癌症,在我国发病率和死亡率分别位居第四位和第三位。肝细胞癌(hepatocellular carcinoma,HCC)最为常见,占原发性肝癌的70%~90%。肝癌的治疗失败、耐药性和高死亡率与恶性细胞的异质性以及复杂的肿瘤微环境(TME)密切相关。因此,了解肝癌的细胞图谱和分子组成,对于肿瘤生物学研究和开发新的治疗策略至关重要。单细胞测序是研究肿瘤微环境中细胞成分及其相互作用的有力工具,已被广泛应用于大量肿瘤异质性研究。目前,单细胞测序技术已经为肝癌肿瘤微环境、肿瘤发生发展机制、克隆进化、免疫治疗等方面提供了深入见解。
下面小编将从研究进展、应用方向、百迈客项目经验三个方面分别进行介绍,总结出单细胞转录组测序技术在肝癌中的代表性文章,希望为各位老师提供一些新的研究思路。
研究进展
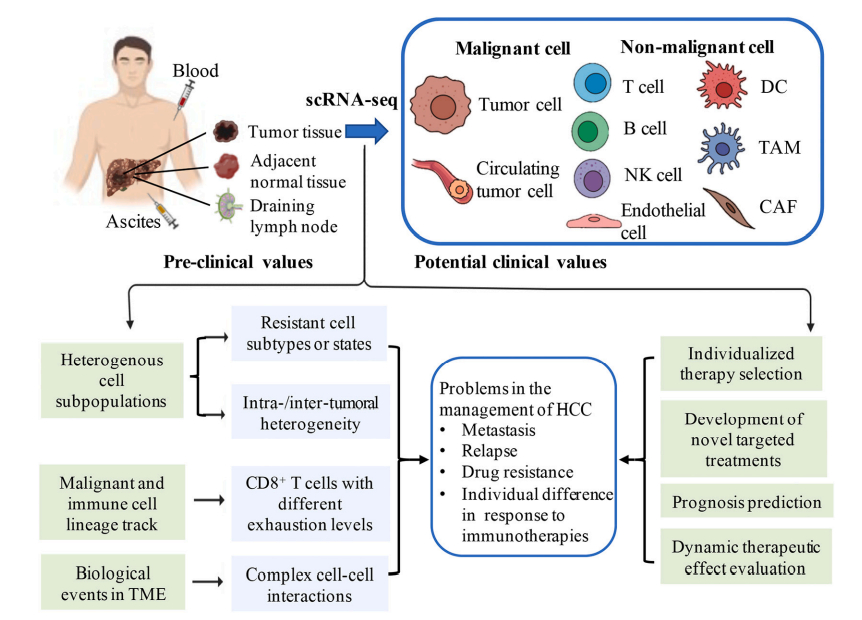
单细胞测序技术自2009年问世以来,在研究人员和临床医生中越来越受欢迎。与bulkRNA-seq相比,scRNA-seq最显著的优势在于对肿瘤异质性的详细描述,包括HCC在内的许多恶性肿瘤的棘手问题。scRNA-seq绘制了单个肝癌细胞的基因表达图谱,并确定了容易被忽视的耐药亚群的特征,尤其是在CSC中。肿瘤间异质性(ITH)阻碍了HCC治疗结果的改善。同时,scRNA-seq通过绘制免疫细胞的综合景观来实现肿瘤免疫。对于HCC患者,T细胞、B细胞、NK细胞、TAM和DC已被鉴定并具有特征基因。几种新发现的细胞亚型,例如MAIT,DPT细胞和LAMP3+ DCs可能为开发新的靶向免疫疗法带来新思路。此外,肿瘤免疫微环境不是静止的,单细胞分析有助于揭示多种免疫细胞亚型的起源和动态转变。在各种肿瘤浸润淋巴细胞和骨髓细胞中,CD8+T细胞的发育轨迹已得到充分研究。结合scRNA-seq、单细胞TCR测序分析可能有助于评估新抗原特异性、细胞毒性和异质T细胞亚群的进化连通性。此外,针对生物事件的治疗有利于CTC存活,例如EMT和Treg募集,在控制HCC血源性转移和肝移植受者复发方面显示出巨大潜力。通过scRNA-seq除了鉴定肝癌恶性和非恶性细胞、细胞亚群和/生物标志物深入剖析HCC异质性,也可以为个体化联合治疗提供理论依据。【1】
应用方向
1、绘制肝癌异质性图谱
案例1、单细胞转录组测序揭示了HBV相关肝细胞癌的免疫抑制图谱和肿瘤异质性【2】
标题:Single-cell RNA sequencing shows the immunosuppressive landscape and tumor heterogeneity of HBV-associated hepatocellular carcinoma
期刊名称:Nat Commun
影响因子:12.121
发表日期:2021年6月
样本设计:8例HCC患者的肿瘤组织
研究内容:本研究通对HBV 相关人类肝细胞癌 (HCC) 患者进行单细胞测序,研究发现肿瘤相关巨噬细胞抑制肿瘤 T 细胞浸润,Treg细胞又会进一步使肿瘤浸润性 T 细胞和 NK 细胞因行使天然的肿瘤免疫功能进一步处于耗竭状态。此外,研究发现,TIGIT-NECTIN2 相互作用调节免疫抑制环境,在HCC 小鼠模型中敲除敲低Nectin2会持续诱发肿瘤变小、恢复 T 细胞浸润并减少T 细胞耗竭,进一步证明TIGIT-NECTIN2靶向治疗HCC的潜力。
案例2、单细胞转录组学揭示了肝癌中肿瘤内异质性和干细胞相关亚群的图谱【3】
标题:Single-cell transcriptomics reveals the landscape of intra-tumoral heterogeneity and stemness-related subpopulations in liver cancer
期刊名称:Cancer Lett
影响因子:7.36
发表日期:2019年6月
研究内容:根据EPCAM表达,HCC 单细胞显示出两个不同的主要细胞群。在EPCAM +细胞群中多个癌基因表达上调,另外EPCAM +细胞群中还存在一个CD24 + /CD44 +的稀有细胞亚群,可能是新的干细胞相关亚型,CTSE是该群细胞中上调最多的特征基因。敲除CTSE显著降低了体外肿瘤细胞的自我更新能力和体内致瘤性能力, CTSE的干性作用通过裸鼠体内致瘤性测定得到进一步证实。研究表明单细胞基因组是描绘 HCC 肿瘤异质性的有利工具,可以鉴定到稀有的细胞亚群,长远来看能更好的指导精准医疗。
案例3、单细胞测序揭示肝癌免疫微环境的动态特征【4】
标题:Landscape and Dynamics of Single Immune Cells in Hepatocellular Carcinoma
期刊名称:cell
影响因子:38.637
发表日期:2019年8月
样本设计:16例肝癌(HCC)患者癌、癌旁、淋巴结、血液和腹水样本,分选CD45+细胞
研究内容:本研究发现免疫细胞类型表现出不同的组织偏好性,T 细胞中,包含调节型 T 细胞、耗竭型CD8+ T细胞和增殖型 T 细胞,主要在肿瘤中富集,髓系细胞主要在腹水中富集。腹水是肝癌患者常见的病理现象,其产生与肝癌预后不良有关,然而腹水中的免疫细胞组成及其与肝癌的联系尚不清楚。研究者为了探究腹水中细胞的潜在起源,将腹水的免疫细胞与其他组织细胞进行比对分析,发现腹水中的淋巴细胞和髓系细胞来源明显不同,淋巴细胞主要映射到血液、肿瘤和邻近肝脏中,而髓系细胞主要定位于肿瘤组织。基于线粒体突变的谱系追踪结果显示,肿瘤组织和腹水中的细胞具有共同谱系。随后作者研究了腹水和其他组织中巨噬细胞的关系,发现巨噬细胞存在从肿瘤到腹水迁移的过程。作者对不同组织部位的免疫细胞进行综合表征分析,探究了免疫细胞在癌症环境中的动态特性,从而揭示TME、LN和腹水中髓系细胞和淋巴细胞的差异谱系和迁移关系。
案例4、肿瘤细胞生物多样性驱动肝癌微环境重编程【5】
标题:Tumor Cell Biodiversity Drives Microenvironmental Reprogramming in Liver Cancer
期刊名称:Cancer Cell
影响因子:26.604
发表日期:2019年12月
样本设计:9例肝癌(HCC)患者和10例肝内胆管癌(iCCA)患者
研究内容:本文构建了19名HCC和iCCA患者的单细胞转录组图谱,并开发了一种测量与预后相关的 ITH 程度的方法。研究发现肿瘤内和肿瘤间的恶性细胞以及肿瘤微环境存在不同程度的异质性。VEGFA 对CAF、TAM和TECs具有特异性,对T细胞不具有特异性,同时,VEGFA主要在恶性细胞中表达。VEGFA是缺氧诱导因子 1-α (HIF1A) 的直接靶标,HIF1A 是感知缺氧的关键因素,缺氧可直接诱导HIF1A转录及其蛋白水平,从而激活其下游的缺氧信号。表明恶性细胞VEGF 表达与 TME 重编程有关,从而促进有利于肿瘤进展的免疫抑制环境。此研究表明,测量肿瘤细胞的生物多样性可能是一种可行的方法,可以确定肿瘤进化的共同特征,以预测肝脏肿瘤的侵袭性。研究为免疫检查点抑制剂和抗 VEGF 的联合治疗以提高治疗效果提供了基本原理。
2、肝癌发生发展机制(肿瘤-免疫循环系统)
案例5、先天淋巴细胞ILC2通过 CXCL2-中性粒细胞诱导的免疫抑制促进 HCC 进展【6】
标题:Group-2 Innate Lymphoid Cells Promote HCC Progression Through CXCL2-Neutrophil-Induced Immunosuppression.
期刊名称:Hepatology
影响因子:14.679
发表日期:2021年11月
样本设计:1个HCC患者及正常肝脏样本,分选LIN-造血细胞用于单细胞测序
研究内容:固有淋巴细胞已经在不同类型的肿瘤中被鉴定到,它是一类没有重组抗原特异性的先天免疫细胞,主要分为ILC1、ILC2和ILC3家族。目前研究较多的ILC2因其没有T细胞和B细胞接受体,因此其功能以上下游依赖的方式变化,尽管在一些肝脏疾病中有被研究,但ILCs在肝癌中的具体角色并不清楚。此文章中作者通过FACS和scRNA技术发现了ILCs在HCC病人中显著的富集,并且和肿瘤的反复、整体的生存率都有关系。通过流式细胞仪鉴定到了一群HCC产生的ILC2s,它们的杀伤细胞凝集素样亚家族G成员1表达降低,同时肿瘤细胞里E-钙粘蛋白的减少会进一步减少KLRG1 ,此外KLRG1-ILC2显示趋化因子的产生增加,包括C-X-C基序趋化因子(C-X-C基序)配体(CXCL)-2和CXCL8,它们反过来招募中性粒细胞形成免疫抑制剂,导致肿瘤恶化。因此,在小鼠肝癌模型中,恢复ILC2s中的KLRG1、抑制ILC2s中的CXCL2或耗尽中性粒细胞可抑制肿瘤进展,总体表明HCC相关的ILC2s是一种促进肿瘤发展的免疫调节细胞类型,靶向这些ILC2s可能催生HCC的新疗法。
案例6、肝癌中的肝星状细胞通过产生生长分化因子15促进肿瘤生长【7】
标题:Hepatic Stellate Cells in Hepatocellular Carcinoma Promote Tumor Growth Via Growth Differentiation Factor 15 Production
期刊名称:Gastroenterology
影响因子:17.373
发表日期:2020年12月
样本设计:12例HCC患者肿瘤组织和非肿瘤组织
研究内容:大部分的HCC由肝纤维化发展而来,而HSCs则作为成纤维细胞产生大量的基质蛋白,在肝纤维化中扮演了重要的角色。本文中作者通过对HSC特异性缺陷的Atg-7和生长分化因子缺陷的(GDF-15)小鼠进行链脲霉素处理高脂饮食。同时做了LX-2 HSC细胞系和人肿瘤细胞混合培养。通过单细胞测序发现,小鼠模型中,GFAP-Atg7KO比野生型小鼠的肿瘤数量少并且小。LX-2和肝癌细胞的混合培养中,LX-2的细胞自噬被促进,Atg7-KO则能减弱LX-2细胞自噬和肝癌细胞生长,同时Atg7-KO可减弱LX-2细胞自噬和肝癌细胞生长也出现了同样的现象。RNA测序发现LX-2和HepG2共培养后GDF15表达增加,GDF15KO的LX-2细胞系没有发现癌症细胞的促进增殖,在脂肪肝炎的模型中,GDF15的缺乏会减少肿瘤的大小。综上所述在HCC微环境中,以自噬依赖方式产生GDF15的HSC可能与肿瘤发生有关。
3、预后标志物及治疗靶点开发
案例7、肝癌内皮细胞重编程促进免疫抑制性巨噬细胞的产生【8】
标题:Onco-fetal Reprogramming of Endothelial Cells Drives Immunosuppressive Macrophages in Hepatocellular Carcinoma
期刊名称:cell
影响因子:38.637
发表日期:2020年10月
样本设计:14名HCC患者(5 名 HepB -和 9 名 HepB +)及1例健康捐赠者的肝脏样本,估计胎龄 (EGA) 为16 周和 21 周的胎儿肝脏样本
研究内容:众所周知,肿瘤细胞能够概括早期胎儿发育的特征,包括获得干细胞样特征、EMT(上皮-间质转化)和癌胎蛋白的表达。研究绘制了人类肝脏从胚胎发育到肝癌细胞的单细胞图谱,发现肝细胞癌肿瘤微环境具有明显的胚胎样重编程特征,并在跨物种比较分析中发现小鼠胚胎,胚胎肝脏以及肿瘤巨噬细胞之间存在显著的相似性,表明胚胎肝脏发育与HCC生态系统之间存在一个共享程序,即胎-瘤重编程。同时,研究揭示了VEGF/NOTCH信号在维持HCC免疫抑制的胎-瘤生态系统中的重要作用。VEGF/NOTCH介导的免疫抑制胎-瘤系统的概念不仅为癌症治疗干预提供了新的靶点,而且还可以作为潜在的生物标志物用于计划使用免疫治疗的HCC患者,研究也为鉴定和理解其他癌症中的类似机制开辟了道路。
案例8、单细胞测序揭示早期复发肝癌特征性免疫图谱【9】
标题:Single-cell Landscape of the Ecosystem in Early-relapse Hepatocellular Carcinoma
期刊名称:cell
影响因子:38.637
发表日期:2021年1月
样本设计:12例原发肝癌和6例早期复发肝癌患者的肿瘤组织和癌旁组织,进行全长单细胞转录组测序,并采用2个独立的队列(第1队列,4例患者的配对原发肿瘤和复发肿瘤;第2队列,47例患者的配对原发肿瘤和复发肿瘤)对相关结果进行验证(见下图)。
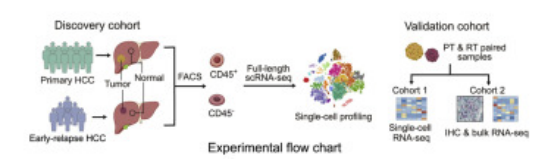
研究内容:本文构建了12例原发性肝细胞癌患者和6例早期复发肝细胞癌患者癌和癌旁的单细胞图谱,发现与原发性肝癌微环境相比,复发性肝癌呈现独特的免疫生态系统,即DC比例增加,Tregs减少,T细胞增殖减少,CD8+T细胞丰度更高。通过整合TCR克隆和Monocle分析,研究者确定了CD8+T细胞的分化路径。PT和RT样本中CD8+T细胞表现出相同的分化轨迹,但表现出明显不同的免疫和转录状态,与原发性肝癌样本(PT)相比,早期复发性肝癌样本(RT)中的CD8+T细胞耗竭信号的表达减少,表达免疫检查点基因的细胞比例减少,组织驻留基因增加,而共刺激和耗竭分子减少。同时,研究者发现免疫检查点基因CTLA4、HAVCR2和TIGIT在复发肿瘤的T细胞中表达降低,这表明针对这些标志物的检查点阻断方法可能对原发性肝癌有效,但对复发患者无效。综上所述,治疗原发性或复发性肝癌需要不同的治疗方法。
案例9、FABP5作为人肝细胞癌免疫代谢标志物的鉴定【10】
标题:Identification of FABP5 as an immunometabolic marker in human hepatocellular carcinoma
期刊名称:J Immunother Cancer
影响因子:9.913
发表日期:2020年7月
样本设计:20名HCC患者癌和癌旁样本,分选T细胞
研究内容:本文从HCC患者中分离CD3+CD45+T细胞并进行单细胞转录组测序,分析结果表明,肿瘤组织中存在多个耗尽的T细胞(Tex)群体,CD137 可识别并丰富 Tex,具有卓越的效应功能和增殖能力,这群细胞表达FABP5以及线粒体氧化代谢作用增强。抑制 FABP5 表达和线粒体脂肪酸氧化会损害富含 CD137 的 Tex 的抗细胞凋亡和增殖,这些观察结果已通过生成CD137 CART得到验证。118 例 HCC 患者的组织微阵列免疫组织化学染色显示肿瘤内 FABP5高CD8 +T 细胞浸润与总生存期和无复发生存期有关。118例HCC患者的组织微阵列免疫组织化学染色显示,肿瘤内FABP5高CD8+T细胞与总生存率和无复发生存率相关。结果表明,肿瘤微环境可以对 T 细胞功能施加代谢限制。CD137 是一种在某些 Tex 上高度表达的共刺激分子,它利用外源脂肪酸和氧化代谢来介导抗肿瘤免疫。免疫代谢标志物 FABP5 应在更大的纵向研究中进行研究,以确定它们作为 HCC预后生物标志物的潜力。
4、解析肿瘤耐药机制
案例10、晚期肝癌患者受益于派姆单抗:结果来自单臂 2 期试验【11】
标题:Hepatocellular carcinoma patients with high circulating cytotoxic T cells and intra-tumoral immune signature benefit from pembrolizumab: results from a single-arm phase 2 trial
期刊名称:Genome Medicine
影响因子:10.675
发表日期:2021年4月
样本设计:10名BLCL-C期患者派姆单抗治疗前后的PBMC样本
研究内容:本文对索拉非尼治疗失败后接受派姆单抗治疗的HCC患者的pbmc进行单细胞转录组测序,研究表明派姆单抗在索拉非尼治疗失败后总体缓解率为10%。在使用临床病理学特征的单变量分析中,女性、PD-L1 阳性和低中性粒细胞与淋巴细胞比 (NLR) 被确定为派姆单抗反应的促成因素。CTNNB1 的体细胞突变和 MET 的基因组扩增仅在无应答者中发现。通过 RNA 测序的转录谱确定,pembrolizumab 应答者表现出 T 细胞受体 (TCR) 信号激活与 MHC 基因的表达,表明 T 细胞细胞毒性水平增加。在对 10 个治疗前和治疗后外周血单个核细胞 (PBMC) 进行单细胞测序时,获得部分缓解或疾病稳定的患者表现出向细胞毒性 CD8+ T 细胞的免疫转变。综上,具有细胞毒性 T 细胞浸润的 HCC 患者,以及活跃循环 CD8+ T 细胞的增加和中性粒细胞相关标志物的下调,显著受益于派姆单抗治疗。
百迈客项目经验
肝脏是人体代谢和解读的器官,在体内发挥氧化、储存肝糖、合成分泌性蛋白合成等,肝脏也制造消化系统中之胆汁,人肝约有25亿个肝细胞。但是解离肝脏组织悬液并不简单,首先,肝脏代谢旺盛,离体后肝细胞无法进行正常的有氧糖酵解,细胞活力会迅速下降,另外,肝细胞的线粒体很多,每个细胞大约有1000个左右,遍布于胞质内。因此,很难得到符合单细胞测序要求的单细胞悬液。百迈客生物在肝脏组织单细胞悬液制备方面有丰度的实操经验,开发了独有的解离体系,下面来看实验结果:
实验结果

人肝癌样本,悬液背景干净,活性91.69%,结团率6%

人胆管癌样本,活性90.45%,结团率7.2%
Tips: 肝实质细胞经过解离后因为缺氧非常容易发生凋亡,导致占比很低,如果老师关注肝实质细胞的话,建议采用单细胞核悬液的方法。
如果您对我们的方案感兴趣,欢迎点击下方按钮联系我们,我们将免费为您设计文章思路方案。
参考文献
- Li, Xin-Yue et al. “Understanding initiation and progression of hepatocellular carcinoma through single cell sequencing.” Biochimica et biophysica acta. Reviews on cancer, vol. 1877,3 188720. 15 Mar. 2022
- Ho, Daniel Wai-Hung et al. “Single-cell RNA sequencing shows the immunosuppressive landscape and tumor heterogeneity of HBV-associated hepatocellular carcinoma.” Nature communications vol. 12,1 3684. 17 Jun. 2021
- Ho, Daniel Wai-Hung et al. “Single-cell transcriptomics reveals the landscape of intra-tumoral heterogeneity and stemness-related subpopulations in liver cancer.” Cancer letters vol. 459 (2019): 176-185.
- Zhang, Qiming et al. “Landscape and Dynamics of Single Immune Cells in Hepatocellular Carcinoma.” Cell vol. 179,4 (2019): 829-845.
- Ma, Lichun et al. “Tumor Cell Biodiversity Drives Microenvironmental Reprogramming in Liver Cancer.” Cancer cell vol. 36,4 (2019): 418-430.
- Xu, Xingyuan et al. “Group-2 Innate Lymphoid Cells Promote HCC Progression Through CXCL2-Neutrophil-Induced Immunosuppression.” Hepatology (Baltimore, Md.) vol. 74,5 (2021): 2526-2543.
- Myojin, Yuta et al. “Hepatic Stellate Cells in Hepatocellular Carcinoma Promote Tumor Growth Via Growth Differentiation Factor 15 Production.” Gastroenterology vol. 160,5 (2021): 1741-1754.
- Sharma, Ankur et al. “Onco-fetal Reprogramming of Endothelial Cells Drives Immunosuppressive Macrophages in Hepatocellular Carcinoma.” Cell vol. 183,2 (2020): 377-394.
- Sun, Yunfan et al. “Single-cell landscape of the ecosystem in early-relapse hepatocellular carcinoma.” Cell vol. 184,2 (2021): 404-421.
- Liu, Fangming et al. “Identification of FABP5 as an immunometabolic marker in human hepatocellular carcinoma.” Journal for immunotherapy of cancer vol. 8,2 (2020).
- Hepatocellular carcinoma patients with high circulating cytotoxic T cells and intra-tumoral immune signature benefit from pembrolizumab: results from a single-arm phase 2 trial.






 京公网安备 11011302003368号
京公网安备 11011302003368号