今天小编给大家分享一篇宏基因组在神经系统疾病研究中的应用,本研究通过宏基因组测序技术和代谢产物预测分析方法阐明了益生菌通过调节肠道微生物菌群的神经活性以缓解人类的压力和焦虑的左右机制。百迈客微生物产品部具有多年宏基因组研究经验,针对不同类型的样本均具有丰富的实验经验,对于提取困难样本还研发了微量建库技术(”无偏差”宏基因组微量建库:难提取样本的福音),此外宏基因组APP还提供40余项免费个性化分析内容,同时与代谢组多组学联合分析全新升级,包含普氏分析、相关性分析、随机森林等多项内容,为您提供全面的肠道菌群研究方案,欢迎各位老师前来咨询!
背景介绍
压力在人们的生活中无处不在,严重的时候会引起人类焦虑甚至抑郁。目前抑郁影响着全球3亿多人,每年有近80万人因抑郁自杀身亡。最近的研究已经证明压力会扰乱人类肠道微生物菌群的平衡,进而导致焦虑、抑郁等心理疾病。人类和肠道微生物的基因组沟通进化,导致肠道、肠道神经系统和中枢神经系统之间存在复杂的互作。肠道菌群参与各种激素、神经递质的合成、释放,其紊乱会导致压力、焦虑、抑郁、帕金森疾病和阿尔兹海默症。人类需要维持肠道微生物菌群平衡,从而保证身体健康。足量的益生菌可以与肠道菌群相互作用,使宿主保持心理健康。在这个过程中,益生菌调节宿主的肠道微生物群落,及某些神经活性化合物的合成、释放。因此提出了基于益生菌治疗某些神经和神经退行性疾病的疗法。高质量的人类和动物相关研究表明,肠道微生物群在许多与压力相关的情况中发挥着重要作用。然而,肠道微生物组在压力相关条件下的因果关系和贡献程度尚不清楚,本文旨在从肠道微生物组的角度阐明这种机制。
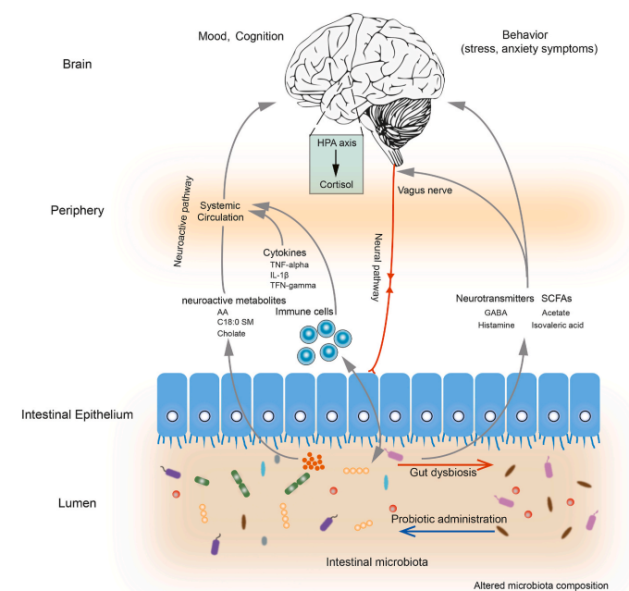
中文标题:食用益生菌可调节肠道微生物菌群的神经活性以缓解人类的压力和焦虑
英文标题:Probiotic consumption relieved human stress and anxiety symptoms possibly via modulating the neuroactive potential of the gut microbiota
期刊:Neurobiol Stress (IF:5.441)
发表时间:2021年1月
材料与方法
实验设计:实验组包含43名受试者,每日口服Lactobacillus plantarumP-8(2 克;2×10^10 CFU/小袋/天);对照组包含36名受试者,每日口服安慰剂麦芽糊精,第0周和第12周收集粪便样本。
研究技术:宏基因组测序分析 + 代谢产物预测分析(Melonnpan)
结果
1、 有压力的成人的肠道微生物菌群的基因组特征
获得的 589 个物种水平的基因组(SGB: species-level genome bins) 可表示宏基因组数据 78.56 ± 6.46%的数据(图 1a)。 SGBs分布在13门23纲30目49科91属341种,大多数 SGB 被分配到厚壁菌门 (57.72%),其次是拟杆菌门 (14.60%)、放线菌门 (12.56%) 和变形菌门 (8.15%)。50 个 SGB 在物种水平上仍未绘制和未表征,代表未培养物种。这些未培养的物种主要属于三个门,即厚壁菌门 (72%)、拟杆菌门 (11.67%) 和变形菌门 (4%) (图1b 和c)。
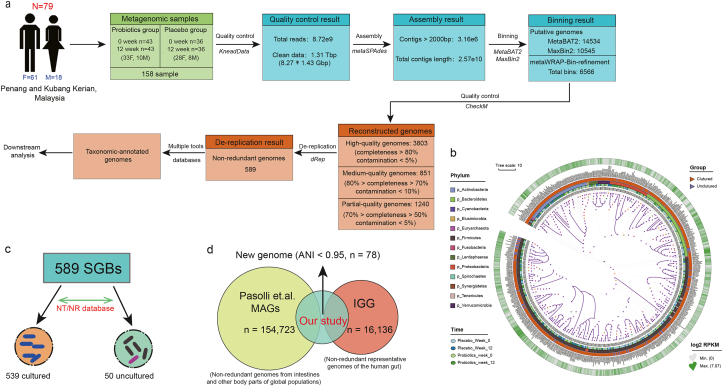
(a) 宏基因组组装、分箱、构建和去重复的流程中产生了总共 589 个高质量SGB。(b) 589 个高质量 SGB 的系统发育位置。树的热图显示了在实验期间 SGB 的每千碱基读取数 (RPKM) 的 log2 倍变化。(c) 在 589 个 SGB 中,分别有 539 个和 50 个之前培养过和未培养过。(d) 78 个SGB的新颖性。通过与 IGG 数据库(16,136 个非冗余代表性人类肠道基因组的集合)和 Pasolli et al. MAGs 数据库(来自全球人口肠道和其他身体部位的 154,723 个非冗余基因组的数据集)的交叉比较发现都不匹配 (<95% average nucleotide similarity) 。
2、益生菌调节肠道微生物群组成
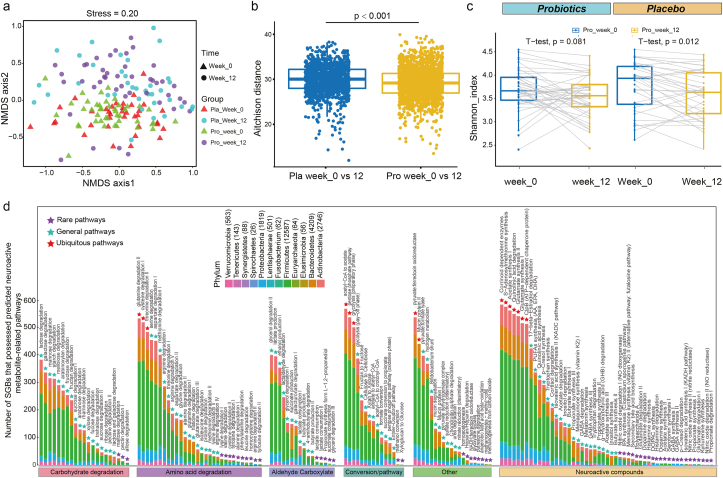
为了评估益生菌对有压力的成人肠道微生物群的影响,NMDS分析结果表明第0周和第12周的微生物群结构存在明显差异。ANOSIM 进一步分析发现益生菌组和安慰剂组在第0周没有显著差异(R = 0.003,P = 0.354),但在第12周显示出显著差异(R = 0.041,P = 0.028)。而是,安慰剂接受者在第0周和12周之间的 Aitchison 距离差异显著大于益生菌接受者(P = 0.001;图2b)。此外,与第0周相比,安慰剂接受者的Shannon多样性指数在第 12 周显著下降(P < 0.05),在益生菌接受者中没有该显著下降(图2c)。上述这些结果共同表明,尽管 P-8 组和安慰剂组在12周试验后均表现出alpha/beta多样性的变化,但益生菌治疗导致的肠道微生物群多样性和结构的变化较小。
“核心菌群”由稳定的人体肠道关键微生物组成,与人体健康息息相关。本研究确定了13个核心SGBs。通过比较益生菌处理前后的益生菌组中所有SGB的丰度,确定了差异丰度的SGB。6个核心SGBs 和 17个非核心SGBs 的丰度随着益生菌处理前后,显著变化;SIMPER 分析发现,这些 SGBs 加起来占微生物群落变异的 13.65%。同时,安慰剂组中1个核心SGB和12个非核心SGB的丰度发生显著变化,共同占微生物群落变异的4.85%。此外,在第0周,安慰剂组和益生菌组之间的10个 SGB(例如,B. longum、Megamonas funiformis、Subdoligranulum sp. 60_17、Bacteroides sp . 和三个未培养物种)显示没有显著差异。但它们在第12周变得显著差异,占微生物群落变异的5.41%。SIMPER 分析的结果表明,益生菌/安慰剂处理或不同时间点之间的微生物群落变化主要是微生物群落的整体变化,而不是个体优势物种的变化。
3、益生菌调节肠道微生物群相关的神经活性化合物
使用Valles-Colomer 等人开发的基于模块的分析框架,预测我们样品的神经活性化合物。分别有32个和 17个差异丰度模块与神经活性合成和降解相关(图 3a 和 b)。根据其代谢途径的潜力,合成/降解相关的 GBMs 可以分为六个功能亚组。 仅在第12周发现,两组之间编码合成相关的 GBMs(SGBMs)的总丰度存在显著差异(P < 0.001)。此外第 12 周,编码SGBM I(氨基酸和衍生物合成)和SGBMs IV(SCFAs合成)的SGBs在时P-8组和安慰剂组之间差异很大(P < 0.01)。此外,在第12周时,益生菌组中参与SGBMs II(神经递质I合成;含有 γ-氨基丁酸 (GABA) 的三种合成途径)的SGBs丰度较高。在第12周,益生菌组中编码 DGBMs II(神经递质I降解)和 DGBMs III(神经递质II降解)的 SGBs的丰度在第0周和第12周之间显著差异。DGBMs的其他亚组,例如DGBMs I(氨基酸降解)、DGBMs IV(SCFAs 降解)和DGBMs VI(维生素降解),在试验后仅发生了轻微波动。
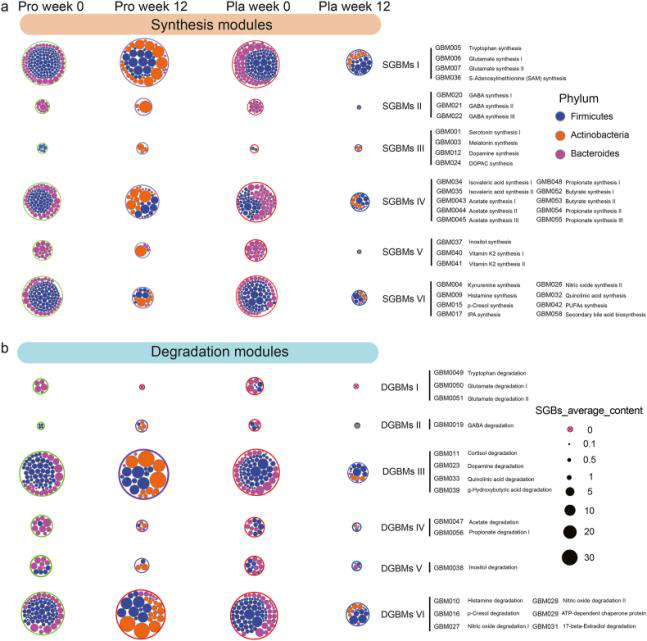
门级肠脑模块 (GBM) 的分布。显示了益生菌 (pro) 和安慰剂 (pla) 组中不同类型的 (a) 合成相关的GBM (SGBM) 和 (b) 降解相关的GBM (DGBM) 的分布及其在门水平上的组成。已鉴定的 SGBMs/DGBMs 根据其代谢物合成的预测功能分别分为六组(I 至 VI),并将它们相关的物种水平基因组箱(SGBs)分配给相应的门。外圈的大小代表相应 SGB 的平均丰度。
4、食用益生菌调节预测的肠道神经代谢组
MelonnPan 被用于寻找 SGB与潜在神经代谢物之间的相关性。预测了80种代谢物。其中,脱氧胆酸、谷氨酸盐和胆酸盐是最丰富的三种代谢物。通过 NMDS 分析评估受试者预测的粪便代谢组的变化,在不同时间点收集的样本形成了清晰的聚类(stress= 0.0862;图4a)。Procrustes 分析发现微生物组和代谢组谱之间存在正相关性(correlation= 0.386;P = 0.001;图4b),表明样品的代谢物输出与产生它的SGB一致。P-8组和安慰剂组在12周试验后肠道代谢物谱发生显著变化(P < 0.001;比较每组第0周和第12周的数据),而 ANOSIM 发现在第0周两组之间的代谢物谱没有显著差异。在 P-8 组和安慰剂组中分别鉴定出41和12种不同丰度的代谢物。在第0周和第12周之间,这些丰度差异的代谢物,在丰度水平上显著差异。在临床试验后,发现一些代谢物具有相同的变化趋势,例如,在第12周,两组的泛酸、烟酸、石胆酸盐水平显著降低,同时预测的胞嘧啶水平显著增加( P < 0.05 )。这些变化可能不是益生菌治疗所特有的。相比之下,益生菌接受者的胆酸盐、花生四烯酸、肌酸、苏式鞘氨醇、赤藓糖酸和C18:0鞘磷脂的平均预测丰度显著增高(P < 0.05;图4c),代表食用益生菌会发生一些神经相关代谢物的特异性变化。
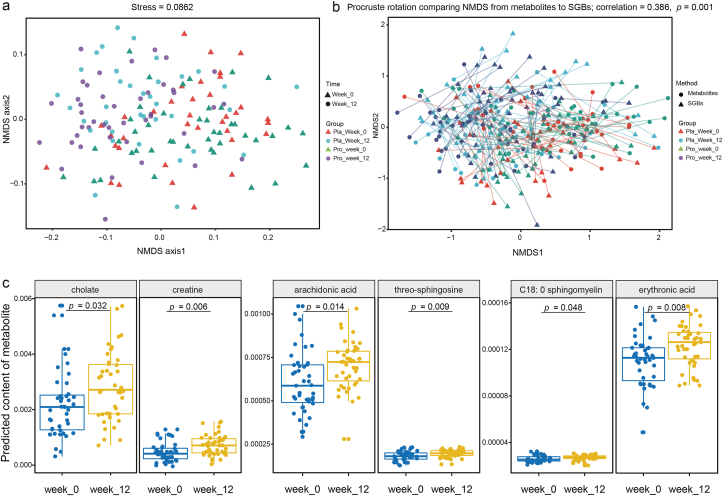
益生菌 (pro) 和安慰剂 (pla) 组在两个时间点的预测肠道代谢组之间的差异。(a) 非度量多维标度(NMDS,Bray-Curtis 相似性指数)和(b)对在第 0 周和第 12 周对两组受试者的预测微生物组和代谢组进行了Procrustes 分析,表明显示微生物组学和代谢组学特征之间的正协同性(correlation = 0.386;P = 0.001)。(c) 益生菌组第 0 周和第 12 周之间预测的差异神经活性代谢物。p 值经 FDR 法校正,阈值 P < 0.05 表示显著。
结论
本研究从肠道微生物菌群的角度阐明益生菌L.plantarum P-8 在缓解成人的压力、焦虑相关症状方面的机制。研究结果表明,益生菌诱导的肠道微生物菌群与人们的压力、焦虑之间存在潜在联系,肠脑轴(gut-brain axis)能够参与缓解压力相关的症状。益生菌的有益效果不仅取决于微生物多样性的变化,还依赖于肠道宏基因组在SGB和功能基因水平的调节。
文献下载:
https://international.biocloud.net/zh/article/detail/33511258
(复制链接到浏览器下载原文,如果没有云平台账号需要先注册)





 京公网安备 11011302003368号
京公网安备 11011302003368号