(或点击二维码直接报名)

PART ONE
论文内容详解
威宁黑麦是我国的栽培黑麦早抽穗优良品种,具有抗白粉病和条锈病的能力。为了解析黑麦优良性状的遗传和分子基础,促进黑麦及相关作物的基因组和育种研究,作者对威宁黑麦进行了基因组测序和分析。
- 基因组装与注释
- 转座子分析
- 黑麦基因组进化和染色体共线性研究
- 基因重复及其对淀粉生物合成基因的影响分析
- 黑麦种子贮藏蛋白(SSP)基因位点的解析
- 转录因子(TF)及抗病基因的注释和分析
- 早抽穗性状相关基因表达特征的研究
- 黑麦驯化过程中染色体区域和基因座的挖掘
流式预估黑麦基因组大小约为7.86 Gb,结合PacBio、Illumina、Hi-C、遗传图谱、BioNano光学图谱等技术进行基因组组装。最终组装7.74 Gb基因组(为预估基因组大小的98.47%),scaffold N50 为1.04 Gb,并将93.67%的序列挂载至7条染色体上(图1)。黑麦中每条染色体基因组大小均在1G左右(2R、3R、4R、6R、7R(~1Gb);1R(0.94097 Gb)、5R(0.99891 Gb) ),比乌拉尔图小麦(T. urartu;Tu;AA型)、节节麦(Aegilops tauschii;Aet;DD型)、野生二粒小麦(T. turgidum ssp. dicoccoides;WEW;AABB型)、普通小麦(Ta)和大麦(Hv)等复杂的麦类中的单条染色体基因组均要大。超大的基因组及染色体,对黑麦基因组组装,特别是染色体挂载带来了巨大的挑战。
将组装结果与两个冬季黑麦品种(Lo7和Lo225)构建的染色体连锁图相比,威宁黑麦1R至7R物理图具有较高的一致性。在先前报道的Lo7的pyro-sequencing reads中97.45%可以定位到威宁基因组,平均序列同源性为97.71%,平均序列覆盖率为97.27%。LAI值为18.42,远高于先前发表的小麦和大麦基因组的LAI值。BUSCO评估结果为96.74%。并注释了86,991个蛋白编码基因。尽管黑麦基因组非常复杂,通过以上评估结果说明,本次研究构建了一个高质量的威宁黑麦基因组。
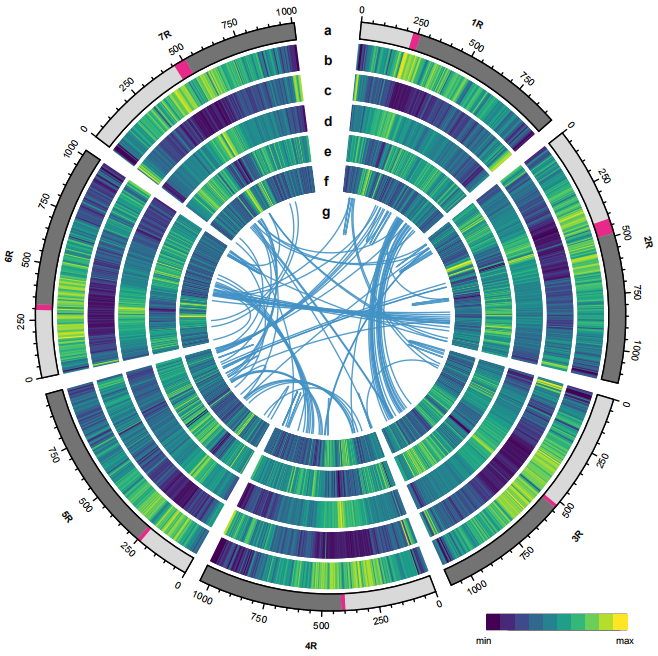
图1 黑麦基因组特征
威宁黑麦基因组中90.31%被注释为转座子(TE),共包含537个家族的2,671,941个成员,这些TE的含量明显比普通小麦 (84.70%), 乌拉尔图小麦 (81.42%), 节节麦 (84.40%), 野生二粒小麦 (82.20%)以及大麦 (80.80%)更高。其中长末端重复反转录转座子(LTR-RTs)是主要的转座子,在注释的TEs中占 84.49%。
与乌拉尔图小麦、节节麦及大麦的LTR-RTs进行比较发现:(1)Gypsy是威宁黑麦基因组扩张的主要原因之一(Fig. 2a),并且有3个LTR-RT家族(Daniela, Sumaya, Sumana)在威宁黑麦中特异扩张,其中Daniela的占比最高 (Fig. 2b)。(2)威宁黑麦中完整的LTR-RTs插入时间存在独特的双峰分布(Fig. 2c),最近一个扩增峰出现在50万年前,另出现在1.7 百万年(MYA)左右(与大麦相同) (Fig. 2c)。(3)这种双峰分布模式由Gypsy RTs的扩增主导(Fig. 2d)。
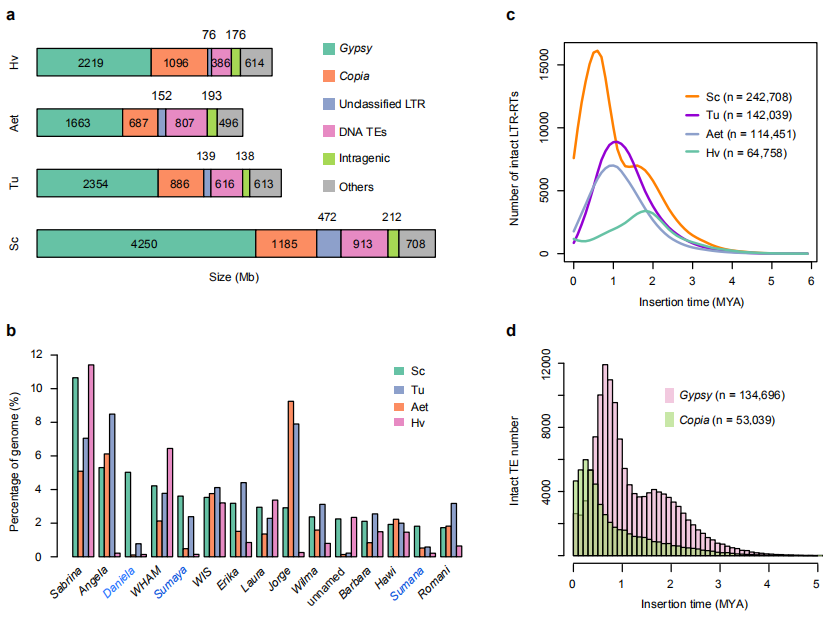
图2 黑麦中转座子分析
通过比较威宁黑麦、乌拉尔图小麦、节节麦、普通小麦(亚基因组TaA、TaB和TaD)、大麦、水稻Os(Oryza sativa ssp. japonica)、二穗短柄草Bd(Brachypodium distachyon)、玉米Zm(Zea mays)、高粱Sb(Sorghum bicolor)、谷子Si(Setaria italica)基因组,共找到2517个单拷贝同源基因。通过对单拷贝基因组构建进化树和计算分化时间发现,在大麦和小麦分化后(15MYA)黑麦和二倍体小麦发生了分化(9.6 MYA) (Fig. 3a)。
作者以水稻为祖先参考基因组,研究了威宁黑麦的染色体进化。威宁黑麦与水稻共鉴定出23个大的共线性区,包含10949对同源基因,可推断出祖先染色体片段在1R到7R之间的排列(图3b):(1)3R来源于一条古老的染色体AGK1/Os1,该染色体的一段易位到6RL;(2)1R和2R分别由两条祖先染色体组成,1R与AGK10/Os10嵌套插入AGK5/Os5有关,2R与AGK7/Os7嵌套插入AGK4/Os4有关;(3)4R, 5R, 6R,7R是通过复杂易位从至少三条祖先染色体上获得的(图3b)。
在威宁黑麦基因组与普通小麦3个亚基因组的比较中,1R、2R和3R分别与小麦1、2和3组染色体完全共线。在4R中发现与4A/4B/4D、7A/7B/7D或6A/6B/6D部分共线性的三个区域。5R与5A完全共线,与5B、5D部分共线是由于易位的4B或4D片段在5BL或5DL的长臂融合(图3c)。在6R中,观察到3个区域与6A/6B/6D、3A/3B/3D或7A/7B/7D部分共线。这些数据将有助于黑麦在禾本科比较基因组学研究以及黑麦与普通小麦杂交研究中的应用。
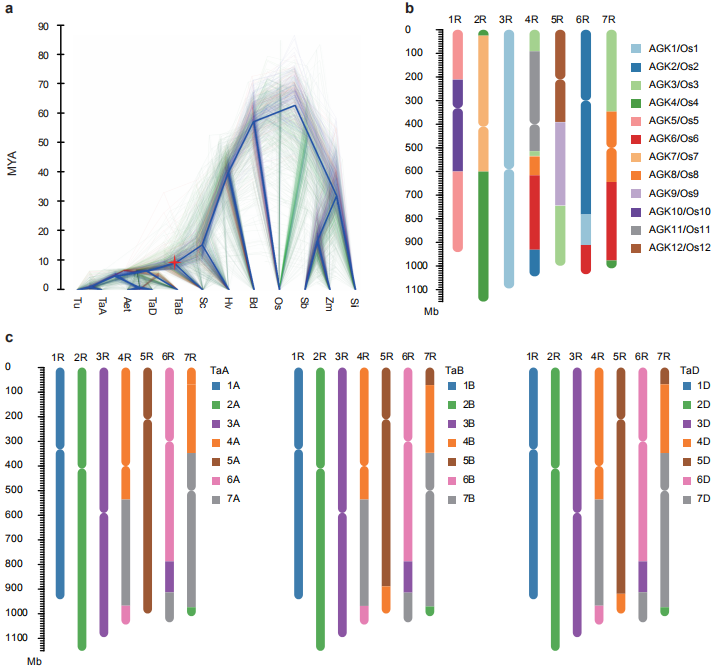
图3 黑麦基因组进化及染色体共线性分析
作者在威宁黑麦中检测到4217个单拷贝基因、23753个分散重复基因 (DDGs)、6659个近端重复基因 (PDGs)、7077个串联重复基因(TDGs)和1866个片段重复基因。转座重复基因(TrDGs)由TE活性诱导的,它们是DDGs的主要组成部分。作者以大麦为参考,在威宁黑麦中鉴定出10357个TrDG,远远大于以相同方式计算的乌拉尔图小麦(7145)和节节麦(7351)中TrDG的数量(图4b)。威宁黑麦所特有的TrDG(5926)也比乌拉尔图小麦(3513)和节节麦(3327)所特有的TrDG更多(图4b)。
接下来作者研究了黑麦淀粉生物合成相关基因(SBRGs)中的基因复制。研究发现这些重复类型在黑麦淀粉生物合成相关基因(SBRGs)中普遍存在,并且不同的SBRG的复制基因之间往往表现出表达差异,说明不同类型的基因复制可以丰富黑麦基因在重要生物过程中的遗传多样性(图4c),这些黑麦SBRGs的新变化可能为调控植物淀粉生物合成和性质提供新的酶活性,因此解析全套黑麦SBRGs有利于提高黑麦的产量潜力和营养品质。
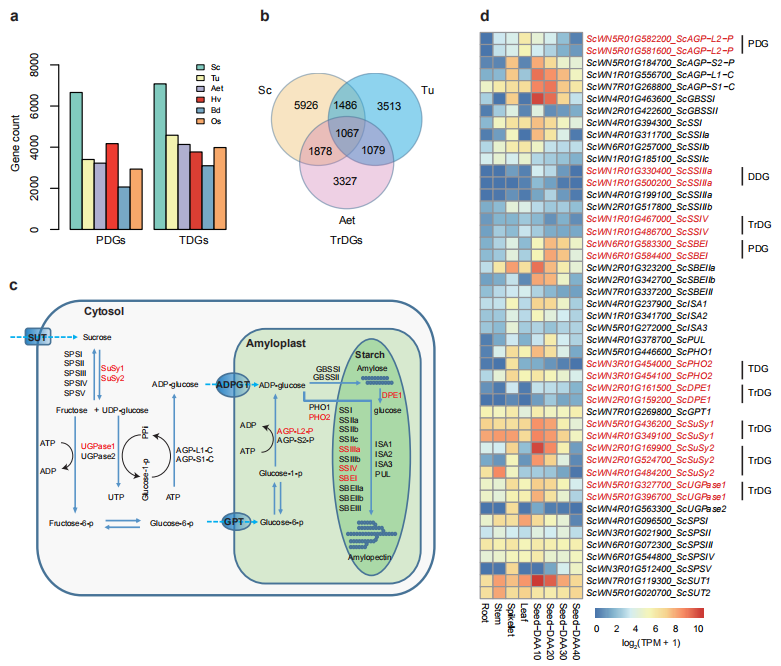
图4 黑麦基因重复及其对淀粉合成相关基因多样性的影响
与小麦和大麦相似,黑麦在胚乳组织中积累了丰富的储存蛋白SSPs。作者利用威宁基因组组装技术对黑麦SSP基因座进行了分析。
在威宁黑麦中未发现小麦低分子量麦谷蛋白亚基(LMW-GSs)或大麦B-hordein的同源序列(图5b),表明在黑麦进化过程中携带这些基因的染色体片段缺失,这可能是1BL1RS易位系小麦品种中,品质受影响的主要原因。并且在威宁黑麦基因组中未发现α-醇溶蛋白基因,这说明小麦及其近缘种的α-醇溶蛋白(α-gliadin)基因可能在小麦和黑麦分化之后进化产生的。这些SSP分析结果阐明了黑麦碱基因座的结构和组成,这将有助于进一步研究黑麦、小黑麦和小麦的加工和营养品质。
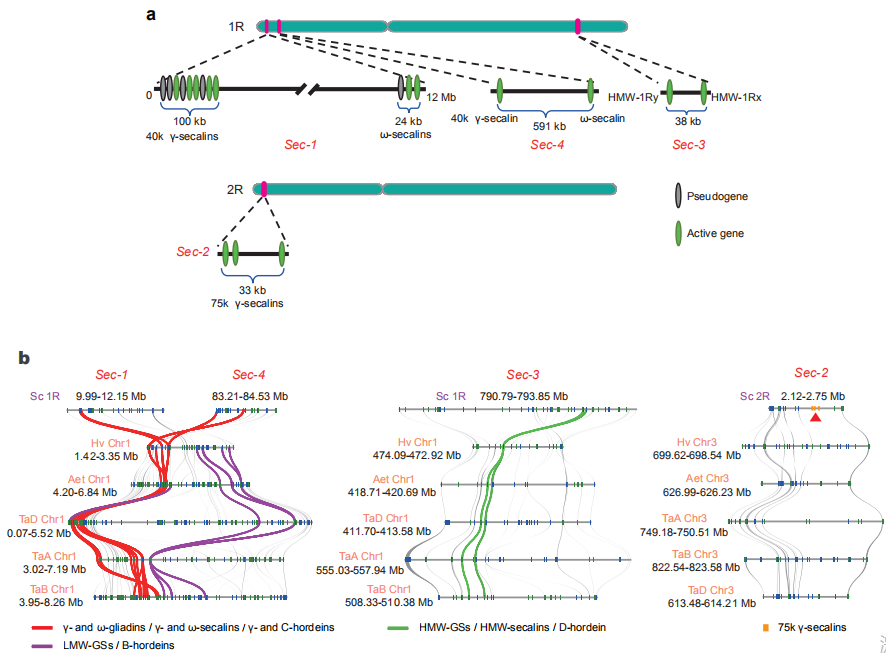
图5 黑麦碱位点分析
作者利用iTAK预测了威宁黑麦和其他8种禾本科植物的TF基因,在注释的65个转录因子基因家族中,威宁黑麦有28个家族成员增加,其中AP2/ERF TF基因家族成员增加幅度较大。威宁黑麦的抗病相关基因(DRA)数量(1989)比乌拉尔图小麦(1621)、节节麦(1758)、大麦(1508)、二穗短柄草(1178)、水稻(1575)以及普通小麦的A(1836)、B(1728)和D(1888)亚基因组多。鉴于AP2/ERF TFs和DRA基因在植物对非生物逆境和生物逆境的反应中的重要作用,上述发现可能有助于黑麦和相关作物的有效遗传研究和分子改良。
在长日照条件下,威宁黑麦比荆州黑麦提前抽穗10-12天(图6a),这与威宁黑麦茎尖分生组织发育更快有关(图6b)。在威宁黑麦基因组中,注释到在长日照条件下高表达的两个开花位点(FT)基因ScFT1(ScWN4R01G446100)和ScFT2(ScWN3R01G192500)。播种后7天和10天,ScFT1和ScFT2在威宁黑麦中的表达水平显著高于荆州黑麦(图6c),且ScFT蛋白在黑麦中积累到相对较高水平,而荆州黑麦中几乎没有(图6d)。检测到的ScFT蛋白的大小(~29 kDa)比预测出的ScFT1和ScFT2的分子量大(~19 kDa)(图6d),表明ScFT蛋白具有潜在的翻译后修饰。用高效检测磷蛋白的磷酸标记SDS-PAGE分析表明,威宁黑麦中ScFT确实发生了翻译后磷酸化修饰。
作者突变了ScFT2磷酸化相关的两个残基(S76和T132),并为ScFT2构建了一系列去磷模拟位点(S76A、T132A和S76A/T132A)和磷模拟位点(S76D、T132D和S76D/T132D)。当使用马铃薯X病毒载体在烟草中进行外源表达时,ScFT2和去磷双突变体ScFT2S76A/T132A相对于游离GFP(对照)和其他ScFT2突变体,表现出持续促进烟草生长(图6e)。与GFP相比,ScFT2和三个去磷突变体(ScFT2S76A、ScFT2T132A及ScFT2S76A/T132A)的异位表达提高了开花植株的百分比,ScFT2S76A/T132A尤其明显,但在表达三个拟磷突变体(ScFT2S76D, ScFT2T132D, or ScFT2S76D/T132D)中没有观察到这种促进作用(图6f)。免疫印迹分析表明,ScFT2、ScFT2S76A、ScFT2T132A和ScFT2S76A/T132A在烟草植株中的积累量相当高,但ScFT2S76D、ScFT2T132D和ScFT2S76D/T132D在烟草植株中的积累量却很低(图6g)。因此,保守的S76和T132残基的改变影响了ScFT2控制植物开花的功能,这与ScFT2蛋白稳定性的改变有关。本研究首次发现FT磷酸化对开花时间控制的影响,为更全面地探索FT蛋白控制植物开花的分子和生化机制提供了新的途径。
作者进一步研究了光周期Photoperiod(Ppd)基因的表达,该基因在长日照条件下正调控FT的表达。在威宁和荆州黑麦的转录组分析中发现了一个表达Ppd的基因ScPpd1(ScWN2R01G043000)。该基因在威宁黑麦内的表达非常早,在播种2 天后达到表达高峰;而荆州黑麦在播种4天后才达到高峰(图6h)。根据ScPpd1对黑麦抽穗期的调控作用,研究者利用威宁×荆州F2代群体,检测到与前期研究一致的三个主效抽穗期QTL(Hd2R、Hd5R和Hd6R)。
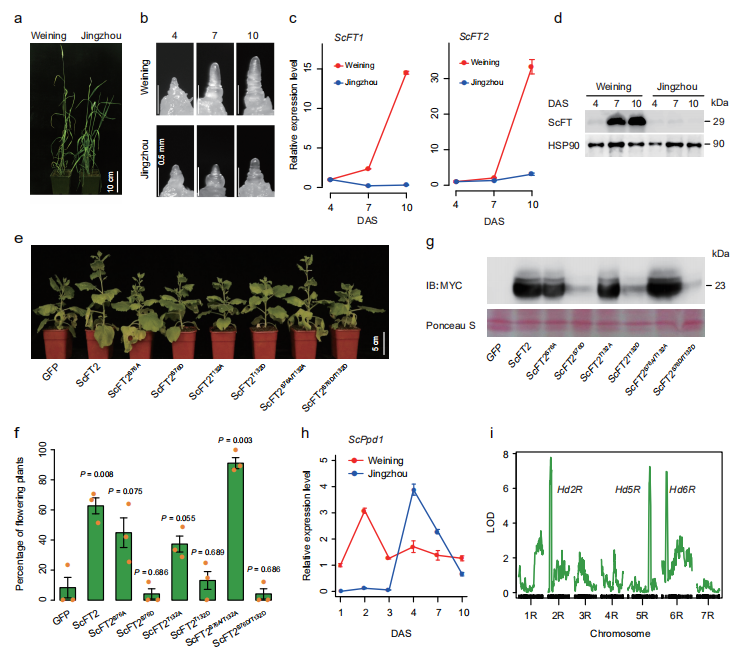
图6 威宁黑麦早期抽穗性状的发育及基因表达特征
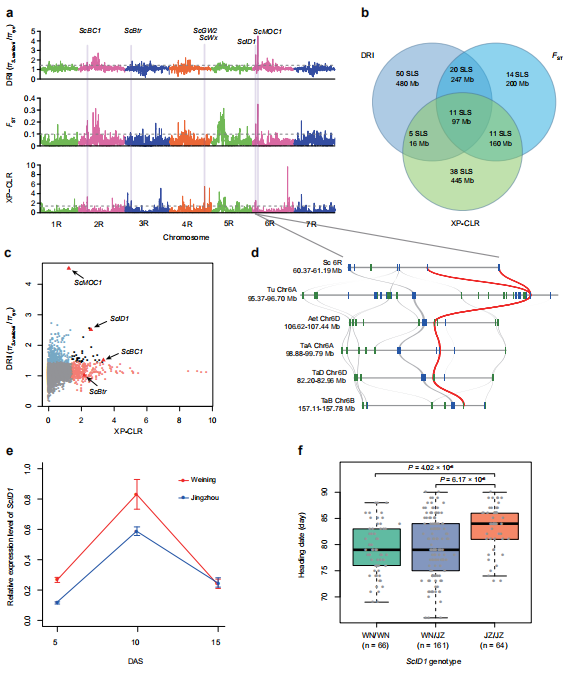
对驯化基因的分析可以促进对作物性状的理解和改良,但在黑麦中这类基因的分子分析方面进展甚微。作者通过全基因组选择清除分析,利用在栽培黑麦和瓦维洛夫黑麦(S. vavilovii)之间鉴定的123647个SNPs,挖掘黑麦驯化相关染色体区域和基因座。DRI、FST、XP-CLR分析中,共同识别到11个选择信号(图7a-c)。通过与水稻和大麦的共线性比较,发现了一些可能的选择清除位点,包括已在水稻或大麦中已被功能分析的ScBC1、ScBtr、ScGW2、ScMOC1、ScID1和ScWx的同源基因(图7a-c)。
检测到的ScID1基因座包含一对具有相同编码序列的ScID1同源序列(ScWN6R01G057200和ScWN6R01G057300,下称ScID1.1和ScID1.2)(图7d)。ScID1.1和ScID1.2蛋白与玉米ID1(63.19%)和水稻RID1(65.34%)具有很强的同源性,这两个蛋白在玉米和水稻中都被发现调控着从营养体向花发育的转换。ScID1.1和ScID1.2在威宁黑麦幼叶中的表达水平高于荆州黑麦(图7e)。在威宁×荆州分离的F2群体中,ScID1JZ/JZ纯合植株的平均抽穗期显著晚于ScID1JZ/WN或ScID1WN/WN个体(图7f),这与荆州黑麦相对于威宁黑麦的晚花表型相一致(图6a)。以上结果表明ScID1可能参与了抽穗期的调控,并可能通过黑麦驯化进行选择,使作物成熟度得到适当的调整,以更好地适应生长环境。






 京公网安备 11011302003368号
京公网安备 11011302003368号