英文题目:Unveiling COVID-19-associated organ-specific cell types and cell-specific pathway cascade
中文题目:揭示与新冠病毒(COVID-19)有关的器官特异的细胞类型以及细胞特异的通路级联反应
发表期刊:Briefings in bioinformatics
发表时间:2020.09.24
影响因子:8.99
研究背景
血管紧张素转换酶2(ACE2)作为COVID-19的特异性受体在宿主细胞中发挥着重要作用,从而使得新冠疫情大流行。与特异的肺泡II型细胞相比,ACE2在膀胱、回肠、肾和肝脏中相对的高表达。在本研究中,通过对五个组织的单细胞测序识别出ACE2高表达的细胞类型;随后,构建蛋白质-蛋白质互作网络(PPIN),以识别形成功能性中心节点的潜在生物标志物。经研究发现,肾素-血管紧张素系统和PPAR信号通路对加强新冠病毒感染具有重要作用,本文也显示出PPAR蛋白家族在功能性中枢节点中起到重要的作用。为理解潜在标志物的功能,通过构建通路语义网络研究相关的通路,随后,对识别出的通路用PageRank算法进行排秩;接着,这些通路网络也由一些基本的代谢通路所构成,比如胰岛素抵抗通路等。经过一系列的研究表明,血管紧张素和PPAR蛋白质家族可以认为是新冠患者可能的治疗靶点。
研究流程
总的来说,这篇文章遵循着获取数据、数据处理、识别特异的细胞类型以及进行语义通路的构建等的流程来进行研究(Figure 1)。
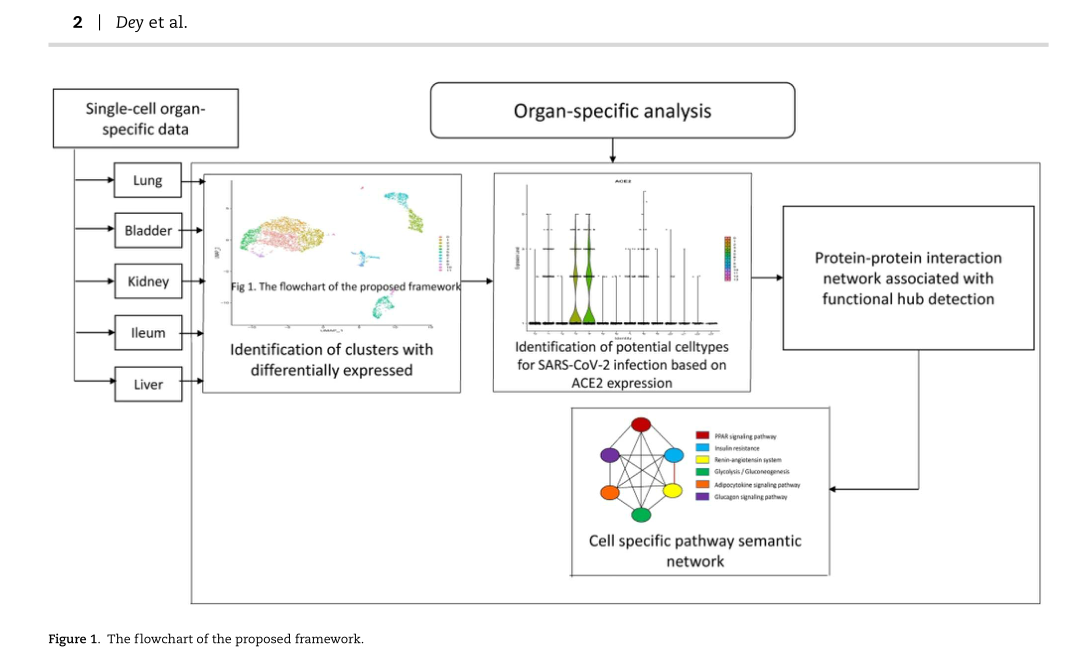
材料和研究方法
从GEO中获取(膀胱、回肠、肾、肝脏和肺等)不同组织和器官的单细胞测序数据,膀胱的样本是GEO accession no. GSE129845,sample GSM3723358; 回肠的样本是GEO accession no. GSE134809,sample GSM3972018;肾的样本是GEO accession no. GSE131685;肝脏的样本是GEO accession no. GSE115469,肺脏的样本是 GEO accession no. GSE122960。
SeuratV3.0用来产生原始的count矩阵,并筛选线粒体数>5%的细胞,然后用”LogNormalized”函数进行标准化,并用乘以10000后取自然对数进行归一化。主成分方法用来构建k近邻图,细胞用”FindClusters”方法进行聚类,并用UMAP工具来进行可视化。通过Wilcoxon秩和统计检验,使用“FindMarkers”函数将最小百分比设为0.25来识别每个聚类中最高差异表达的基因标记。
研究结果
一、肺组织细胞特异的功能节点
由于ACE2、AGT和PPARA在PAT2细胞中显著表达,因此PAT2细胞可作为肺组织的潜在的与新冠病毒感染的细胞。ACE2表达水平的表达图提示肺对病毒血症具有高度的易感性。然而,该研究也鉴定了两种不同的细胞,即浆细胞和肥大细胞。在浆细胞中,三种转录均显著表达,而在肥大细胞中,AGT和ACE2显著表达。
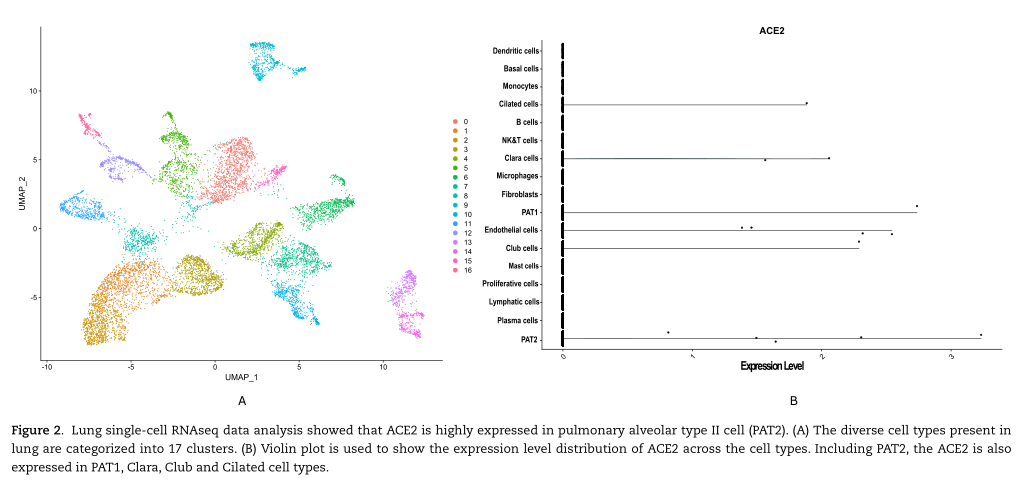
二、膀胱和肾组织细胞特异的功能节点
在膀胱中,ACE2与尿路上皮细胞有较高的亲和力,如Figure 3所示。与PPARA不同,来自PPAR家族的PPARG表达水平显著。从肾脏来看,ACE2在近端小管细胞和平滑肌细胞中表现出更高的亲和力(如Figure 4所示)。
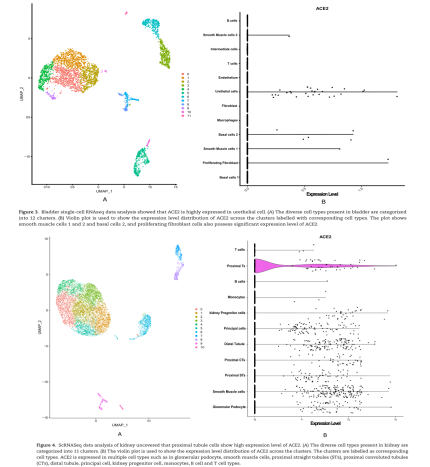
三、回肠与肝脏细胞特异的功能节点
回肠和肝脏是代谢系统的一个区域,两个器官都有ACE2阳性的上皮样细胞。在回肠中,肠上皮细胞和纤毛上皮细胞有显著表达ACE2, AGT和PPARA(Figure 5),但是,Figure 6中显示相对于其他器官,这些细胞表达水平相对较低。类似地,胆管细胞是主要存在于肝组织中的一种上皮细胞。在这些细胞类型中,ACE2、AGT和PPARA标记物的表达值较高。
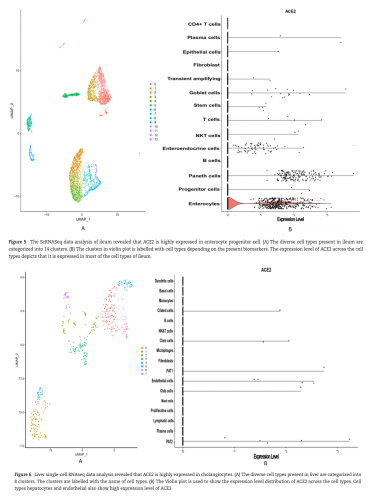
四、通路语义网络结果
考虑到每一途径的生物学过程,本文构建了语义相似度图。ACE2在三种不同类型的肺细胞中均有高表达,研究中分别在Figure 7A、B和C中给出了Mast、PAT2和浆细胞的通路语义网络。在膀胱中,ACE2在一种特殊的细胞类型中表达,即尿路上皮细胞(如Figure 8A所示)。而在肾脏中,ACE2的近端小管细胞(如Figure 8B所示)和平滑肌细胞(如Figure 8C所示)表达率较高。在回肠细胞类型,如纤毛上皮细胞(如Figure 9A所示)和肠上皮细胞祖细胞(如Figure 9B所示)显示ACE2的显著表达水平。与膀胱器官相似,ACE2在肝脏中表达于一种特殊的细胞类型,即胆管细胞(如Figure 9C所示),ACE2表达水平显著。在通路语义网络图中,节点表示一条特定的路径,加权边定义两条路径之间的相似度值,刻画共享生物过程的最大数量。
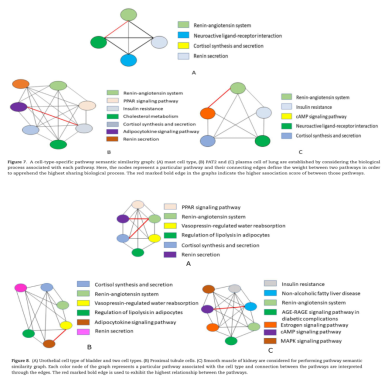
在通路语义计算过程中,得到一个合成矩阵,利用该矩阵对每个细胞类型进行PR算法,并根据得分对细胞类型进行排序。我们发现肾素-血管紧张素系统(RAS)和PPAR信号通路在大多数prime细胞类型中获得较高的排名。此外,胰岛素抵抗在这三个器官中也占有重要地位。Figure 10提供了一个热图,对应于来自不同细胞类型的每个通路的PR值。如前所述,通过计算PR值和对应的rank来表示网络中各个通路的影响。根据整体排名和得分,通路在heatmap中很好地分离。含有AGT和PPAR家族蛋白的通路在缺乏胰岛素抵抗通路的回肠中排名靠前。此外,PPAR信号通路在肝细胞类型中缺乏。有趣的是,皮质醇的合成和分泌途径在某些细胞类型中起着重要作用。
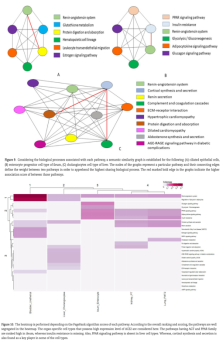
在单个细胞类型中,受影响的细胞和通路调节之间的关系如Figure 11所示。只显示了每个器官中高度表达ACE2的细胞类型。从图中可以看出,PPAR信号通路和RAS是感染后的主要通路。这种细胞类型特异性的研究发现一些途径在肺中是共同的,但影响率是不同的,对膀胱和肾脏也类似。
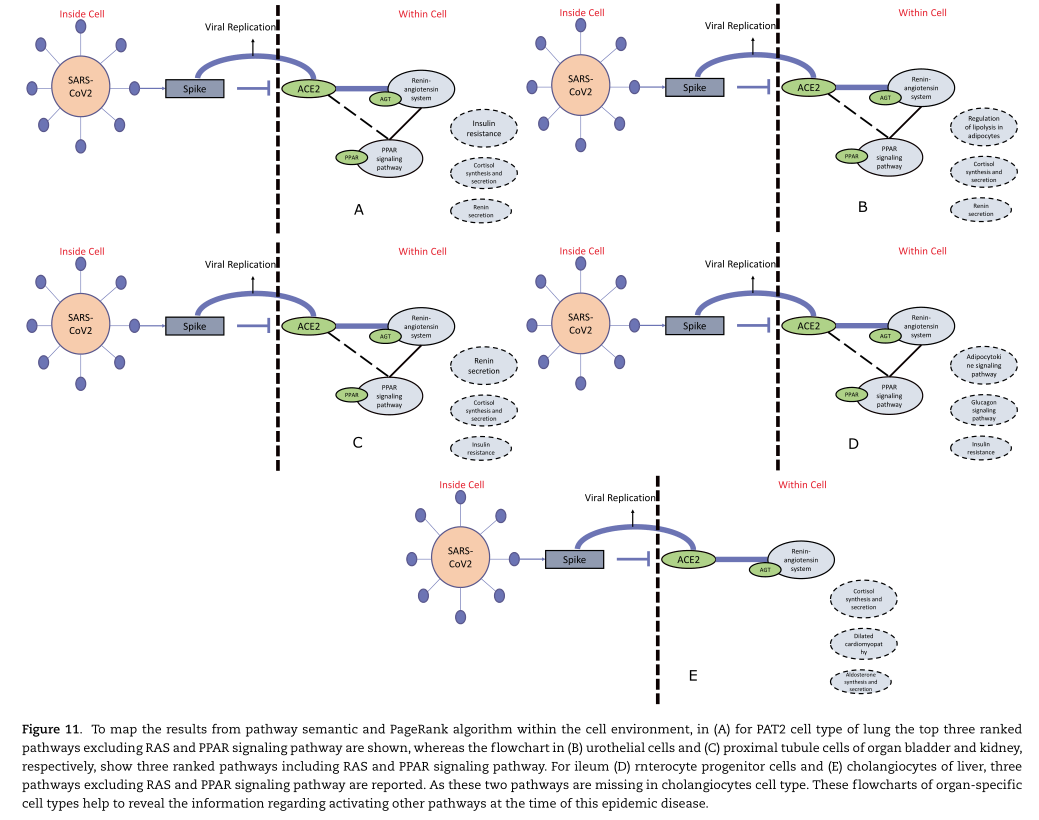
研究结论
本文采用的基于单细胞的生物信息学策略旨在揭示器官特异性可能感染的细胞类型。本研究的主要目的是确定COVID-19感染期间ACE2失调可能的通路连接。首先,从五个器官中检测细胞类型;此外,每一种有影响的细胞类型都有一系列的生物标志物,标志物是根据与ACE2连接的交互功能枢纽来排序的。有趣的是,AGT和PPAR家族转录本在每个功能枢纽中都是具有共同的作用。这两份转录本将ACE2和功能群落的其余样本连接起来。根据相关文献,既往观察到血管紧张素和PPAR家族蛋白参与COVID-19等不同感染,在本实验中,研究了PPAR信号通路的影响,PPAR通路和RAS信号通路已经在hub-specific pathway语义网络中得到了证明。该网络表明,上述途径的显著调节可以影响正常代谢通路的正常功能,以及少数其他通路,如胰岛素抵抗。因此,这些通路是COVID-19感染患者重要的治疗候选靶标。
小编有话说:
单细胞数据集的深度挖掘,通过构建通路语义网络可以揭示更多细胞特异的通路级联反应和蛋白互作网络,更加全面表征细胞间互作关系。数据集的挖掘依赖于生信工程师的专业技能,如此高大上的生信分析对于一般科研工作者来说还是有一定门槛。不过百迈客强大的生信工程师团队和云平台(BMKCloud)已经实现你零基础分析的所有梦想!52款APP实现高度自由个性化分析,118款工具、交互的个性化分析提供无上限分析实操,云平台课堂高效助您方案设计和信息分析,百迈客云成为您的私人信息分析平台,让基因分析更简单。
想了解更多百迈客云分析平台?点击文末“阅读原文”(http://www.biocloud.net/),多款分析工具等您来解锁哦~






 京公网安备 11011302003368号
京公网安备 11011302003368号