每个人的衣橱的里面都会有一件白色的T恤,因为百搭。其实测序界也有一件白色的T恤,小伙伴们你们猜出来了吗?没错,它就是转录组。转录组是一款比较基础的测序产品,他可以和不同的组学进行搭配,或是用于找关键的biomarker,或是用于协助解析分子机制。
今天小编就带着大家看一篇关于的转录组、RNA甲基化、蛋白组联合的文章。这篇文章中RNA甲基化是采用的MeRIP-seq二代的技术,操作相对比较复杂,现在已经可以升级做ONT RNA甲基化,值得一提的是这篇文章的整体思路是可以借鉴的。
文献名:m6A modification suppresses ocular melanoma through modulating HINT2 mRNA translation
期刊:Molecular Cancer(IF:15.302)

文章思路快速get :
文章中通过RNA甲基化试剂盒的检测发现在黑素瘤样本中m6A甲基化水平降低,为了进一步研究m6A甲基化在肿瘤样本中的调控机制。采用RNA-seq、MeRIP-seq等技术找到关键的基因HINT2,随后在细胞系中进行敲除实验,检测细胞侵袭、凋亡等情况;同时进行RIP-qPCR、RNA-pull down以及双荧光素酶实验等实验,揭示了m6A甲基化修饰在眼部黑色素瘤肿瘤中调控中的机制,为后续研究以及药物治疗提供了新的见解。
研究背景
恶性黑素瘤( malignant melanoma,MM) 的发生率在常见肿瘤中排第 4 位,分别占男性和女性癌症病例的 6.4%和 4.1%。约 91%的 MM 发生在皮肤上,皮肤黑素瘤( cutaneous malignant melanoma,CMM) 是最具攻击性和致命性的皮肤肿瘤。RNA 甲基化是近年来的研究热点,目前发现其参与了多种肿瘤的发生发展过程,与免疫治疗耐受的发生密切相关,其在黑素瘤中的研究也逐渐引起关注。
技术平台
RNA-seq、MeRIP-seq、Label-free MS
研究结果
1. 黑素瘤样本中m6A甲基化水平降低
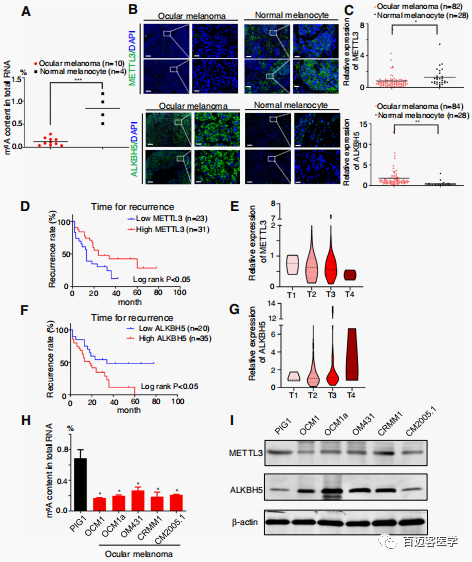
Fig1 m6A水平降低与眼部黑色素瘤预后不良有关
为了研究m6A甲基化在眼恶性黑色素瘤中的功能作用,研究者用甲基化试剂盒先对肿瘤样本和正常样本做甲基化整体水平检测,发现在肿瘤样本中RNA甲基化的水平明显降低(Fig. 1a)。同时通过免疫荧光实验和含量检测,发现甲基化转移酶METTL3相对于正常的样本来说,有明显的降低;而去甲基化酶(eraser)ALKBH5在则明显高于正常组织样本(Fig. 1b-1c)。Kaplan-Meier分析显示METTL3低表达会增强肿瘤早期复发和细胞侵袭,而高表达ALKBH5则显示预后不良。除此之外,黑色素瘤肿瘤细胞系结果也与组织样本中的结果一致。这些数据表明,不管是组织样本还是细胞系样本中,黑色瘤素样本中可以通过低表达METTL3或者高表达ALKBH5来降低m6A修饰。
为了进一步说明上述结论的准确性,研究者在细胞系做分别对METTL3、ALKBH5进行敲除实验。发现沉默METTL3后,正常黑素细胞形成较大的集落,细胞分裂加快,凋亡减少;沉默ALKBH5,m6A甲基化显著增加,细胞分裂减少,凋亡增加。同时转录组RNAseq和GSEA分析都进一步证明在高m6A修饰的细胞系中抗肿瘤明显,并且ALKBH5是主要靶基因簇。
2. 甲基化测序和转录组测序寻找m6A介导的潜在靶点
随后对正常细胞系和肿瘤细胞系进行MeRIP-seq和miCLIP-seq进行甲基化检测。从正常细胞和肿瘤细胞生成的miclipo -seq文库中,平均鉴定出13,083和11,750个m6A峰。实验结果表明,m6A修饰在肿瘤细胞中广泛重复,而正常细胞中有更多的基因只有一个m6A位点。同时鉴定到有5828个m6A显著改变的基因。GO 注释结果显示这些基因主要富集在细胞增殖和细胞死亡。KEGG通路分析显示在HIF-1 和 p53通路有明显富集。并且正常细胞中含有m6A修饰的转录本数量比肿瘤细胞高出5倍以上(Fig2a),而这些转录本主要参与细胞增殖和肿瘤发生相关的几种信号通路(Fig2b)。这些现象都表明m6A在肿瘤发生过程中有着重要的调控作用。
为了系统地阐明眼黑色素瘤中m6A修饰减少导致的基因表达变化,研究者结合转录组、蛋白定量的数据找到了237个相关的基因(Fig2c)。正如预期的那样,这些基因存在m6A修饰,且基因mRNA表达和蛋白表达不一致,说明m6A修饰可能影响转录后调控。找到的这些基因主要还是集中细胞周期、细胞粘附和蛋白过程(Fig2d)。其中HINT2是在正常细胞中蛋白表达和m6A富集最显著的基因之一,因此研究这选择它作为典型例子来分析m6A修饰在肿瘤发生过程中作为翻译调节因子的机制(Fig2e)。在miCLIP-seq数据中,发现3’UTR上的HINT2 mRNA中有一个具有统计学意义的m6A峰,在正常细胞中富集明显(Fig2f)。为了验证该结论的准确性,作者通过RIP-qPCR、Western blotting和qPCR验证了HINT2 mRNA上m6A修饰减少,HINT2蛋白表达下调,而mRNA水平无显著变化。
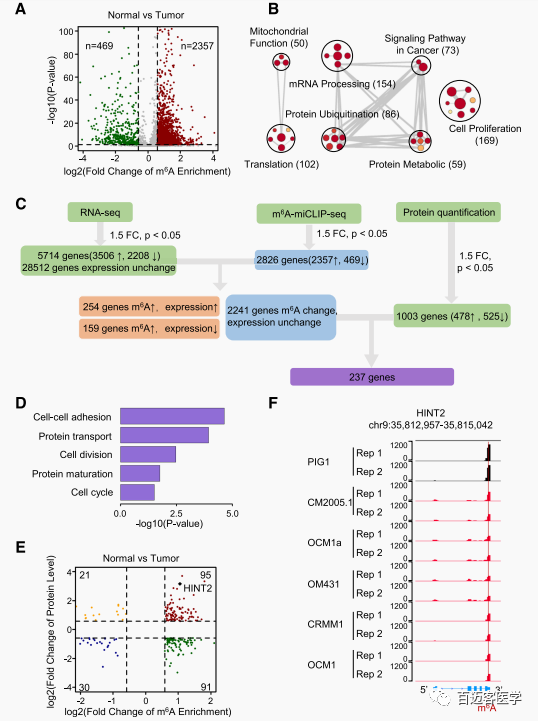
Fig2 转录组范围内识别调控肿瘤发生的m6A靶点
3. HINT2依赖于m6A抑制眼部黑色素瘤
在眼黑色素瘤细胞中,在mRNA水平和蛋白水平均过表达HINT2。发现过表达HINT2后,眼黑色素瘤细胞的细胞增殖、细胞迁移、和克隆形成明显受到抑制,细胞凋亡增加。此外,GSEA显示在肿瘤细胞中HINT2促进凋亡和细胞死亡(Fig3a)。为了确定HINT2在体内肿瘤特征中的作用,过表达HINT2的眼黑色素瘤细胞进行了皮下移植。结果显示:相对于对照组(Fig3b, A组)来说,实验组HINT2过表达组(Fig3b, B组)肿瘤体积持续降低。为了研究这些蛋白表达的变化是否在样本中发生,在眼黑色素瘤和正常组织中进行IF实验(Fig3c),发现HINT2确实在肿瘤样本中下调。除此之外,在眼黑色素瘤组织样本中,低表达的HINT2与不良预后高度相关(Fig3e)。
由于HINT2在眼黑色素瘤中抑制细胞生长和迁移,并且与正常细胞相比,肿瘤中m6A甲基化减少,推测m6A修饰降低会上调HINT2表达从而抑制肿瘤生长。通过对的MeRIP的RNA片段进一步检测发现HINT2 mRNA的 3’UTR上m6A峰被METTL3特异性甲基化,和ALKBH5去甲基化。除此之外,HINT2蛋白的表达水平远远高于mRNA的表达水平。随后在肿瘤细胞系构建敲除HINT2细胞系,结果都表明m6A引导的肿瘤抑制作用部分来源于HINT2的转录后调控。
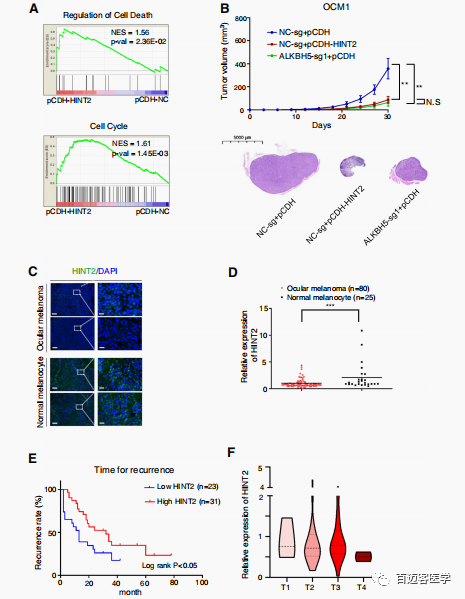
Fig3 HINT2在眼黑色素瘤细胞中起抑癌基因的作用
4. m6A修饰促进了HINT2翻译
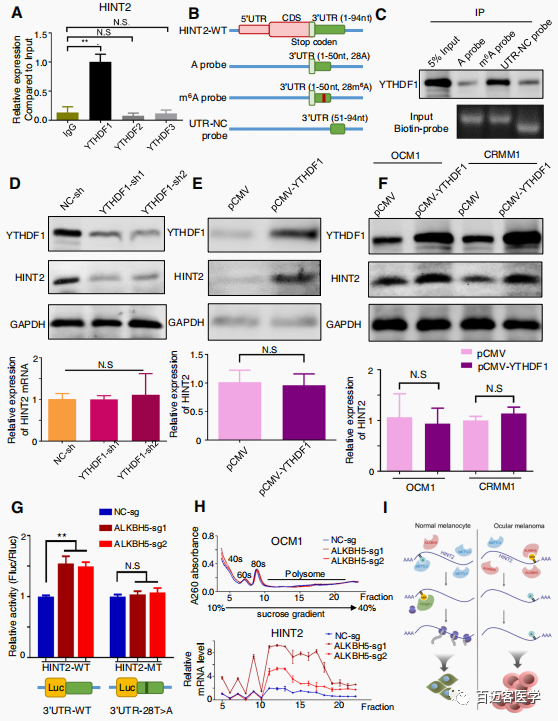
因为m6A甲基化似乎促进了HINT2的翻译,作者假设HINT2转录本是YTH家族的靶点,YTH家族是m6A解读器,调控m6A修饰的转录本的翻译。RIP-qPCR分析显示,HINT2 mRNA与YTHDF1的相互作用强于其他 mRNA(Fig4a)。此外,RNA-pull down实验进一步证实YTHDF1与HINT2 mRNA相互作用,HINT2的m6A修饰极大地促进了其与YTHDF1的结合(Fig4b, c)。YTHDF1表达下调(Fig4d line 1)降低了HINT2 蛋白的表达(Fig4d line2),而YTHDF1过表达(Fig4e, f line 1)增加了HINT2蛋白的表达(Fig4e- f line2)。这些HINT2表达的变化不是由于HINT2 转录本丰度的变化(Fig4d-f);而是mRNA翻译的调控依赖于转录本的甲基化。同时HINT2 3’UTR (WT)或m6A位点突变(MT)序列构建双荧光素酶载体,双荧光素酶实验也显示,ALKBH5显著降低了报告基因的荧光素酶活性,(Fig4g)。具体来说,通过m6A修饰,HINT2转录本与积极转录核糖体的关联得到了改善(Fig4h)。综上所述,当YTHDF1识别HINT2时,m6A修饰对其翻译有影响。
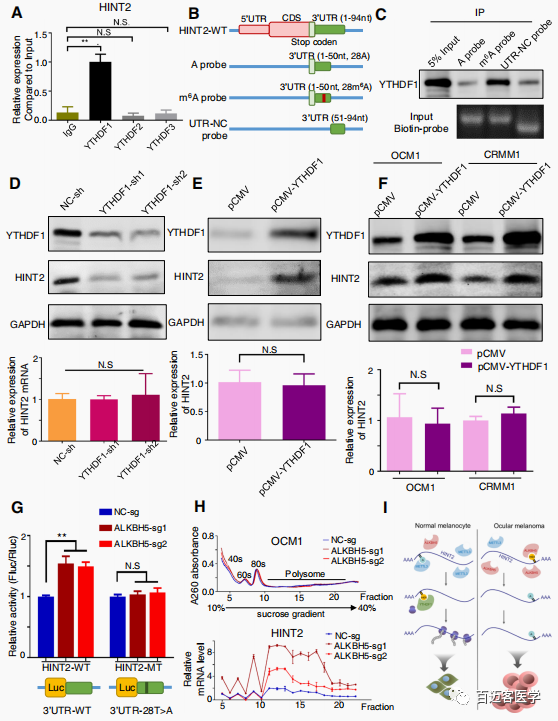
Fig3 YTHDF1 促进 HINT2翻译





 京公网安备 11011302003368号
京公网安备 11011302003368号