2020年8月31日,山西农业大学杂粮分子育种团队与中国农业科学院作物科学研究所等单位合作研究论文“A mini-foxtail millet with an Arabidopsis-like life cycle as a C4 model system”在线发表于国际期刊Nature Plants(IF:13.256),报道了C4禾谷类研究的理想模式植物“小米”的研究成果。山西农业大学的杨致荣教授、中国农业科学院作物科学研究所的张皓珊博士和山西农业大学的李旭凯副教授为论文的共同第一作者;山西农业大学的王兴春教授、韩渊怀教授和中国农业科学院作物科学研究所的隋毅副研究员为论文的共同通讯作者。美国普渡大学和英国诺丁汉大学等单位参与了部分研究。百迈客有幸参与了其中基因组、转录组及数据库构建工作。目前,数据库由百迈客负责维护和运行,暂时托管在公司服务器(http://foxtail-millet.biocloud.net/home)。

研究背景
众所周知,与C3植物相比,C4植物具有较高的光合效率和水肥利用率。因此,若能将C4光合途径整合到水稻等C3作物,将有望大幅提高水稻产量,解决由于人口增长带来的温饱问题。然而,目前常用的模式植物拟南芥和水稻都是C3植物,作为C4作物的模式植物时有很大的局限性,无法解决诸如C4光合代谢以及许多黍亚科特殊的基础问题。
谷子(Setaria italica)起源于中国,是我国几千年来的主栽作物和中华民族的哺育作物。此外,具有抗旱、耐瘠薄和高光效等突出优势,恰恰弥补了拟南芥和水稻作为模式植物的不足,是极具发展潜力的禾谷类模式植物。但谷子生育期较长、株高较高、遗传转化困难,极大地限制了其作为模式植物在功能基因组学研究中的应用。本次研究筛选到一个超早熟谷子突变体“小米”,其生命周期短,植株小,与拟南芥相似。“小米”模式植物体系的建立将极大促进C4高光效、氮素高效吸收利用机制、抗旱机制、遗传驯化和优异品质形成的分子基础等研究,使“小米”成为C4植物功能研究的理想模式系统。
研究材料与方法
每株系约50株T1转基因幼苗进行重测序,每株系约12 Gb的数据(~28×)。晋谷21、“小米”、“小米”2进行重测序比较分析。
11个不同的组织:3日龄种子(种子)、2周龄整株苗(苗)、根、茎、2周龄苗的第一片全展叶(叶1),30日龄植株顶第二叶(叶2)、旗叶(叶3)、第四叶(叶4)、未成熟的圆锥花序(圆锥花序1)、授粉期圆锥花序(圆锥花序2)、灌浆期圆锥花序(圆锥花序3);叶2有5个生物学重复,其他有3个生物学重复。
主要研究内容
1. “小米”的创造与表型表征
2. “小米”的特性由PHYC基因突变引起
3. “小米”基因组组装注释
4. 谷子品种间基因组序列比较
5. “小米”动态基因表达图谱的构建
6. 农杆菌介导高效遗传转化体系的建立
研究结果
1. “小米”的创造与表型表征
利用EMS诱变技术对山西省名优谷子晋谷21进行了诱变,从中筛选到一个超早熟突变体“小米”。
“小米”主要有以下特征:(1)表现出极早的开花表型:抽穗期39天(播种后天数,DAS)左右,约70天内完成了生命周期。而野生型(晋谷21,WT)的平均抽穗期约为82 天(DAS),成熟期为130 DAS(图1b、c);(2)“小米”比野生型矮(图1b),但结实率高12.83%,且种子大小没有显著差异(图1d);(3)“小米”在短日(SD,10h光照/14h暗)条件下比长日(LD,16h光/8h暗)条件下的抽穗晚了约一个月,表明“小米”的早期抽穗依赖于LD条件(图1e)。通过延长日长和优化其他条件,可以将“小米”的生命周期缩短到65天,株高约为29厘米(图1f),每年可以在成长室里完成5到6代。(4)仅需较小的种植面积,类似于种植等量的拟南芥植株。
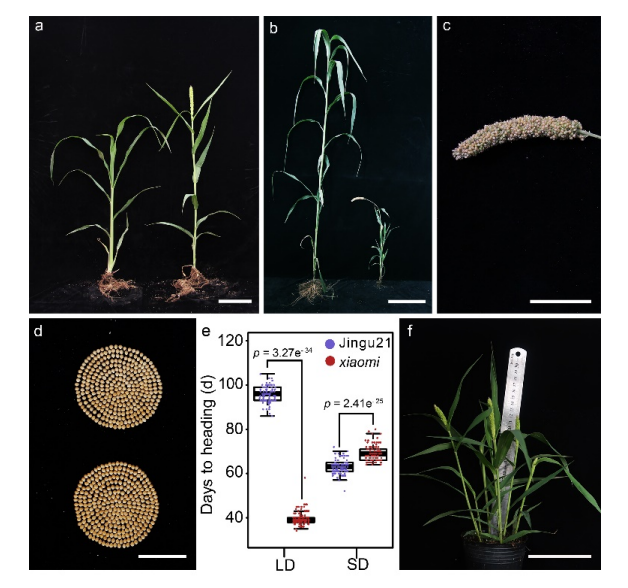
图1 “小米”的表型特征
2. “小米”的特性由PHYC基因突变引起
为了找出导致“小米”早熟的突变,研究者将其与抽穗期为75 DAS的G1杂交。所有9株F1植株均表现出类似G1的晚抽穗表型,由268株组成的F2群体表现出G1型晚抽穗期与“小米”型早抽穗期的分离比为3:1( χ2=0.318<χ2 0.05(1)=3.841),说明“小米”早熟抽穗期是由单基因座隐性突变引起的。利用106个早花F2个体,将该位点定位到9号染色体上的212kb区域,根据“小米”参考基因组的注释,该区域含有27个基因(图2a)。
将“小米”基因组序列与经基因组重测序生成的晋谷21基因组序列进行比较,发现在定位区域只存在一个突变——“小米”基因Si9g09200的编码区从“G”到“T”的突变,该基因编码一种假定的PHYC蛋白(图2a)。在所检测的77个早期抽穗F2个体中,均为T/T纯合突变体。相比之下,在256个晚抽穗个体中,92个是G/G WT纯合子,另外164个是G/T杂合子,反映了基因型和表型之间的完美关联。这种突变产生了一个终止密码子,形成一个截短的蛋白质,占该基因约71%的转录本(转录本1)(图2a-d)。这一突变还导致了113 bp的移码缺失的剪接,形成了占该基因约29%转录本(转录本2)的截短蛋白(图2a-d)。根据预测,被截断的蛋白质缺少第二个PAS结构域的三分之二(肽1)或三分之一(肽2),以及整个HK和HD域(图2d)。
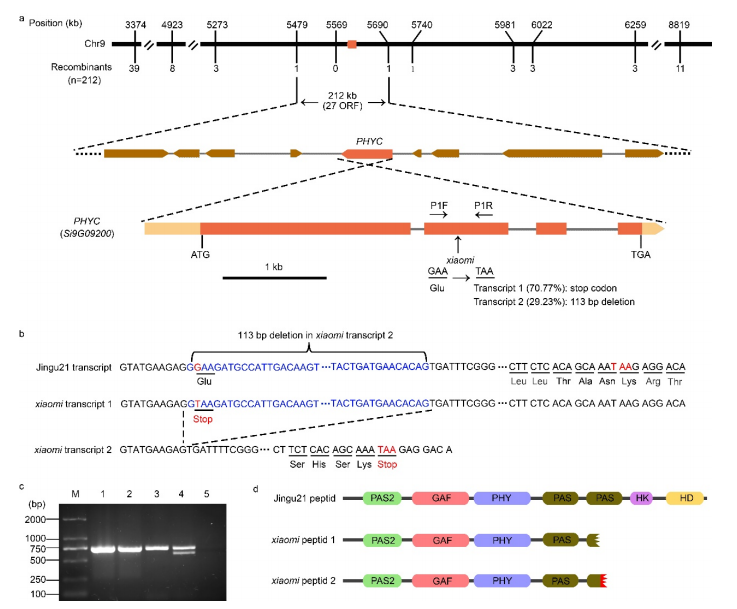
图2 “小米”的分子特征
研究者对另一个来源于晋谷21的突变株——“小米”2号进行了测序。“小米”2号突变体表现出与“小米”相似的早期抽穗表型。PHYC基因座序列比较显示“小米”2号PHYC第一外显子发生单点突变(T674A),导致从保守的亮氨酸变为组蛋白(图3)。这种SNP与M2杂合子突变体的82株早抽穗(A/A基因型)和84株晚抽穗(49 T/A基因型和35 T/T基因型)M3植株的表型分离密切相关。综上所述,这些观察结果证实了早期抽穗表型是由PHYC位点突变引起的。
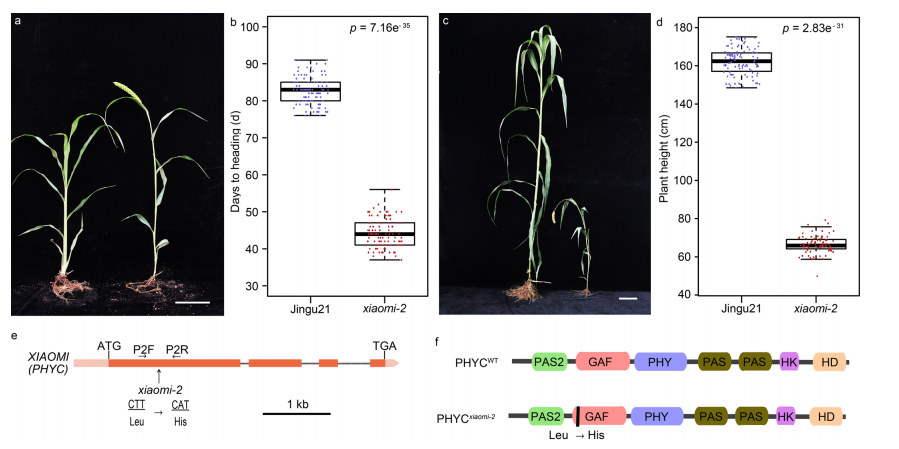
图3 “小米”2号突变体的表型和分子生物学特性
为了了解PHYC位点突变对LD条件下开花时间的影响,研究者利用30-DAS(“小米”抽穗前10天)植株的第二片叶片进行了RNA-seq,并以30-DAS采集的WT叶片为对照。发现与拟南芥振荡器基因、伪应答调节蛋白(PRRs)、PHYTOCLOCK 1 (PCL1) 和GIGANTEA (GI)同源的几个基因在“小米”中的表达受到显著影响(图4)。
与Ghd7同源的下游光周期基因的表达水平下降了约95倍(长日照条件下,增强Ghd7的表达可延迟抽穗期),而与HEADING DATE 1 (Ehd1), HEADING DATE 3a (Hd3a),APETALA1 (AP1)/FRUITFULL (FUL)-like MADS box基因同源的开花基因在“小米”中的表达水平显著增加。Ehd1是水稻光周期开花途径中的一个关键转录调控因子,可以激活叶片中成花素Hd3a的转录。在叶片中产生的Hd3a蛋白被转运到茎尖分生组织,在那里诱导AP1/FUL-like MADS box基因的表达。这些观察结果表明,“小米”早熟的表型是由于光周期通路的中断引起的。
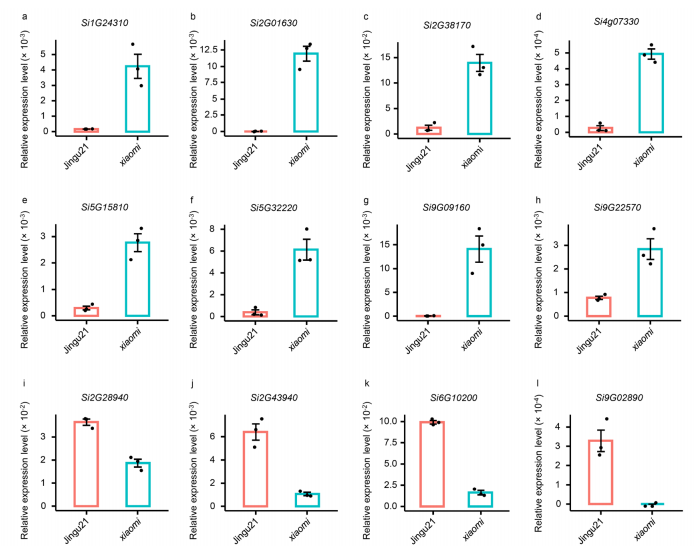
图4 光周期途径RNA-seq结果的qRT-PCR验证
(注:这些蛋白质编码基因命名:Si(代表“小米”),其次是染色体数目和染色体上的基因数,例如,1号染色体上的第一个和第二个基因分别命名为Si1G00010和Si1G00020)
3. “小米”基因组组装注释
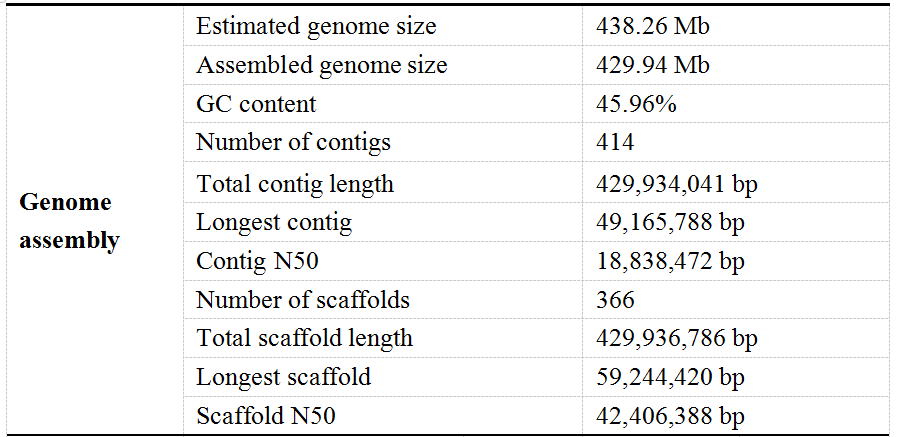
为了便于“小米”作为模型植物的使用,使用PacBio平台组装出429.94 Mb基因组 v1.0(k-mer预估438.26 Mb),contig N50高达18.8 Mb,Scaffold N50为42.41 Mb,并且仅包含48个Gap。其中399.4 Mb通过Hi-C锚定在9条染色体上(挂载率~93%;图5)。根据Illumina DNA比对,组装的错误率约为0.001%(每100kb有一个错误)。BUSCO评估结果为97.78%。这些结果表明“小米”基因组v1.0可以作为研究界的金标准参考。
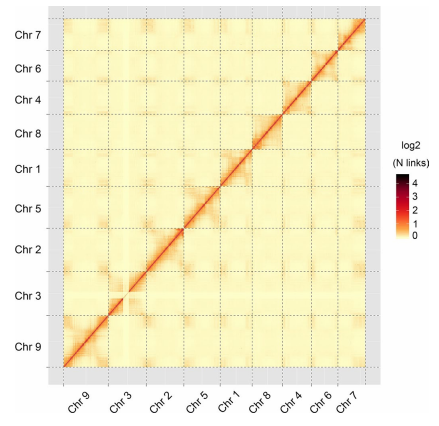
图5 “小米”基因组Hi-C热图
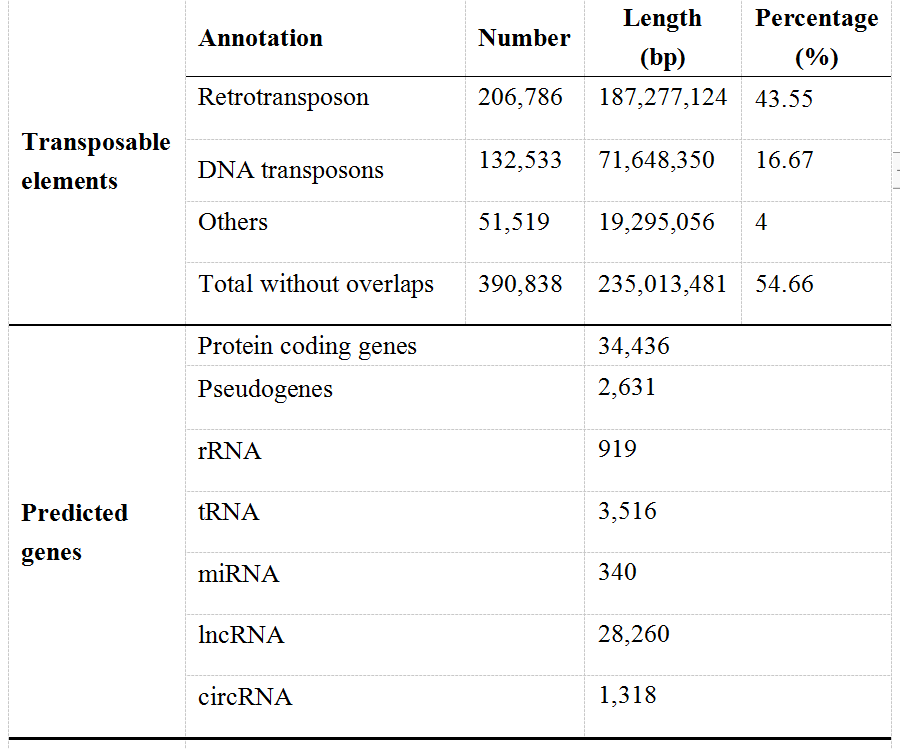
“小米”基因组序列中有237.28 Mb(55.19%)为重复序列。基于从头预测、同源基因预测并结合Iso-seq和RNA-seq,对34436个蛋白质编码基因进行了注释,其中32743个(95.08%)位于9个假染色体上。在GO、KEGG、KOG、TrEMBL、NR数据库中检索这些基因,并与拟南芥和水稻的注释进行比较,检索出具有已知功能的同源基因,共注释33789个基因(98.12%)。此外还注释了919个rRNA基因、3516个tRNA基因、2631个假基因、340个miRNA前体、28260个lncRNA前体和1318个circRNA前体(表1)。
所有的基因组和转录组数据可在数据库(http://sky.sxau.edu.cn/MDSi.htm)公开访问。在这个数据库中,研究人员可以通过染色体坐标、基因或转录符号,或者通过BLAST搜索“小米”基因组、CDS或肽序列来寻找基因组位置。
表1 “小米”基因组组装与注释统计
4. 谷子品种间基因组序列比较
与 豫谷1、张谷和 TT8的3个基因组序列相比,“小米”基因组在基因组覆盖率、contig N50、contig和gap数方面表现出*高的质量。“小米”序列中414.58 Mb(96.44%)对应于豫谷1号 383.52 Mb(95.67%),共有1577935个SNPs。相应区域的大小差异主要由259731个InDel,2804个(总计15.32 Mb)存在变异(>1000bp)和2722个(总计17.38 Mb)缺失变异(>1000bp)引起(图6)。
在“小米”基因组34436个蛋白编码基因中,有32112个基因(93.25%)与豫谷1号基因组(v2.2)共有。2280个“小米”预测基因在张谷基因组中未被发现。在豫谷1号和张谷中均未发现的1030个基因,为“小米”特有基因。
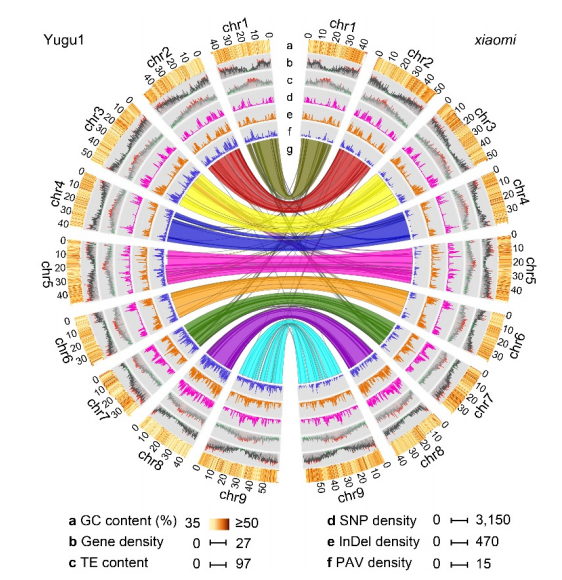
图6 “小米”与豫谷1号基因组比较圈图
5. “小米”动态基因表达图谱的构建
为了建立一个参考的基因表达图谱,研究者测量了“小米”不同发育阶段的11种不同组织的转录水平。总共产生并分析了1054.51 M reads(每个样本约30 M reads)。从顶部第二叶(叶2)到授粉期圆锥花序(圆锥花序2)检测到的基因表达比例为74.26%~82.95%。11个“小米”组织共表达22202个基因。这些基因中,85个(0.25%)在所有被测组织中都有组成性表达,包括一个转录起始因子(Si3G07600)和两个泛素结合酶编码基因(Si1G37980和Si2G05250)。此外,还鉴定了1218个器官/组织特异基因和1226个器官/组织优先表达基因。
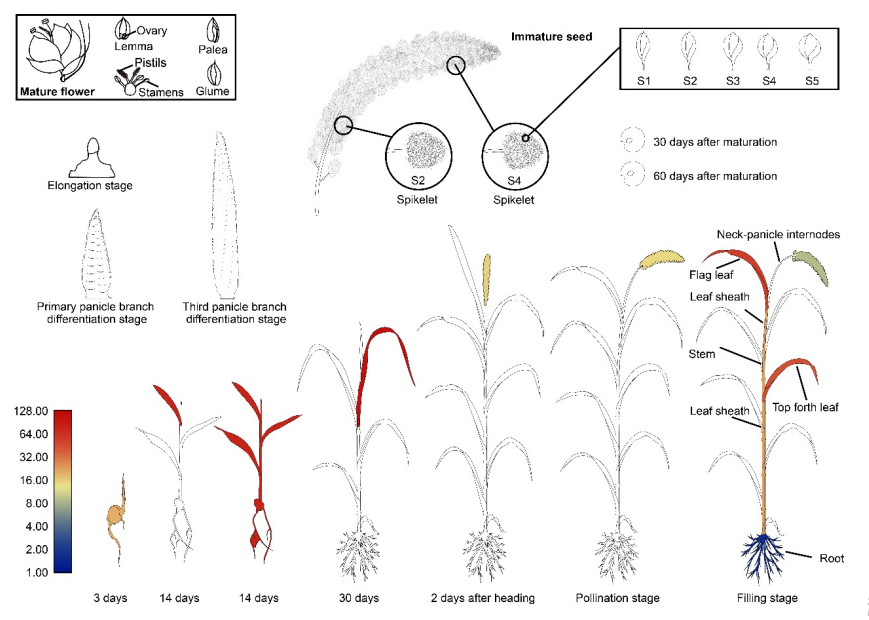
图7 Si9g04830基因表达模式图
6. 农杆菌介导高效遗传转化体系的建立
研究者对各种因素进行了测试,以开发出适合“小米”的农杆菌介导的转化方案。并挑战使用成熟种子作为愈伤组织诱导的起始材料,以避免在使用新鲜组织(如幼花序或未成熟胚)诱导愈伤组织时的昂贵需求。在改良的愈伤组织诱导培养基(CIM)上进行三轮继代培养后,获得了致密的胚性愈伤组织(图8a)。通过使用绿色荧光蛋白(GFP)报告基因来监测农杆菌感染效率,如图8b、c所示,以及筛选转基因愈伤组织的有效性。“小米”的再生能力在CIM培养基上保持良好(图8f)。表达GFP的转基因植株在生根培养基上容易诱导生根,移栽到土壤后成活良好(图8g-i)。
研究者比较了两个常用的选择标记NPTII(新霉素磷酸转移酶II)和HPT(潮霉素磷酸转移酶),NPTII的转化效率为8.05%-38.75%,平均转化效率为23.28%;HPT的转化效率为3.08%-16.67%,平均为8.72%。使用分别扩增GFP基因、UBI启动子、HPT或NPTII选择标记基因的引物,通过PCR来确认转基因原植物(T0)中是否存在转基因(图8j)。观察到绿色荧光蛋白在干种子和发芽种子中的表达,表明转基因已传递给后代(图8k,l)。
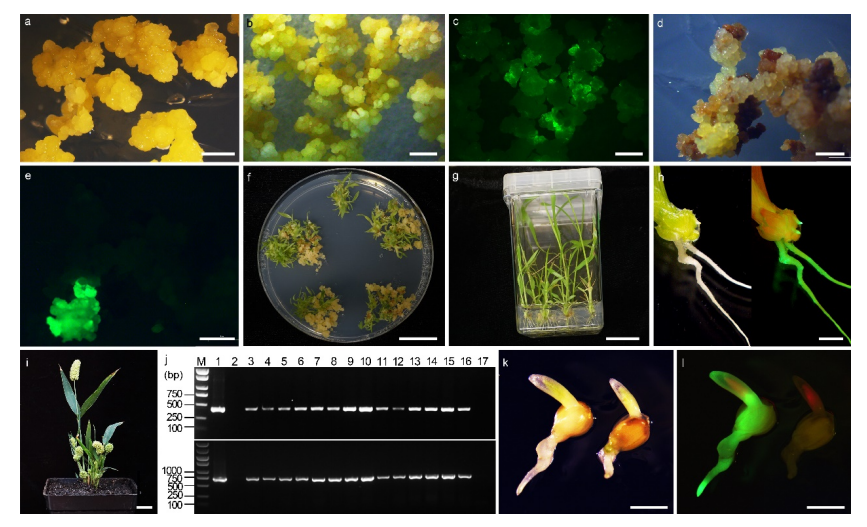
图8 农杆菌介导的“小米”转化研究
用HPT或NPTII标记的13个独立转基因系的基因组测序证实了转基因插入“小米”基因组的正确性,并通过PCR进一步确定了3个检测系的T-DNA插入位点。在盆栽中培育了代表8个转基因事件的T1植株,观察到与未转化的“小米”植株没有明显的表型差异。因此,研究者建立了一个有效的方案,允许在2-3个月内(从农杆菌感染算起)或4-5个月内(从成熟种子开始愈伤组织算起),完成生产准备移植到土壤中的转基因植物(图9)。
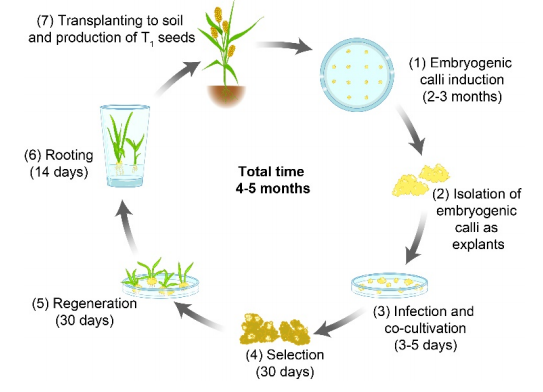
图9 农杆菌介导“小米”转化工艺流程图
小结
本次研究利用EMS诱变技术对山西省名优谷子晋谷21进行了诱变,从中筛选到一个超早熟突变体“小米”。该突变体生育期仅仅两个月左右,株高仅30 cm左右。“小米”的生育期和株高与模式植物拟南芥相当,从而解决了谷子作为C4禾谷类模式植物无法在室内大规模培养的难题。在此基础上,研究团队组装了高质量参考基因组,构建了全生育期基因表达图谱和谷子多组学数据库(http://sky.sxau.edu.cn/MDSi.htm),极大地方便了“小米”功能基因组学研究。经过大量摸索和尝试,建立了一套方便快捷、高效稳定的农杆菌介导的“小米”遗传转化体系(图7)。该体系遗传转化效率高达23.28%,已经接近模式植物拟南芥和水稻的遗传转化水平,解决了“小米”作为模式植物遗传转化效率低下的难题。






 京公网安备 11011302003368号
京公网安备 11011302003368号