C2C12成肌细胞外泌体通过miR-27a-3p促进前成骨细胞MC3T3-E1成骨分化
英文标题:
Exosomes from C2C12 myoblasts enhance osteogenic differentiation of MC3T3-E1 pre-osteoblasts by delivering miR-27a-3p
发表杂志:
Biochemical and Biophysical Research Communications
影响因子:2.559
合作单位:山东省医学科学院
研究背景
越来越多的证据表明,骨与肌肉组织可以影响葡萄糖、能量等代谢。最近,已有报道骨骼和肌肉也可以通过内分泌方式相互调节。并且已确定了一系列参与相互调节的肌肉或骨骼调节剂。关于影响骨形成的候选肌因子(myokines ),胰岛素样生长因子-1(IGF-1)、成纤维细胞生长因子-2(FGF-2)、骨甘氨酸、FAM5家族、白细胞介素-7(IL-7)、IL-5、鸢尾素、卵泡抑素、骨粘连蛋白和基质金属蛋白酶-2(MMP-2)作为成骨促进剂,而肌抑素、转化生长因子-β(TGF-β)、激活素、IL-6、睫状神经营养因子(CNTF)、单核细胞趋化蛋白-1(MCP-1)作为抑制剂,都属于分泌蛋白。
外泌体是由包括肌肉细胞在内的大多数细胞分泌的小囊泡。最近的研究表明,外泌体在细胞通讯中发挥关键作用,通过转移生物活性分子(蛋白质、脂质、mRNA、microRNA)来调节同质和异质受体细胞的功能和分化。例如,作者前期研究表明,成骨细胞衍生的外泌体可以将microRNA载入间充质干细胞,并通过激活Wnt信号通路促进靶细胞的成骨。
考虑到外泌体在细胞通讯中的作用,作者推测外泌体microRNAs是否也可以作为调节骨代谢的特殊“肌细胞因子”。在这项研究中,作者首次提供体外研究证据,证明成肌细胞衍生的外泌体可以进入成骨细胞,促进成骨细胞分化。此外表明miR-27a-3p是这种效应的关键外泌体成分。
研究方法
- 细胞培养与成骨诱导分化:小鼠C2C12细胞培养富集外泌体,MC3T3-E1被诱导骨分化。
- 外泌体富集及miRNA-seq:C2C12细胞外泌体富集,进行miRNA-seq(n=4)。
- 外泌体标记与MC3T3-E1细胞共孵育:观察摄入现象。
- 敲低C2C12中 miR-27a-3p表达,进行RT-PCR定量。
- RT-PCR定量成骨分化标记基因,ALP(碱性磷酸酶)活性测量和茜素红染色。
- MC3T3-E1 Western blot及免疫荧光:验证APC及β-catenin活化。
研究结果
1、C2C12成肌细胞分泌的外泌体可以进入前成骨细胞MC3T3-E1,促进其成骨分化。
将外泌体标记与MC3T3-E1共孵育,观察到这类外泌体(myo-exosomes)能够被MC3T3-E1细胞摄入。并且MC3T3-E1细胞的成骨分化也能够被促进,表现为增强的ALP活性,基质矿化增强,与标记基因ALP/OCN/RUNX2表达上调。对C2C12成肌细胞分泌的外泌体进行小RNA测序,基于测序结果,鉴定出来的miRNA进行共有分析,其中有12个miRNA分子高表达,一些功能被证实的与成骨相关的miRNA分子,例如miR-27a-3p也包括在内。
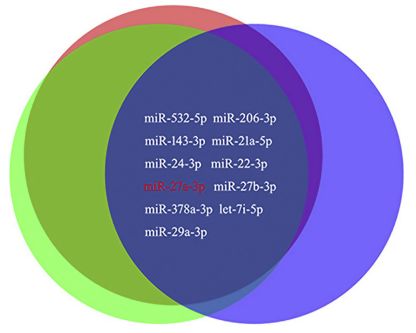 |
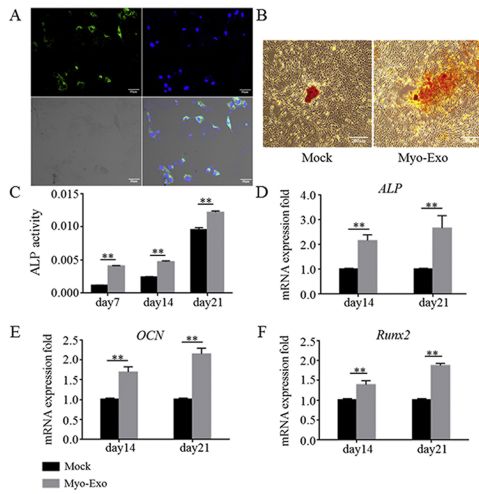 |
2、外泌体的miR-27a-3p在成骨分化中发挥重要作用。
当MC3T3-E1细胞摄入C2C12外泌体后,miR-27a-3p的表达水平升高。进一步敲低miR-27a-3p的表达,C2C12外泌体没有起到促进MC3T3-E1成骨分化的作用。这一结果表明了成肌细胞外泌体依赖于miR-27a-3p发挥促成骨作用。
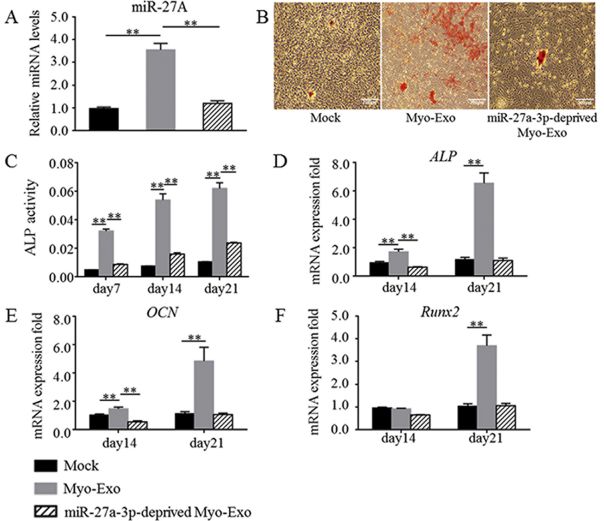
3、C2C12外泌体改变 MC3T3-E1细胞中miR-27a-3p的表达,靶向APC从而激活Wnt/β-catenin pathway。
在成骨分化过程中,Wnt/β-catenin pathway起到重要作用,APC作为该通路的负调节蛋白已被证实直接受miR-27a-3p调控。MC3T3-E1摄入外泌体后,APC的表达受到明显抑制,β-catenin的表达显著升高且被激活。当miR-27a-3p敲低后,外泌体对APC-β-catenin pathway没有影响。
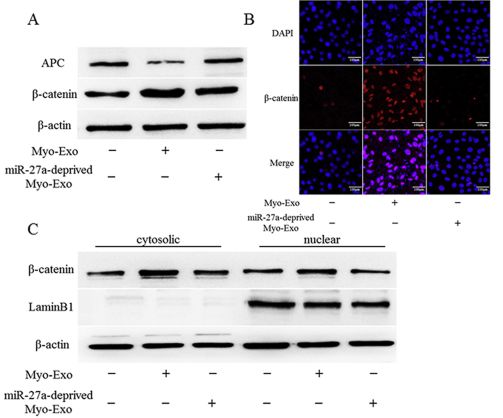
总结
成肌细胞外泌体可以进入前成骨细胞,并促进成骨分化。该效应依赖于外泌体中的miR-27a-3p释放,随之引起前成骨细胞中的β-catenin通路活化。文章研究对肌因子调控肌肉-骨互作提供了新见解,并且强调了成肌细胞外泌体miR-27a-3p作为肌肉相关的异常骨重建的指标和互作靶标的可能性。
参考文献:
Xu Q, Cui Y , Luan J , et al. Exosomes from C2C12 myoblasts enhance osteogenic differentiation of MC3T3-E1 pre-osteoblasts by delivering miR-27a-3p. Biochemical and Biophysical Research Communications, 2018.
如果您的项目有任何问题,欢迎联系我们,我们将给您满意的答复。






 京公网安备 11011302003368号
京公网安备 11011302003368号