
2018年11月14日中国农业科学院生物技术研究所谷晓峰研究团队与百迈客共同合作研究项目“N6-MethyladenineDNA Methylation in Japonica and Indica Rice Genomes and Its Associationwith Gene Expression, Plant Development and Stress Responses”在杂志Molecular Plant上在线发表!通讯作者为谷晓峰研究员。谷老师是中国农业科学院生物技术研究所研究员,博士生导师。围绕发育和产量开展表观遗传学研究,发现多个通过RNA修饰、DNA甲基化、组蛋白修饰等机制调控生育期的新机制。在Molecular Cell、Developmental Cell、PLoSBiology等国际学术期刊上发表文章20余篇。
英文题目:N6-Methyladenine DNA Methylation in Japonica and Indica Rice Genomes and Its Association with Gene Expression, Plant Development and Stress Responses
中文题目:粳稻和籼稻基因组N6-甲基腺嘌呤DNA甲基化及其与基因表达、植物生长和应激反应的关系
发表杂志:Molecular Plant
影响因子:9.326
发表时间:2018.11.14
合作单位:中国农业科学院生物技术研究所
研究背景
N6-甲基腺嘌呤(6mA)是在真核生物和原核生物中发现的丰富的DNA修饰之一,6mA的研究主要集中在其在原核生物中的功能。近年来,动物真菌拟南芥和绿藻的研究开始揭示6mA甲基化的全基因组模式及其在真核细胞中调节基因表达的作用。6mA在植物中的生物学功能在很大程度上是未知的,水稻是世界上重要的作物之一,也是分子和遗传学研究的模式物种,以扩展我们在植物中6mA的知识。
研究材料
粳稻日本晴栽培种Japonica Nipponbare (Nip) ;籼稻栽培种 Indica 93-11
研究方法
Denovo:PacBio RSII (Nip:117X;93-11:116X);Illumina (Nip:129X;93-11:41X)
Dot blot 分析;LC-MS/MS分析;6mA-IP-Seq;6mA-IP-qPCR;6mA-RE-qPCR;RNA-seq(IlluminaHiSeq X-ten); PacBioSMRT检测6mA;CRISPR-Cas9诱变。
研究结果

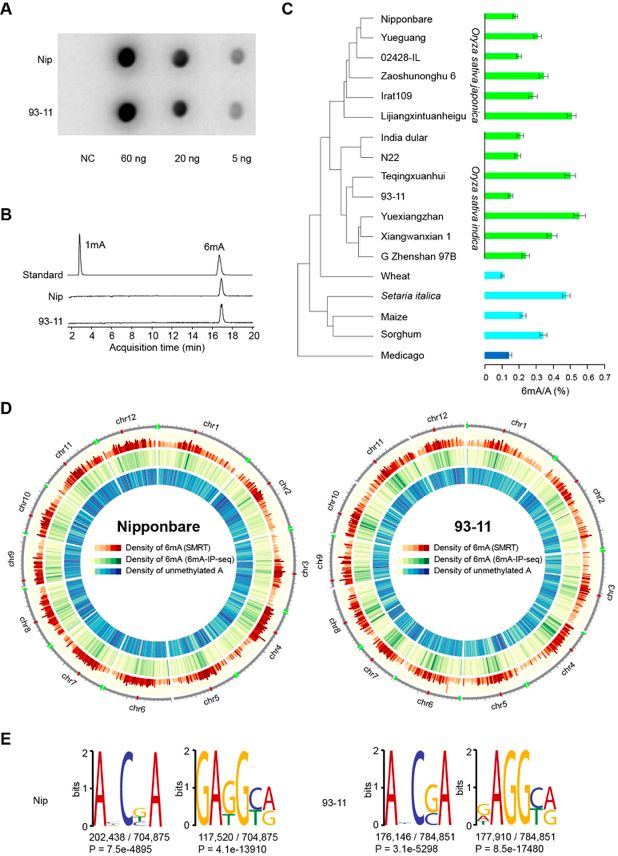
LC-MS/MS结果显示水稻幼苗的6mA含量在0.15%~0.55%之间,与小麦、玉米、高粱、小米及苜蓿相当。通过SMRT(单分子实时测序系统Single MoleculeReal Time)测序数据,在Nip和93-11中分别检测出704875个和784912个6mA位点(每条链的覆盖率≥25,质量值≥20)。超过90 %的6mA – IP – seq峰与至少一个由SMRT测序鉴定的6mA位点重叠,此外,6mA – IP – qPCR分析分别独立验证了从Nip和93- 11的12条染色体中随机选择的48个阳性和24个阴性基因座。甲基化水平高的位点显示高富集度,而甲基化水平低的位点显示低富集度。使用6mA-RE-qPCR验证了带有CATG motif的10个阳性和2个阴性的随机选择的基因组。表示了SMRT技术在6mA检测中的可靠性。
Circos图显示Nip和93-11的12条染色体中广泛分布6mA位点。6mA位点在染色体臂中部富集,尤其在着丝粒周围异染色质区域附近富集,在染色体末端附近6mA密度较低。在未甲基化的腺嘌呤中,没有观察到这种模式,这表明基因组范围的6mA分布在水稻基因组中不是随机的。Nip(ANCBA)和93-11(ANMGA)丰富的motif在两端含有两个保守的腺嘌呤,在中间含有一个胞嘧啶,类似于拟南芥的6mA motif。而第二个富集的motif类似于在秀丽隐杆线虫中鉴定的6mA motif(GAGG)(图2)。
❖ Nip和93-11的6mA甲基化基因
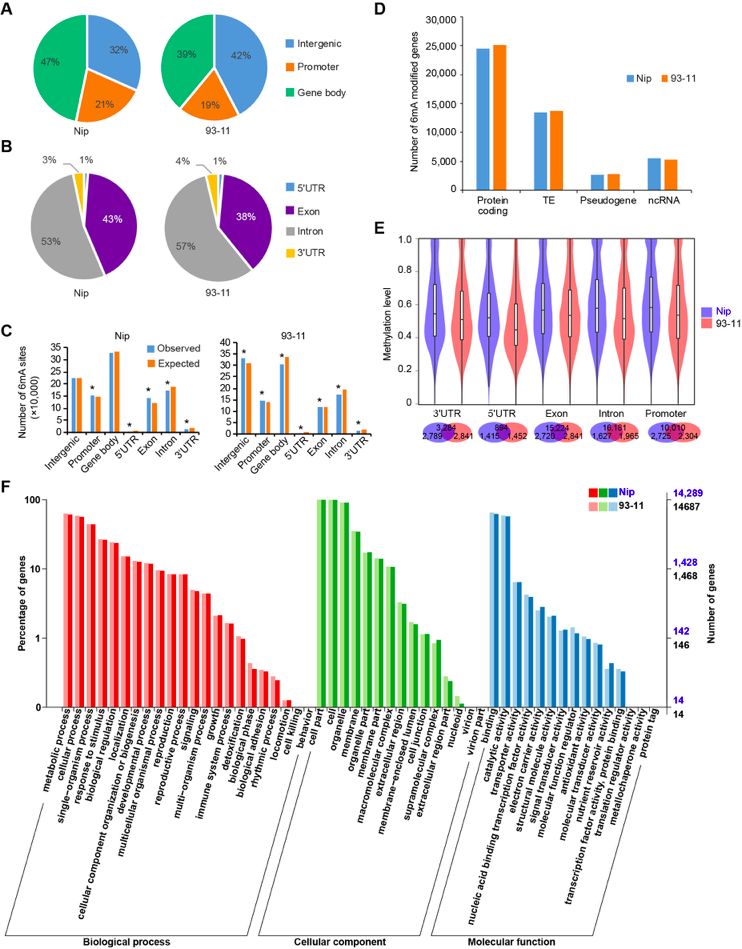
RNA-seq分析表明在Nip和93-11中,在6mA位点有大量的高表达基因甲基化,大量未甲基化基因在低水平表达。6mA甲基化基因的表达水平显著高于非6mA基因,并且高表达基因显示出较高的6mA占用率,特别是在启动子和基因体区域中包含6mA位点的基因。6mA与水稻中的活性表达基因有关。5mC在水稻基因组中高丰度存在,影响基因表达,研究发现5mC和6mA之间没有相关性(图4)。

❖ 水稻Nip、93-11和拟南芥6mA甲基体的比较

粳稻和籼稻对环境胁迫有不同的耐受性。Nip对冷和盐胁迫表现出更大的耐受性,而93-11对热胁迫表现出更大的耐受性。用LC-MS/MS分别研究了Nip和93-11幼苗在冷胁迫、热胁迫和盐胁迫下的DNA甲基化动力学,并探讨了胁迫反应差异的潜在表观遗传学基础。6mA水平在低温胁迫下明显降低,在高温或盐胁迫下显著增加,而5mC水平保持稳定。6mA水平的变化在Nip和93-11之间表现出显著的差异。水稻6mA含量与耐冷性呈负相关,与耐盐性和耐热性呈正相关(图6)。
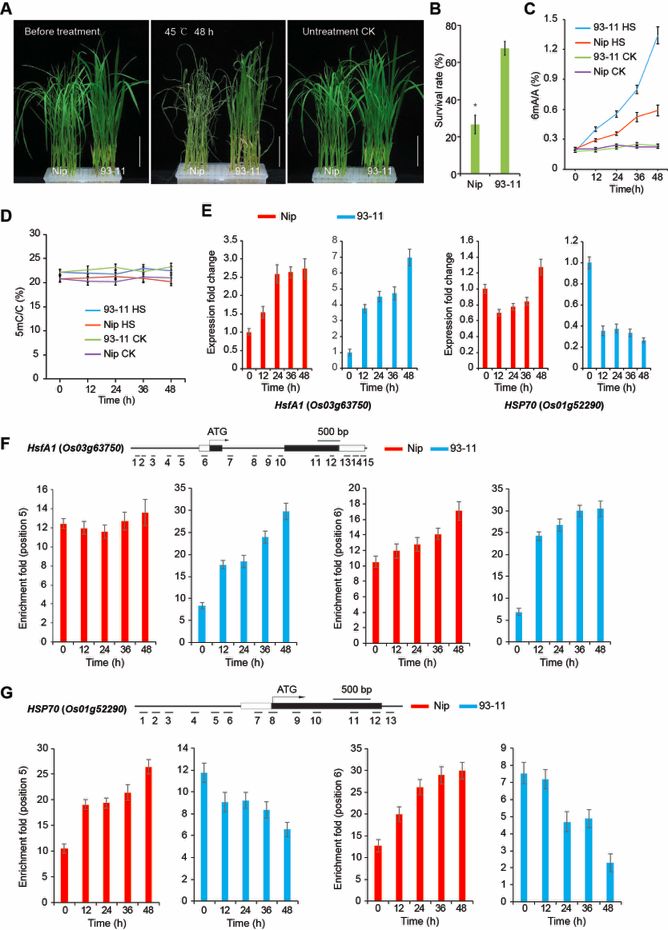
根据SMRT测序结果,筛选出候选的6mA修饰的热胁迫相关基因,如热休克转录因子A1(HsfA1)和热休克蛋白70(HSP70)。HSFA1是热胁迫反应的主要转录调控因子,其在非胁迫条件下受到HSP70的抑制。HSFA1功能缺失导致热胁迫敏感表型。HsfA1和HSP70表达的变化与其6mA水平的变化呈正相关,这可能是Nip和93-11之间热胁迫耐受性差异的原因。
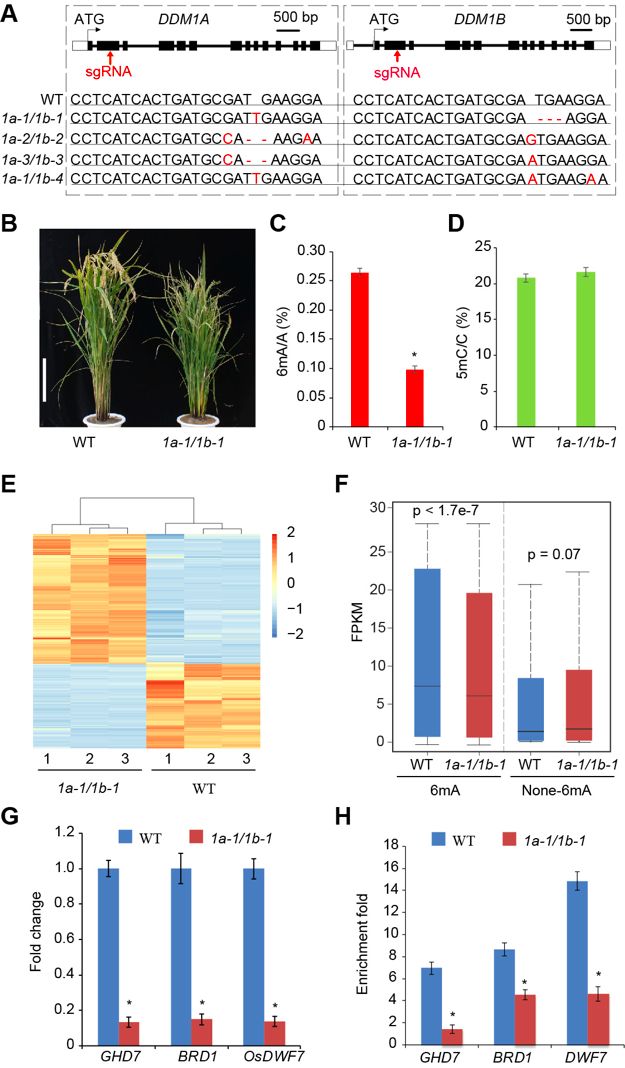
水稻基因组含有两个DDM1同源基因DDM1a和DDM1b,由于功能冗余,只有T-DNA插入单突变体产生的双突变体DDM1a/1b表现出发育表型。然而,DDM1a/1b不产生活花粉,导致种子呈空壳和深色。用CRISPR-Cas9对Nip背景中的DDM1a和DDM1b进行了有针对性的诱变,并鉴定了10个独立的T1系用于DDM1a、DDM1b单突变和4个独立的DDM1a/DDM1b(1a/1b)双突变型。在任何不同类型的DDM1a或DDM1b纯合子单突变体中均未观察到表型。与野生型植物相比,所有纯合1a/1b系表现出相同的矮化表型。1a-1/1b-1显示出降低的结实率,而另外3个双突变体显示不育。LC-MS/MS对DNA甲基化水平的定量测量显示6mA水平显著降低,但1a/1b植物中5mC水平变化不大。6mA-IPqPCR分析显示,6mA水平在大多数随机选择的位点中显著降低。RNA-seq结果表明野生型中6mA修饰基因的表达水平显著高于1a-1/1b-1植物中的相同基因,野生型中非6mA基因与1a-1/1b-1植物中的相应基因之间没有表达水平差异。结果表明6mA水平与基因表达呈正相关。
6mA-IP-qPCR证实了野生型植物SMRT测序鉴定的6mA位点,1a-1/1b-1植物中6mA水平显著降低。结果表明,抽穗期7(GHD7)、BR-缺陷矮秆1(BRD1)和DWF7的表达水平与其DDMa介导的6mA修饰相关(图7)。







 京公网安备 11011302003368号
京公网安备 11011302003368号