英文题目:Enteric dysbiosis-linked gut barrier disruption triggers early renal injury induced by chronic high salt feeding in mice
中文题目:小鼠慢性高盐喂养诱导的与肠道生态失调相关的肠道屏障破坏引起早期肾损伤
发表杂志:Experimental & Molecular Medicine
影响因子:5.063
合作单位:南方医科大学病理生理学系
01.研究背景
高血压的患病率不断增加,正在成为世界各地的主要公共卫生问题。高血压的发病机制尚不完全清楚。慢性高盐饮食相关的肾损伤是高血压发展的关键风险因素。然而,高盐摄入引发肾脏损害的机制知之甚少。
暴露于食用盐的第一个器官是肠道。肠道异常(包括肠道生态失调和肠道通透性增加)与许多肠外疾病有关。例如,饮酒可诱发肠道生态失调,并可破坏肠道屏障完整性,从而使病原体相关分子渗入血液并转移至肝脏,导致肝脏脂肪变性和进一步酒精性肝炎。基于这一理论,作者旨在研究高盐摄取是否能够直接破坏肠内稳态,并反过来引发早期肾损伤。
02.研究方法
1、取材:
• 6-8周龄雄性无病原体的C57BL / 6小鼠
• 饮用水中添加2%NaCl,连续饲喂小鼠8周,以诱导早期肾损伤
• 对于抗生素实验,将多粘菌素B(150mg / l)和新霉素(200mg / l)连续添加到NaCl饮用水中喂食8周
2、测序
• 粪便样本(盲肠内容物)或回肠/结肠粘膜层分离细菌——16S测序
• 回肠和结肠组织——转录组测序
03.研究结果
1、慢性高盐摄入导致肠道生态失调
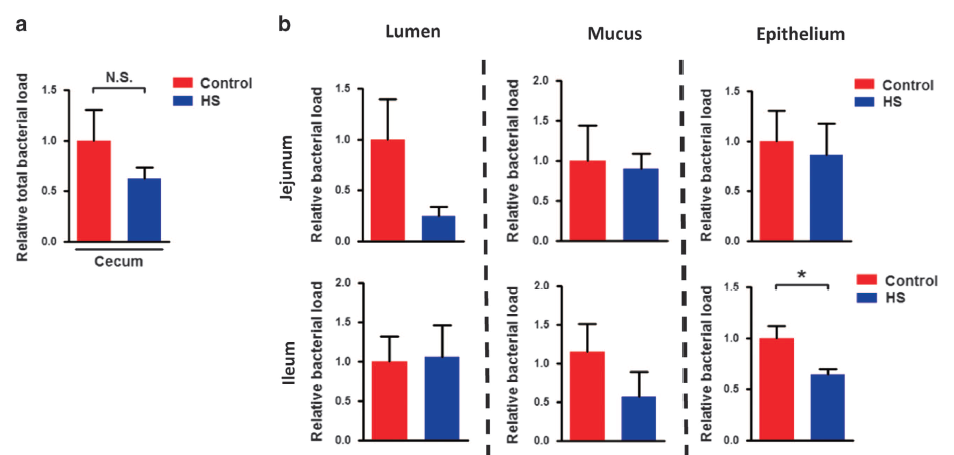
慢性高盐HS喂养后,盲肠中的总细菌负荷略微降低。分离不同部位的菌群,慢性HS喂养后,回肠上皮和结肠腔内的细菌负荷也降低。
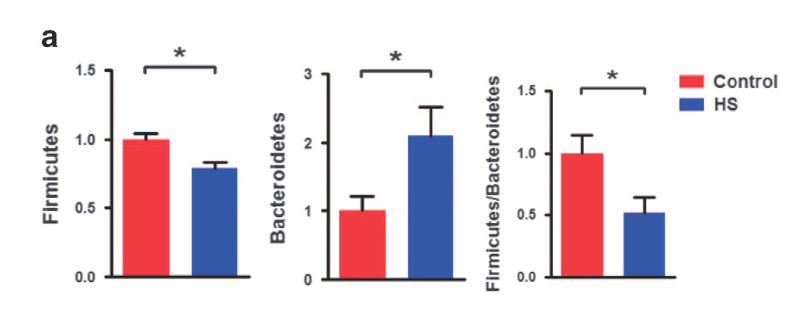
慢性HS处理显著降低厚壁菌门水平,并提高拟杆菌门的水平,这表明菌群组成在HS摄入后发生改变。
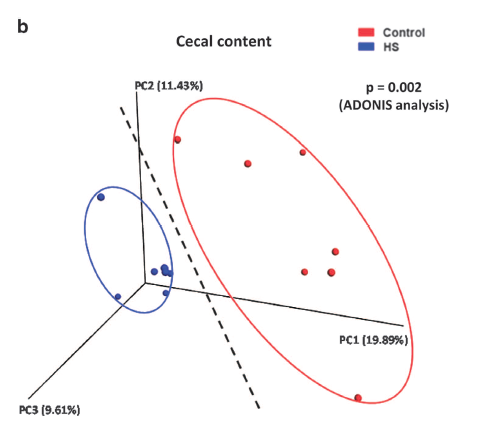
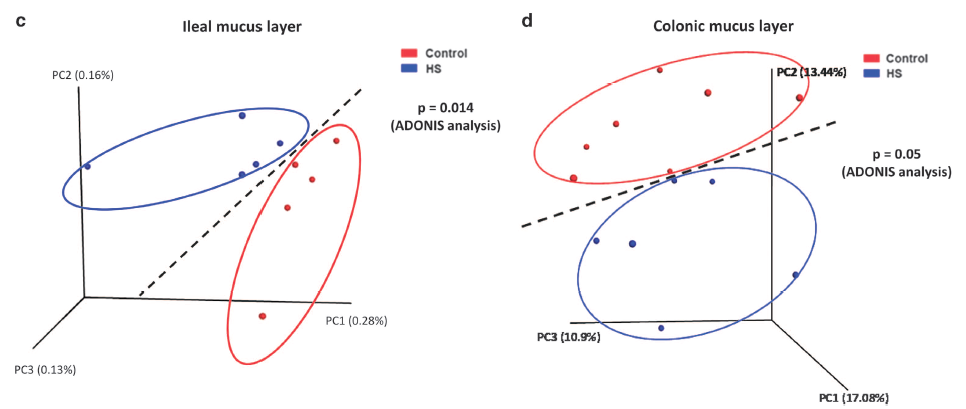
16S rRNA测序表明, HS组的盲肠内容物(cecal content)菌群组成与对照小鼠相比,在门和纲水平上明显不同。特别是在HS处理后,盲肠内容物中放线菌门和厚壁菌门中的Actinobacteria、Firmicutes和Bacteroidetes以及纲水平中的Actinobacteria,Clostridia和Bacteroidia所占比例显著改变。使用未加权的uniFrac分析的主坐标分析(PCoA)显示,HS组和对照组盲肠内容物菌群分别聚类(P = 0.002,ADONIS分析)。粘膜细菌也是影响肠道病理生理状态的重要因素,回肠粘膜( ileal mucosa)和结肠粘膜(colonic mucosa)在整个胃肠道中的细菌数量最多。因此,进一步分析了位于回肠粘膜层和结肠粘膜层的细菌。未加权的uniFrac分析显示,HS组和对照组在回肠粘液层分别聚类(P = 0.014,ADONIS分析)。而在结肠粘液层,对照组和HS组也形成两个聚类类别,分离趋势明显(P =0.05,ADONIS分析)。
2、慢性高盐喂养导致以炎性反应受损为特征的肠道异常
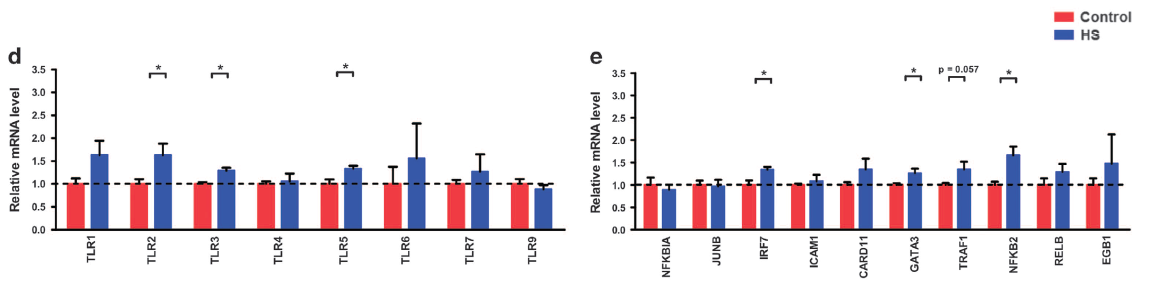
对照组和HS喂养组小鼠的回肠和结肠上皮形态无明显差异,同时,慢性HS喂养不影响肠中的细胞死亡。炎症标志物的表达随着慢性HS摄入发生显著改变。特别是,Ccl4、Ccl5和IFN-γ在HS小鼠的回肠中表现出更高的mRNA表达水平。回肠中IFN-γ免疫组织化学的结果也进一步证实了这一基因表达数据。由于TLR家族蛋白和Nf-κB是参与病原体相关免疫反应的主要分子,作者进一步评估了TLR家族和Nf-κB基因表达,发现TLR2、TLR3和TLR5 在回肠中趋于更高的mRNA表达水平。HS处理后IRF7、GATA3和NFKB2的表达显著上调。HS喂养后,回肠中CD38的表达升高。
通过二代测序进行转录组测序分析,比较对照组和HS组之间涉及“细胞因子-细胞因子受体相互作用”、“NF-κB信号通路”和“Toll样受体信号通路”的所有相关基因的表达。结果表明回肠和结肠中,两组之间许多基因的表达存在差异。
3、慢性高盐摄入导致肠道屏障功能丧失,并促进细菌移植进入肾脏
通过粪便白蛋白含量检测肠通透性,结果显示HS喂养促进肠道渗漏。同时,HS摄入显著降低结肠中的tjp-1、tjp-2、claudin-1、claudin-7和claudin-8基因表达。此外,与对照小鼠相比,HS摄入后,回肠和结肠中形成屏障的紧密连接ZO-1蛋白的表达水平显著降低以及结肠中的Occludin蛋白显示出显著较低的趋势。另一方面,在HS喂养后,回肠和结肠中“成孔”紧密连接蛋白Claudin-2蛋白的表达显著升高。这些数据清楚地表明肠道屏障被慢性HS摄入所破坏。
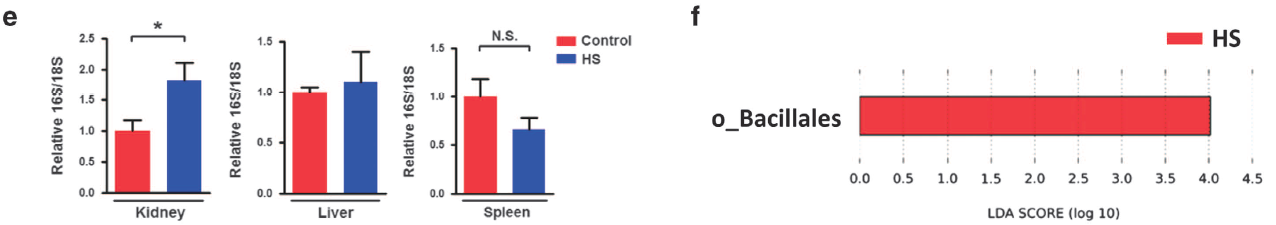
肠道通透性增加可能导致肠道细菌或细菌产物易位至肠外组织。通过使用16s PCR来识别细菌DNA,检测肾脏、肝脏和脾脏中的细菌易位。有趣的是,慢性HS摄入促进了细菌易位进入肾脏,但不会进入肝脏或脾脏。LEfSe试验结果表明,与对照组相比,HS处理的肾脏中富含属于肠道细菌的杆菌。与对照动物的肾脏相比,在HS喂养的肾脏中,芽孢杆菌(Bacillus)和游动微菌(Planomicrobium)分别增加了2.6倍和8.7倍。
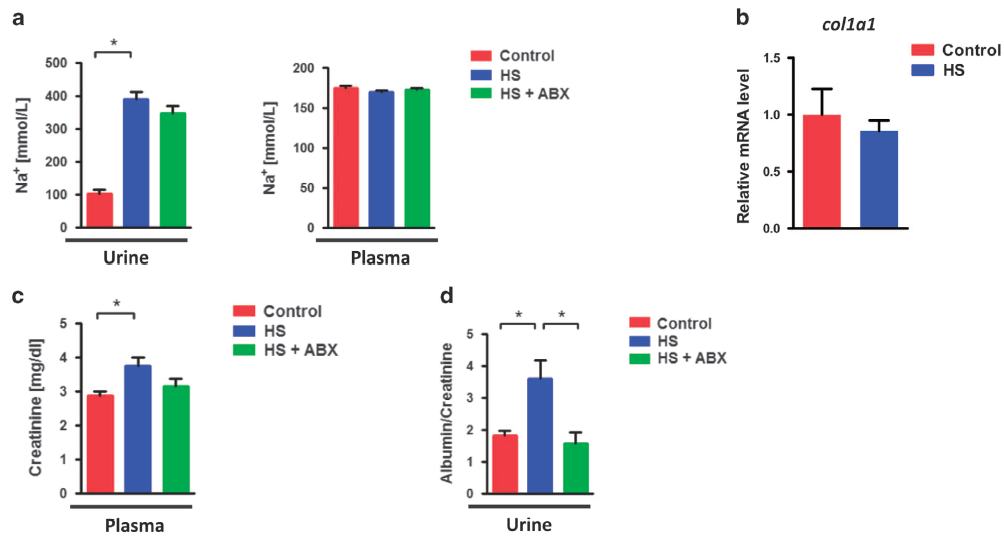
4、慢性高盐喂养相关的肠道屏障破坏和肾损伤取决于肠道微生物菌群
给予小鼠抗生素(多粘菌素B和新霉素,antibiotics,ABX)处理后,恢复了HS喂养诱导的回肠IFN-γ的过表达和肠道渗漏。通过尿和血浆Na +浓度测量,发现抗生素并不改变钠负荷。HS喂养增加了血浆肌酐(creatinine)水平,与HS治疗相比,抗生素治疗后具有较低但不显著的血浆肌酐水平。HS喂养小鼠的肾功能障碍主要标志物–尿白蛋白/肌酐比率显著增加,但抗生素治疗几乎可以完全恢复肾功能。抗生素施用还可以降低HS诱导的凋亡细胞升高。以上结果表明,抗生素治疗能够改善HS喂养引起的肠道渗漏和早期肾损伤。
5、慢性高盐喂养引起的收缩压升高取决于肠道微生物菌群
慢性HS喂养可能导致动脉压升高。 虽然HS处理的小鼠的舒张压(DBP)和平均血压没有增加,但收缩压(SBP)在慢性HS喂养后显著升高。有趣的是,抗生素治疗能够完全恢复正常SBP。这些数据强烈表明,慢性HS喂养引起的SBP升高取决于肠道微生物菌群。

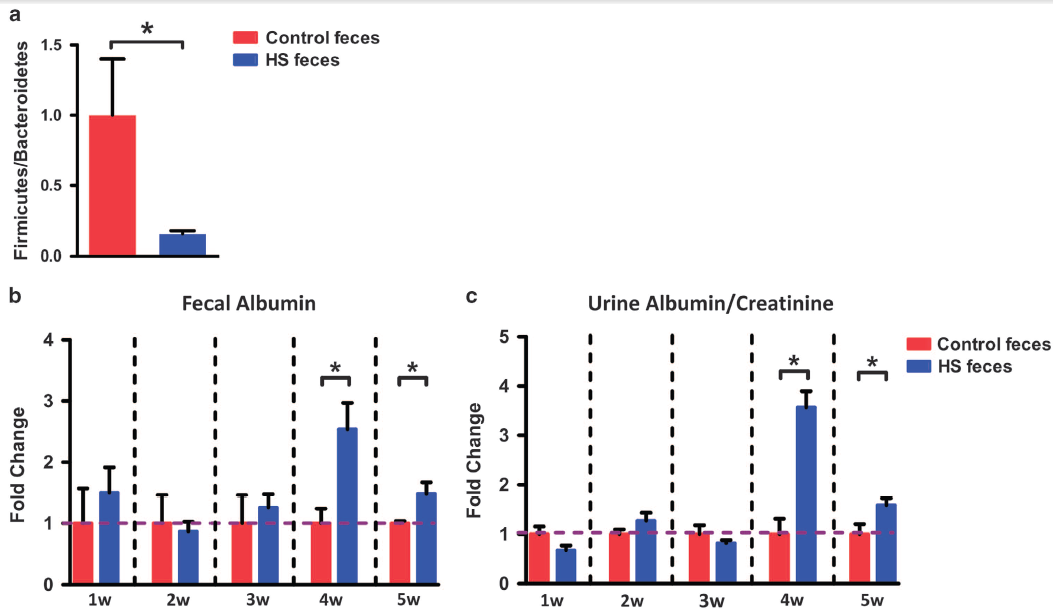
6、慢性高盐处理的小鼠的肠道微生物菌群可以独立地引起肠道泄漏和早期肾损伤
粪便微生物菌群移植实验:喂食正常饮食的两组小鼠口服来自对照和HS处理的小鼠的粪便。移植8周后,接受对照粪便的对照小鼠中的微生物菌群组成改变的主要标记物–盲肠厚壁菌/拟杆菌比例明显高于接受HS粪便的小鼠,这一点与作者之前的数据一致,表明HS喂养会降低盲肠中的厚壁菌 / 拟杆菌比例,并说明了粪便微生物菌群移植实验是成功的。给药4周后,粪便白蛋白含量检测结果表明,接受HS喂养粪便的小鼠的肠通透性显著增加。并且,尿白蛋白(albumin)/肌酸酐(creatinine)比率(在当前研究中观察到的肾功能障碍的主要表型),在移植4周后接受HS喂养的粪便的小鼠中也显著增加。最后,与对照小鼠相比,HS粪便移植小鼠中的肾脏凋亡细胞数量显著增加。
小 结
该研究通过使用依赖于微生物菌群的“肠-肾轴”理论为研究盐相关性高血压的发病机制提供了新方向。未来的工作将重点关注肠道细菌与盐诱导的高血压的发病之间的联系,将详细说明细菌的应答或细菌中的代谢途径,这些细菌参与并促进由盐诱导的肠道和肾脏病理变化,并且此文中在“肠-肾轴”中的新发现将提供潜在的高血压干预治疗目标。
参考文献
Hu, Jingjuan, et al. “Enteric dysbiosis-linked gut barrier disruption triggers early renal injury induced by chronic high salt feeding in mice.” Experimental & molecular medicine 49.8 (2017): e370.





 京公网安备 11011302003368号
京公网安备 11011302003368号