CUT&Tag测序技术
产品介绍
CUT&Tag 是蛋白-DNA互作的一大革新技术,该技术核心为 Hyperactive pG-Tn5/pA-Tn5 Transposase,该酶是将 Protein G/A 与经过工程学改造的超高活性 Tn5 转座酶进行融合,形成同时具备转座酶与 Protein G/A 活性的新型融合酶,专门适用于蛋白质-基因组互作研究的CUT&Tag 技术核心酶。
技术原理
CUT&Tag(Cleavage Under Targets and Tagmentation)是一种可应用于表观遗传学领域的DNA-蛋白质互作研究新技术,主要用于研究转录因子或组蛋白修饰在全基因组上的结合或分布位点。
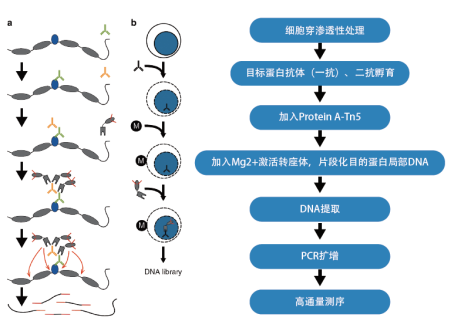
产品优势
细胞起始量低:可兼容低至60个细胞,甚至单细胞
超高活性:兼具pG/A &Tn5活性,DNA片段化活性极高
信噪比高:信噪比显著优于ChIP-Seq
实验重复性好:平行样本之间的重复性好
分析流程
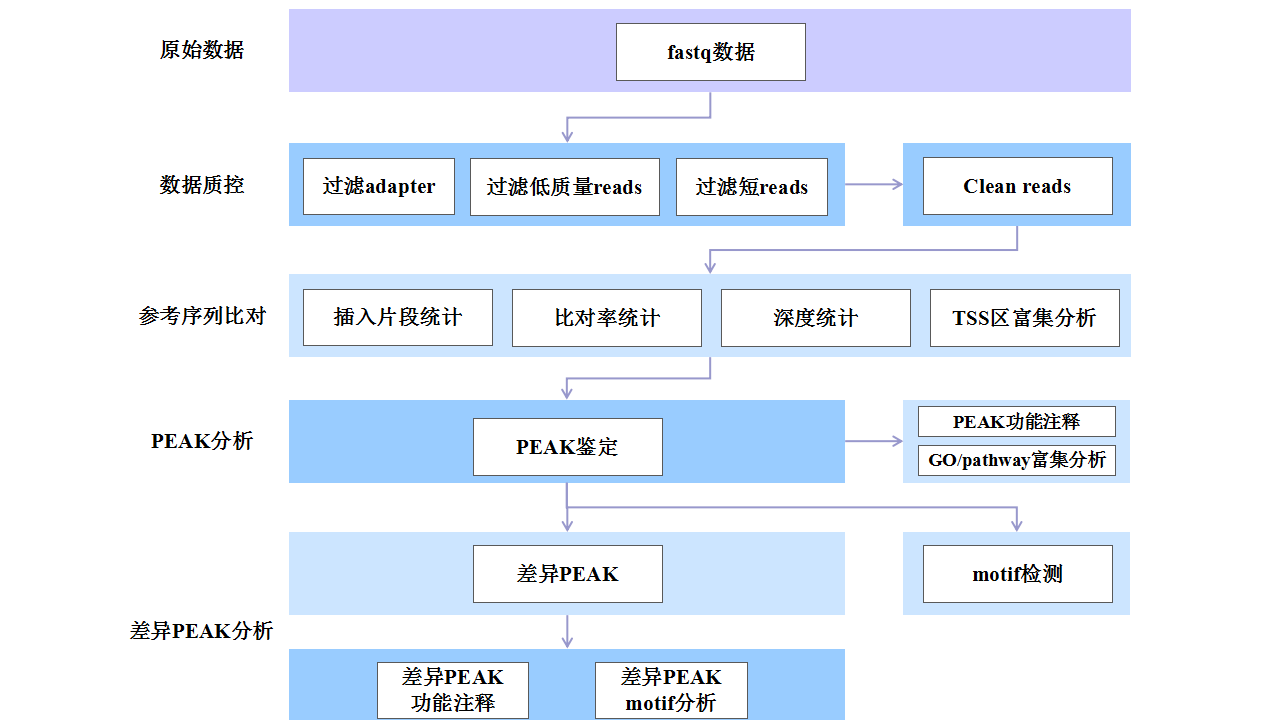
送样要求
A. 贴壁细胞 将贴壁细胞用移液器缓慢地吹/刮至悬浮状,或采用胰酶或 EDTA 消化方法制备细胞悬液。B. 悬浮细胞 确定细胞生长状态良好,细胞融合度达到 80%。
结果展示
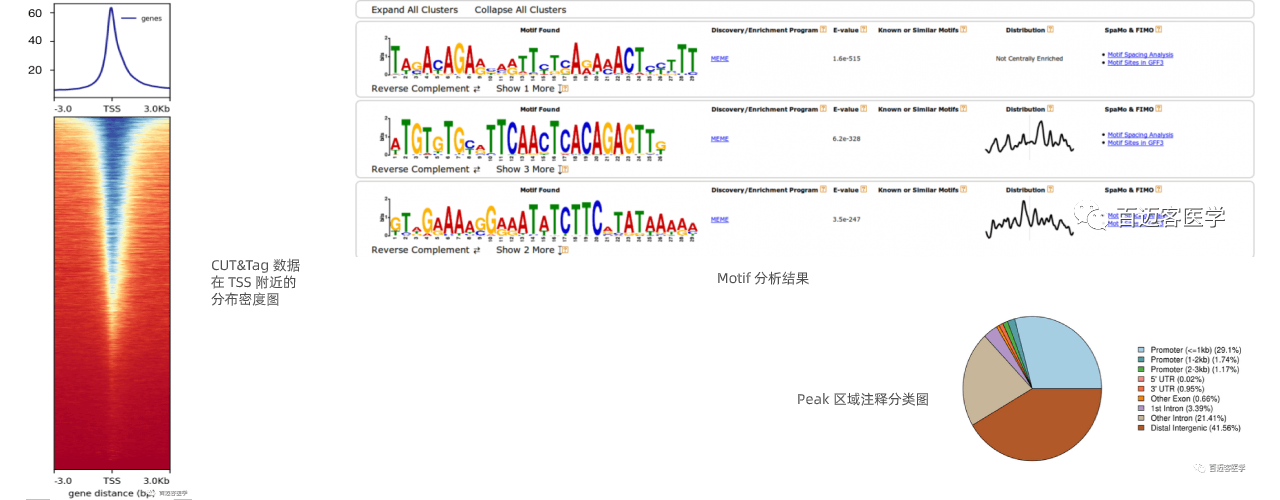
常见问题
CUT&Tag适用于什么物种?
CUT&Tag适用于哺乳动物细胞的蛋白-DNA互作研究,酵母、植物等细胞需要经过(破除细胞壁或者提取细胞核)来进行实验。CUT&Tag在哺乳动物细胞系上的应用比较成熟,动物组织经过处理得到悬浮单个细胞同样可以进行实验。
CUT&Tag适用于活细胞,对细胞状态有要求吗?
CUT&Tag在活细胞上确实成功率比较高,在准备细胞时需要保证细胞处于高细胞活性状态,若细胞活性不佳,胞内蛋白质与核酸相互作用的状态会发生改变,对于死亡的细胞,目的蛋白有可能从染色质上脱落,进而影响实验数据。在准备细胞样本时使用台盼蓝进行细胞活性的检测,建议细胞活力大于90%以上。
针对于Tn5切割开放染色质区域的特性,CUT&Tag是否更加适合于开放染色质区域的研究,异染色质上的位点是否适用?
CUT&Tag是ChIP-seq的替代技术,主要用于分析全基因组范围内的DNA-蛋白质相互作用。容易将ATAC-seq技术与CUT&Tag技术混淆,CUT&Tag技术在异染色质位点上有很好的结果,Henikoff推荐的阳性对照就是存在于异染色质区域的H3K27me3,实验数据显示在H3K27me3上有很好的结果。
做ChIP-seq的时候不需要二抗,CUT&Tag二抗的作用是什么?二抗是必须的吗?
ChIP-seq和CUT&Tag都可以研究基因组范围内的DNA-蛋白质互相作用,但是这个是两个完全不同的技术。ChIP-seq需要一抗与pA/pG 磁珠进行结合,钓取目的区域。CUT&Tag实验中的二抗作用是放大信号,在丰度很高的靶蛋白不使用二抗也可以构建出CUT&Tag文库,建议使用二抗。
做CUT&Tag实验的时候,阴性对照和阳性对照怎么设置,IgG的阴性对照有意义么?
针对抗体的阳性对照可以采用RNA Pol II/ 组蛋白,证明系统没有问题。阴性对照使用与一抗相同种属的IgG,阳性对照,阴性对照证明抗体特异,实验结果可信。
如何区分DNA提取步骤里提取到的目的区域和非目的区域?
被提取的DNA片段,只有加上了接头的DNA片段才能在后续的PCR扩增中富集,通过PCR扩增可以特异性的富集目的片段。
对于 CUT&Tag 的实验样本,二代测序上机测序平台如何选择?
使用常规的PE150即可,主流的测序平台如 HiSeq X10以及Novaseq均可。
抗体如何准备?
1)抗体(一抗和二抗)由客户提供。
2)抗体(一抗和二抗)需要是原液,不要进行稀释,每个样本需要寄送 3ul 以上的原液。
3)抗体(一抗和二抗)需要严格按照抗体的说明书进行保存和运输。
4)抗体(一抗和二抗)需说明书需要提前提交给百迈客,以方便安排后续实验。







 京公网安备 11011302003368号
京公网安备 11011302003368号